
Литература:
Лохтин Ю.Н. – Материаловедение изд. Москва. Машиностроение
Гуляев А.П. (+)– Металловедение изд. Москва. Металлургиздат.
Материаловедение под ред. Арзомасова изд. Москва. Машиностроение.
Материаловедение
Материаловедение – это наука, изучающая состав, строение и свойства материалов, зависимость свойств от состава и строения, а также закономерности их изменения от условий обработки и эксплуатации материалов.
Материаловедение устанавливает взаимосвязь между составом, структурой свойством материалов.
Существует 3 способа воздействия на структуру материала:
Термическая обработка
Химико-термическая обработка
Термомеханическая обработка
Строение металлов
Из 92 химических элементов 80 относится к металлам. При взаимодействии этих элементов с окислительными элементами все эти вещества отдают электроны. У металлов слабосвязанные с ядром внешние электроны способны отщепляться от атомов, переходить в относительно свободное состояние, образуя так называемый электронный газ. Металлическое состояние возникает в группе атомов, когда при их сближении внешние электроны теряют связь с отдельными атомами, становятся общими и легко перемещаются между катионами металлов.
Взаимодействие между положительными ионами и обобществлёнными электронами получило название металлической связи.
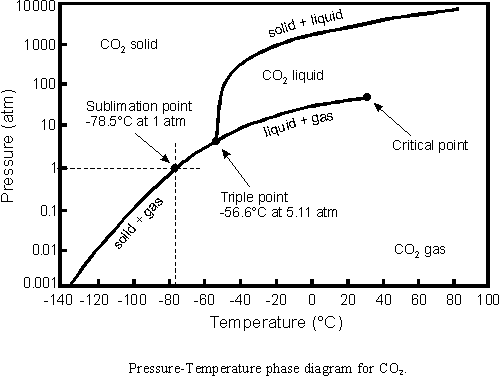
Для твёрдого состояния: En/Ek >> 1
Жидкое: En/Ek~1
Газообразное: En/Ek << 1
Твердые
вещества, в которых частицы располагаются
упорядоченно, называются кристаллическими
веществами. На ряду с кристаллическими
веществами выделяют аморфные вещества.
 Нахождение
твёрдого вещества в аморфном состоянии
невыгодно для системы энергетически.
Система стремиться к минимальному
запасу энергии.
Нахождение
твёрдого вещества в аморфном состоянии
невыгодно для системы энергетически.
Система стремиться к минимальному
запасу энергии.
Силы притяжения уменьшаются по мере притяжения частиц, в свою очередь силы отталкивания возрастают, особенно при малых расстояниях.

Для описания кристаллического строения вещества применяются следующие термины:
Кристаллографическая плоскость
Пространственная кристаллическая решётка
Элементарная ячейка
Кристаллографическая
плоскость – это воображаемые линии,
проведенные через центры атомов,
образующие решётку, в узлах которой
находятся атомы. Многократное повторение
кристаллографических плоскостей
расположенных параллельно и на
определённом расстоянии друг от друга
воспроизводит пространственную
кристаллическую решётку
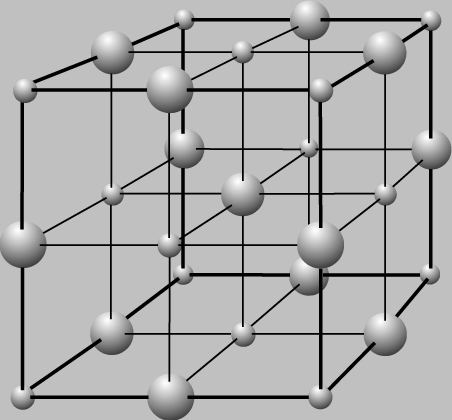
Наименьший комплекс атомов, многократное повторение которого в пространстве позволяет воспроизвести пространственную кристаллическую решётку, называется элементарной ячейкой.
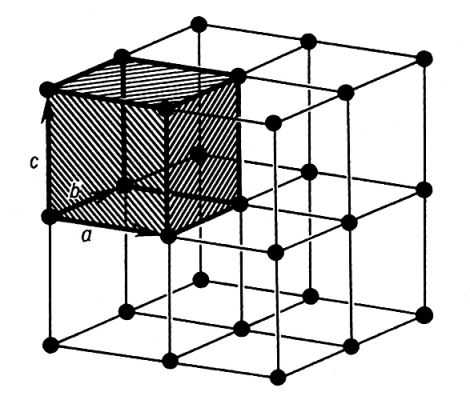 Для
оприсания элементарной ячейки необходимо
знать 6 параметров. Длины рёбер a,
b,
c
и межгранные углы альфа, бета, гамма.
Для
оприсания элементарной ячейки необходимо
знать 6 параметров. Длины рёбер a,
b,
c
и межгранные углы альфа, бета, гамма.
Большинство металлов существуют в трёх основных высокосимметричных кристаллических структурах, а именно:
Объёмно-центрированная кубическая решётка (ОЦК) (а) – представляет собой куб, в вершинах которого находятся катионы металлов и ещё один катион в центре куба (K, Li, W)
Гранецентрированная кубическая решётка (ГЦК) (б) – также представляет собой куб с катионами металлов в вершинах, а также по одному катиону в центре грани (Ni, Pt, Au)
Гексагональная плотноупакованная решётка (ГПУ) (в) – представляет собой шестигранную призму, в вершинах которой находятся катионы металлов. В центре каждого основания по катиону металлов и три катиона между основаниями (Mg, Be, Zn).
Для описания кубических структур достаточно знать величину ребра «а». Для описания гексогональной необходимо знать величину длину ребра и высоту призмы. В ГПУ отношение с/а = 1,633.

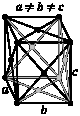
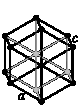
Существуют решётки, подобные кубическим, но у которых длина ребра «с» не равна длине ребра «а». Данные решётки называются тетрогональными, а отношение с/a – называется степенью тетрагональности.
Важной характеристикой кристаллической ячейки является координационное число, которое равно числу атомов, находящихся на наиболее близком и равном расстоянии от данного атома. Для ОЦК оно = 8, ГЦК и ГПУ – 12. Координационное число характеризует плотность упаковки кристаллической решётки, а именно объём, занятый атомом. Плотность упаковки ОЦК - 68%, ГЦК и ГПУ – 75%. Кристаллы имеют небольшие размеры. Металлическое изделие состоит из большого числа кристаллов (зёрен), кристаллические решётки которых сориентированы произвольным образом друг относительно друга, что обуславливает одинаковость свойств поликристаллического тела во всех направлениях, т.е. металлы характеризуются квазиизотропией (ложной изотропией).
Строение реальных кристаллов
В зависимости от размеров, дефекты кристаллической решётки делятся на:
Точечные (0d)
Линейные (1d)
Поверхностные (2d)
Объёмные (3d)
Точечные дефекты.
Наиболее распространёнными являются вакансии (атомные дырки), дислоцированные атомы, а также примесные атомы. Вакансии (а) представляют собой незаполненные узлы кристаллической решётки (всегда существуют в металле при температуре выше 0 К).

Дислоцированный атом (б) – представляет собой атом, находящийся в междоузлье кристаллической решётки.
Технически чистые металлы наряду с атомами основного металла всегда содержат различные примеси. Бывают примесные атомы замещения (б), в том случаи, когда атом примеси замещает атом основного металла в узле кристаллической решётки. В этом случаи параметр кристаллической решётки может уменьшаться или увеличиваться т.к. размер атома примеси отличается от размера атома основного металла.
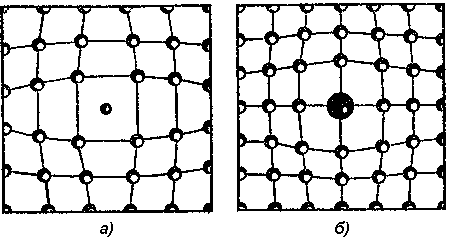
Искажение кристаллической решётки примесными атомами: а) внедрение б) замещение
Также существуют примесные атомы внедрения (а). В этом случаи атом примеси занимает место в междоузлье, в этом случаи параметр решётки увеличивается независимо от размера атома примеси.
Линейные (1d) дефекты – имеют большую протяжённость в одном измерении и малую в двух остальных. К данному типу дефектов относятся дислокации, которые бывают краевыми и винтовыми.
Краевая дислокация – представляет собой полуплоскость, внедрившуюся в кристаллическую решётку.
К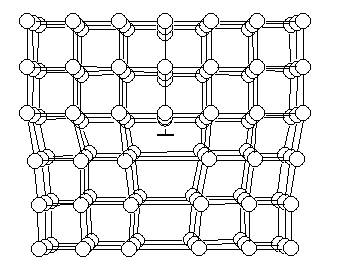 раевые
дислокации, располагающиеся над
плоскостью скольжения называются
положительными и обозначаются как на
рисунке (слева).
раевые
дислокации, располагающиеся над
плоскостью скольжения называются
положительными и обозначаются как на
рисунке (слева).
Под плоскостью скольжения их называют положительными и обозначают буквой «Т» Винтовые дислокации – линия, вокруг которой атомные плоскости изогнуты по винтовой поверхности (бывают левые и правые).

Дислокации притягивают чужеродные атомы, скопления примесных атомов внедрения около дислокации называется облаком или атмосферой Котрелла.
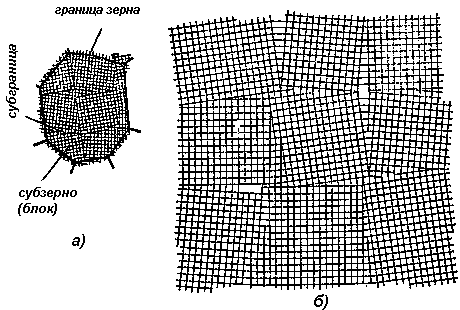
Поверхностные (2d) дефекты – представляют собой границы раздела между различными кристаллами (зёрнами), а также границы, разделяющие участки кристалла с различной ориентировкой. В кристаллах кристаллические решётки разориентированны друг относительно друга на десятки градусов.
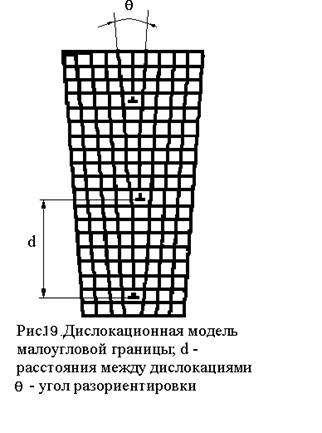
В пределах зерна структура является неидеальной, кристалл состоит из блоков, угол разориентировки которых составляет несколько минут. Границы блоков представляют собой скопление краевых дислокаций.
В объёме блока структура практически идеальная, если не учитывать наличие точечных дефектов. Блоки объединяются в более крупные агрегаты, называемые фрагментами, угол разориентировки составляет несколько градусов.
К объёмным дефектам относят дефекты, которые имеют большую протяжённость в трёх измерениях (поры, трещины, неметаллические включения).
Формирование структуры металлов и сплавов при кристаллизации
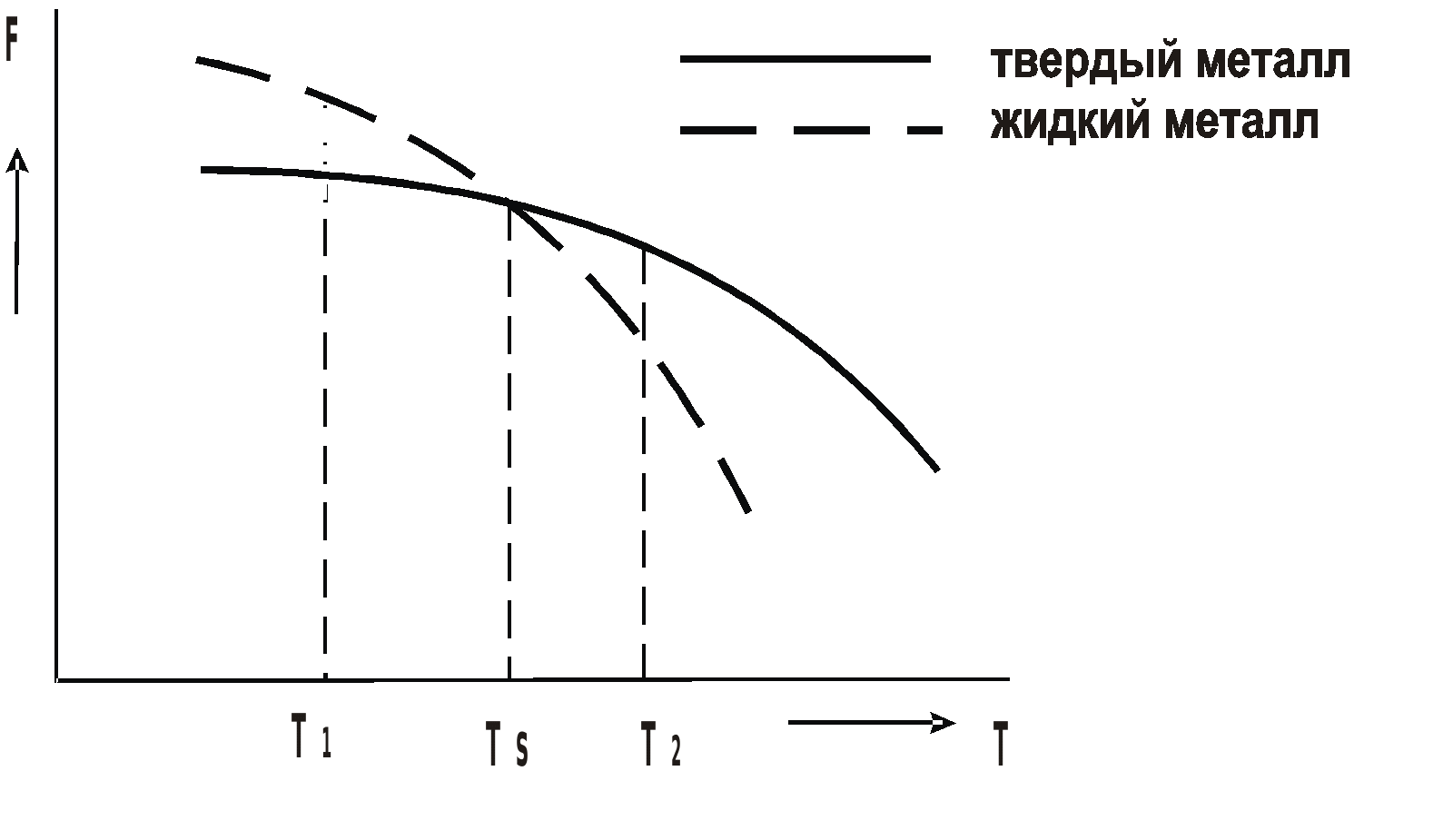
- где точка пересечения графиков есть равновесная температура.
Для каких-то данных условий процесс кристаллизации будет происходить при какой-то температуре Тк, вследствие того, что мы будем иметь выигрыш в свободной энергии.
Разность между равновесной температурой и реальной температурой кристаллизации называется степенью переохлаждения
Процесс перехода металла из жидкого в кристаллическое состояние можно описать с помощью кривых охлаждения в координатах «температура»/«время». Величина степени переохлаждения зависит от скорости охлаждения.
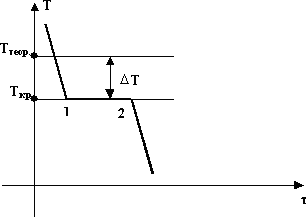
При охлаждении с большей скоростью кривая будет более «крутой».
Процесс кристаллизации состоит из двух элементарных процессов:
Образование «зародышей» (центров кристаллизации)
Рост кристаллов из образовавшихся центров кристаллизации
Механизм самопроизвольного образования центров кристаллизации. В жидком металле имеет место ближний порядок, т.е. упорядоченное расположение атомов, распространяющиеся на небольшое расстояние. Вследствие тепловой подвижности атомов ближний порядок неустойчив. При температурах, близких к температуре кристаллизации, происходит образование участков, в которых атомы расположены так же, как в кристаллах. Данные группировки называются фазовыми флуктуациями. При определённых условиях фазовые флуктуации могут стать центрами кристаллизации. Для этого фазовая флуктуация должна иметь размер больше критического.
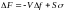
V = объём фаз. дол.
f = разность свободных энергий жидкого и твёрдого состояния
S = суммарная величина поверхности раздела
Сигма – поверхностное натяжение

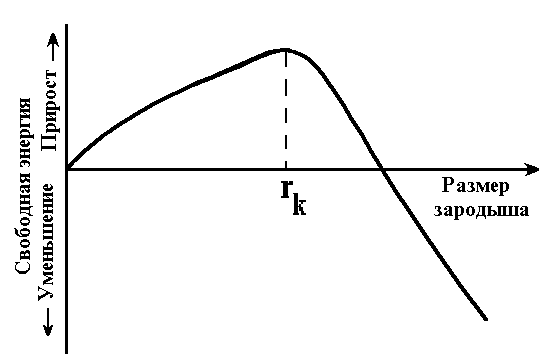
Минимальный размер зародыша (Rk) – способного к росту при данных температурных условиях называется критическим размером зародыша, а сам зародыш – критическим или равновесным. Минимальный размер зародыша зависит от степени переохлаждения. Т.к. разность или выигрыш в свободной энергии при увеличении степени переохлаждения возрастает, то критический размер зародыша – уменьшается.
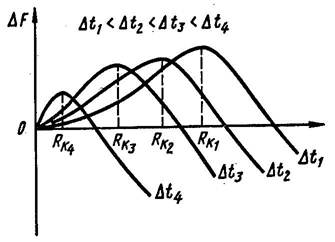
С увеличением степени переохлаждения размер критического зародыша уменьшается, что приводит к резкому увеличению числа центров кристаллизации. Все зародыши, размером меньше критического в результате теплового движения атомов растворяются в жидкой фазе.
С целью получения мелкозернистой структуры в расплавы вводят вещества, называемые модификаторы. Бывают модификаторы первого и второго рода:
Модификаторы первого рода - труднорастворимые вещества, играющие роль готовых центров кристаллизации
Модификаторы второго рода - поверхностно активные вещества (ПАВ), которые адсорбируются на поверхности и в центрах кристаллизации и препятствуют его растворению в жидком металле
