
- •21. Механические и конформационные свойства мембран. Фазовые переходы.
- •Раздел 5. Транспорт веществ и биоэлектрогенез
- •22. Транспорт неэлектролитов через мембраны. Диффузия: движущая сила. Закон Фика. Понятие об облегчённой диффузии.
- •23. Транспорт ионов через мембрану. Механизмы и движущая сила пассивного транспорта. Уравнение электрохимического потенциала.
- •24. Энергия иона и причины её понижения при транспорте через биомембраны.
- •26. Электродиффузная теория транспорта ионов через мембрану. Уравнение Нерста-Планка для потока ионов через мембрану. Уравнение Гольдмана.
- •27. Индуцированный ионный тран-т через мембрану.Затраты энерг. По формуле Борна.
- •25. Электрические свойства биомембран и транспорт ионов. Понятие о двойном электрическом слое. Плотность распределения ионов в зависимости от расстояния. Электрокинетический потенциал мембраны.
- •29. Ионный транспорт в каналах. Понятие об энергетическом профиле канала. Уравнение силы тока, переносимого ионами.
- •30. Зависимость энергетического профиля ионного канала от заполнения канала, от биоэлектрических процессов. Селективность каналов.
- •31. Общие свойства ионных каналов нервных волокон. Na-канал, к-канал, их селективность.
- •32. Функционирование ионных каналов в зависимости от от внешнего электрического потенциала, понятие воротного устройства.
- •33. Активный транспорт ионов. Перенос ионов за счет энергии атф. Схема работы каналов.
- •34. Сопряжение ионообменных процессов с гидролитическим расщеплением молекулы атф. Конформационные переходы Na, k- атФазы.
- •35. Транспорт протонов в энергосберегающих мембранах. Образование градиента электрохимических потенциалов в биомембранах.
- •36. Потенциал покоя. Формула Нерста для мембранного потенциала. Уравнение Томаса.
- •37. Потенциал действия. Мембранный потенциал и изменение ионной проницаемости мембраны. Описание ионных токов в модели Ходжкина-Хаксли.
- •38. Образование воротных токов в мембранах нервных волокон. Распространение электрического импульса в нервных волокнах.
- •39.Фотопревращение бактериородопсина. Строение бактериородопсина, конформационные переходы молекулы при поглощении кванта света. Внутримолекулярный перенос протона.
- •40. Фотоизомеризация родопсина в фоторецептурной мембране зрительных клеток позвоночных. Проницаемость мембраны и светоиндуцированный электрический сигнал
- •Фоторегуляторные и фотодеструкционные процессы Фоторегуляторные реакции
- •41. Ультрафиолетовое излучение и фотодеструкционные процессы в днк: фотоизомеризация, фотогидротация, образование пиримидиновых аддукатов. Механизмы фотореактивации.
- •42.Действие ультрафиолетового излучения на белки, на биомембраны.
31. Общие свойства ионных каналов нервных волокон. Na-канал, к-канал, их селективность.
В нервных волокнах наиболее полно охарактеризованы два типа каналов: Na+ - канал и К+ - канал.
Входящий и выходящий потоки Na+ в Na+ - канале независимы. В энергетическом профиле – высокий центральный барьер (рис. 5.7, кривая 1). Однако проводимость канала зависит от рН среды, протонирование кислотной группы блокирует канал. При физиологических значениях рН состоянию канала с депротонированной группой более соответствует профиль, в котором центральный энергетический барьер расщеплен на два (рис. 5.7, кривая 2). Протонированный центр притягивает катионы, облегчая вход в канал, одновременно затрудняется выход из потенциальной ямы, который может облегчится, когда в боковом участке связывания появляется второй катион. Электростатическое отталкивание способствует выходу первого катиона, второй катион может заполнить центральную яму.

Рис. 5.7. Энергетические профили натриевого и калиевого каналов возбудимых мембран: 1 и 2 — альтернативные модели Na+ -канала (Рубин, 2004).
При транспорте К+ наиболее медленная стадия – переход через границу мембраны. Канал все время находится в заполненном «двухчастичном» состоянии. Выход иона в раствор сопровождается сдвигом ионов по всему каналу. Число ям – два, поэтому порядок транспорта увеличивается вдвое. К+ - каналы содержат широкое устье со стороны мембраны, которое может блокироваться со стороны цитоплазмы (рис. 5.8.).

Рис. 5.8. Калиевые каналы аксона (I) и саркоплазматического ретикулума (II):
1—широкое устье диаметром около 1 нм, 2 — узкая часть поры, 3 — критическое сужение (селективный фильтр), штриховыми линиями показан возможный внешний участок связывания тетраэтиламмония, 4 — белковый компонент, 5—липидный бислой, о, i — соответственно внешняя и внутренняя стороны мембран (Рубин, 2004).
Ион К+ эффективно взаимодействует со всеми атомами кислорода в стенках поры (рис. 5.7), его энергия в поре незначительно больше, чем в воде.
Ион Na+ эффективно связывается только с двумя атомами кислорода в селективном центре, энергия его выше чем в воде, поэтому он не проходит через селективный центр К+ - канала.
32. Функционирование ионных каналов в зависимости от от внешнего электрического потенциала, понятие воротного устройства.
Открывание каналов в нервных волокнах происходит при изменении внешнего электрического потенциала и обеспечивается специальным молекулярным «воротным» устройством. Воротное устройство открывается с помощью управляющего сенсора, чувствительного к внешнему электрическому полю (рис. 5.9).
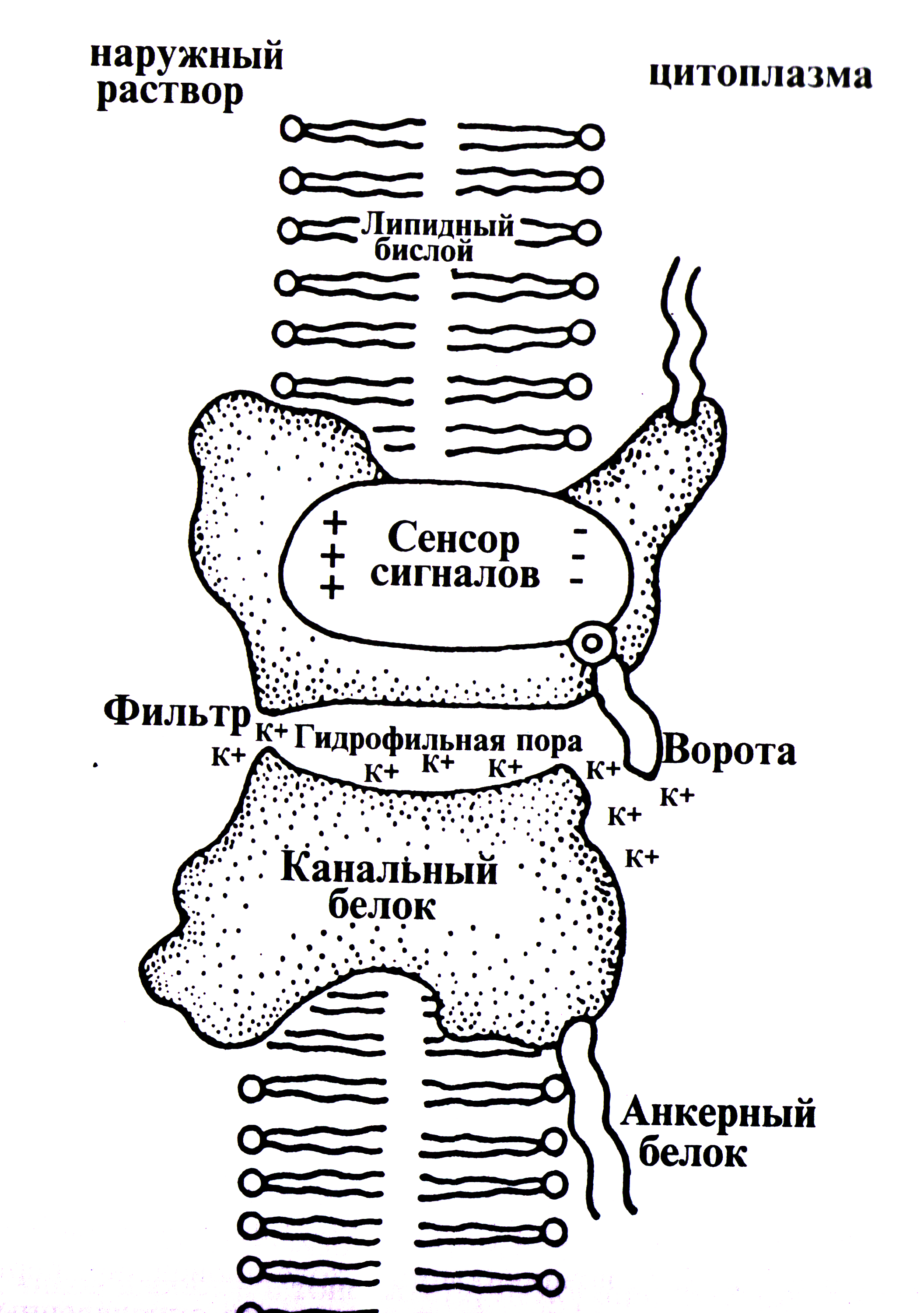
Рис. 5.9. Схематическое изображение ионного канала
«Тело» канала состоит из трансмембранного белка, погруженного в липидный бислой. Макромолекула включает 1900-4000 аминокислотных остатков, уложенных в одну или несколько полипептидных цепей, а также несколько сот сахарных остатков, ковалентно связанных с аминокислотами.
Внутренняя поверхность поры включает в основном гидрофильные аминокислоты.
Для открывания и закрытия ворот канала требуется обратимое изменение конформации белка. Вероятность открытия и закрытия определяется состоянием сенсора, который содержит несколько заряженных групп, двигающихся под влиянием мембранного электрического поля.
Na+ - канал под действием деполяризующего импульса быстро открывается, после прекращения действия импульса – быстро закрывается. В К+ - канале ток быстро увеличивается при деполяризующем импульсе, инактивация - более медленная.
Молекулярное строение каналов. Для выяснения механизмов активации и инактивации каналов необходимо знание структуры макромолекул, входящих в состав канала.
Ацетилхолиновый рецептор в нервно-мышечных соединениях позвоночных.
Нервный импульс вызывает освобождение в синаптическую щель ацетилхолина, который связывается в мембране с рецептурными молекулами белка. Происходит деполяризация мембраны (до 0 мВ), открытие Na – каналов, возникновение потенциала действия в мышечном волокне.
Ацетилхолинэстераза гидролизует ацетилхолин до ацетата и холина.
Ацетилхолиновый рецептор (белок) встроен в мембрану, содержит сегменты М1 – М4 (рис. 5.10). Полипептидная цепь пересекает мембрану 4 раза, сегменты уложены в α-спиральные структуры, в каждом из них 430-500 аминокислот. Пора (канал) образована сигментом М2.

Рис. 5.10. Предполагаемая типология отдельной субединицы ацетилхолинового рецептора
2. Na-, K-, Ca-каналы.
Белки Na-, Ca- каналов состоят из 4 повторов по 300-400 аминокислот, каждый из них включает 6 трансмембранных α-спиральных сегментов (S1-S6) (рис. 5.11). Сегмент S4 несет положительные заряды и играет роль сенсора в воротном механизме канала. Пора образуется между сегментами.
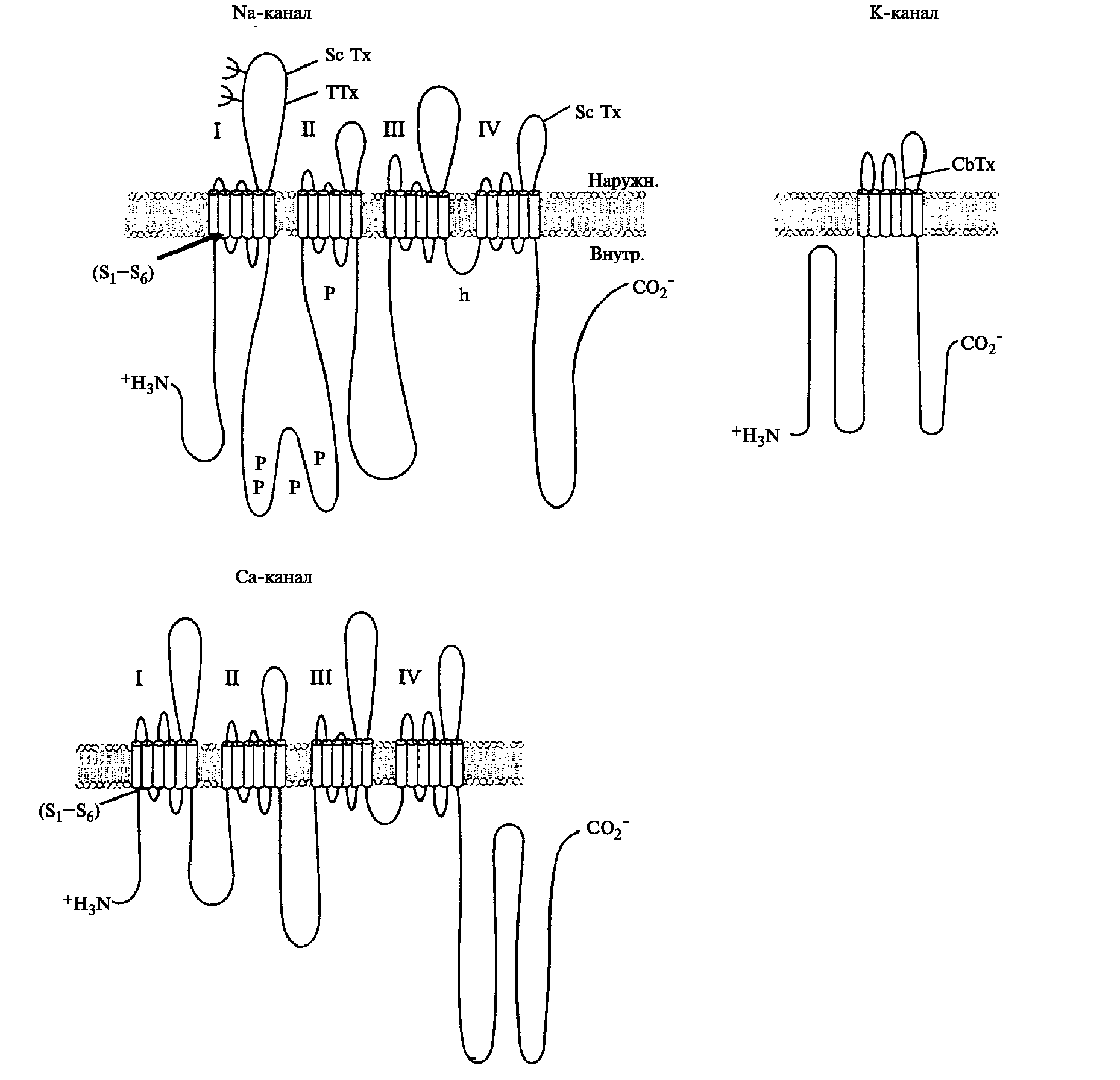
Рис. 5.11. Предполагаемое внутримембранное расположение пептидных цепей главных субъединиц потенциалзависимых ионных каналов (Рубин, 2004).
Мембранные фрагменты обозначены индексами I, II, III и IV. Показаны также участки, в которых располагаются гликозидные группы (ψ), участки фосфорилирования Р, а также зоны взаимодействия с токсинами скорпиона (ScTX), харибдотоксином (СbТХ), сенсор напряжения (+) и функциональный блок (n), ответственный за инактивацию проводимости.
K-канал имеет один сегмент с положительными зарядами (рис. 5.11). Пора образована в пептидной петле между S5 и S6 сегментами.
Механизмы блокировки каналов. Существует два типа блокировки:
Связывание агента непосредственно в поре канала, что препятствует прохождению иона.
Связывание агента с изменением конформации поры, что препятствует открыванию канала.
Фармакологические агенты - блокираторы, подавляющие возникновение потенциала действия и блокирующие селективно натриевый ток: тетродотоксин, сакситоксин, тетраэтиламмоний. Имеют большое значение в исследовании ионной проводимости. Тетродоксин ТТХ содержится в органах некоторых рыб, подавляет возникновение потенциалов действия в органах и мышцах, подавляет натриевый ток. Сакситоксин STX – содержится в жгутиковых, селективно подавляет калиевый ток.
Есть ферменты, повреждающие структуры, ответственные за инактивацию канала и расположенные снаружи канала и в области ворот.
