
- •1.10 Распределение Максвелла
- •Из выражений (1.10.5) и (1.10.6) следует, что
- •Это позволяет записать соотношение (1.10.15) в виде
- •Умножим обе части (1.10.20) на υхd υх . В результате будем иметь
- •1.12. Распределение Максвелла для относительных скоростей
- •1.13 Распределение Больцмана
- •Распределение Максвелла-Больцмана
- •1.14 Экспериментальная проверка распределения молекул по абсолютным значениям скорости
- •Глава 7. Жидкости
- •7.1. Общие свойства
- •8.5. Квантовая теория теплоемкости атомарных кристаллических тел по Эйнштейну
1.10 Распределение Максвелла
В газе, находящемся в равновесии при температуре T , скорость любой молекулы из-за столкновений непрерывно меняется как по абсолютной величине, так и по направлению. Распределение по направлениям движения в состоянии равновесия равновероятно. Если бы это было не так, то в каком-то направлении в газе двигалось бы большее число молекул, чем в другом. В результате возник бы макроскопический поток газа и газ не находился бы в равновесии.
Иначе обстоит дело с абсолютными значениями скоростей молекул: они не будут равновероятны, т.е. функция плотности вероятности F(υ) принимает неодинаковые значения при различных скоростях молекул. При этом, наибольшее число молекул будет группироваться около некоторой средней скорости, к примеру, около средней квадратичной υкв , которая на основании формулы (1.8.7),
![]() (1.10.1)
(1.10.1)
Очень большие, а также весьма малые скорости молекул, по сравнению со средней квадратичной, маловероятны. В самом деле, чтобы молекула могла приобрести при столкновениях очень большую скорость, ей необходимо испытать подряд много таких столкновений, при которых она в основном получает энергию, и почти ни одного столкновения, при котором она ее теряет. Но такие столкновения, очевидно, маловероятны. Поэтому значения функции F(υ) при малых и больших скоростях должны быть малы.
Функция F(υ) в равновесном состоянии газа не должна зависеть от времени. В самом деле, если бы функция распределения зависела от времени, то средняя квадратичная скорость, определяемая по формуле,
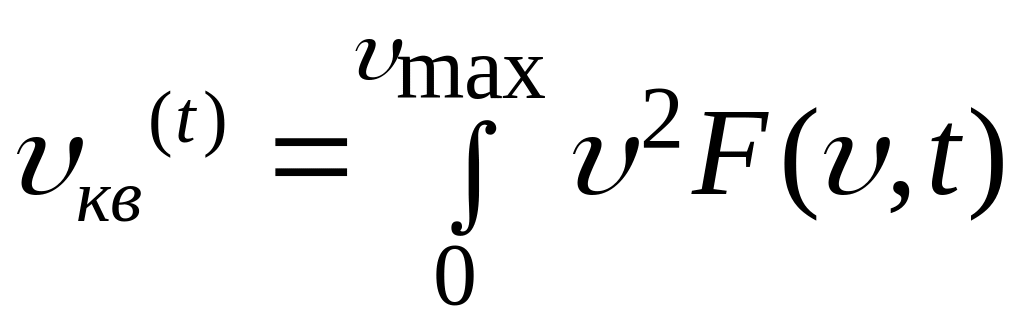 ,
,
также зависела бы от времени. Но это противоречит тому, что в состоянии равновесия (T = const), как видно из (1.10.1), υкв =сonst. Таким образом, из общих соображений, распределение молекул по скоростям должно иметь максимум около среднего квадратичного значения скорости и убывать до нуля от этого максимального значения в сторону больших скоростей молекул. Найдем, следуя Максвеллу, явный вид этой функции.
Спроектируем скорости всех N молекул газа на ось x. Вероятность того, что произвольно взятая молекула имеет проекцию скорости, заключенную в интервале ( υx , υx+dυx)
 ,
(1.10.2)
,
(1.10.2)
где
![]() -
число молекул в газе, которые имеют
проекцию скорости, заключенную
в интервале (
υx
, υx+dυx).
С другой стороны эта вероятность может
быть выражена через плотность вероятности
φ
(υx_)
(см. формулу А.22 Приложения А)
-
число молекул в газе, которые имеют
проекцию скорости, заключенную
в интервале (
υx
, υx+dυx).
С другой стороны эта вероятность может
быть выражена через плотность вероятности
φ
(υx_)
(см. формулу А.22 Приложения А)
![]() (1.10.3)
(1.10.3)
Сравнивая выражения (1.10.2) и (1.10.3) , находим
![]() (1.10.4)
(1.10.4)
Аналогичные соотношения могут быть записаны для проекций скоростей молекул на оси Y и Z.

Важно
отметить, что функции
![]()
![]()
![]() имеют
совершенно одинаковый вид из-за
равновероятности всех направлений
движения молекул и отличаются только
обозначением аргумента.
имеют
совершенно одинаковый вид из-за
равновероятности всех направлений
движения молекул и отличаются только
обозначением аргумента.
Запишем, далее, вероятность того, что случайно "взятая" молекула имеет проекции скорости, заключенные в интервалах
(υx
, υx+dυx),
(υy
, υy+dυy)
и (
υz
, υz+dυz)
или, тоже самое, что эта молекула
движется в направлении, близком к
направлению, определяемом вектором
![]() .
Пo
определению вероятности, она равна
.
Пo
определению вероятности, она равна
 (1.10.5)
(1.10.5)
где
![]() - число молекул, компоненты скорости
которых лежат в
указанных выше интервалах. Если обозначить
совместную плотность вероятности
проекций скорости молекул через
- число молекул, компоненты скорости
которых лежат в
указанных выше интервалах. Если обозначить
совместную плотность вероятности
проекций скорости молекул через
![]() ,
то та
же вероятность (1.10.5), может быть
представлена в виде:
,
то та
же вероятность (1.10.5), может быть
представлена в виде:
![]() (1.10.6)
(1.10.6)
