
- •Содержание
- •Правила и порядок работы в химической лаборатории
- •Теоретическое введение
- •Экспериментальная часть
- •Теоретическое введение
- •Экспериментальная часть
- •Теоретическое введение
- •Экспериментальная часть
- •Теоретическое введение
- •Экспериментальная часть
- •Теоретическое введение
- •Экспериментальная часть
- •Теоретическое введение
- •Экспериментальная часть
- •Теоретическое введение
- •1.2 Реакция с едкими щелочами NaОн или kон:
- •Экспериментальная часть.
- •Теоретическое введение
- •Экспериментальная часть
- •Теоретическое введение
- •4.1 Взаимодействие с дифениламином (с6н5)2nн.
- •5.1 Взаимодействие с н2sо4
- •Экспериментальная часть
- •Теоретическое введение
- •4.1 Взаимодействие с дифениламином (с6н5)2nн.
- •5.1 Взаимодействие с н2sо4
- •Экспериментальная часть
- •Обнаружение анионов
- •Обнаружение катионов
- •Теоретическое введение
- •Экспериментальная часть
- •Контрольные вопросы
- •Теоретическое введение
- •Контрольные вопросы
- •Теоретическое введение
- •Экспериментальная часть
- •Контрольные вопросы
- •Теоретическое введение
- •Экспериментальная часть
- •Контрольные вопросы
- •Теоретическое введение
- •Экспериментальная часть
- •Контрольные вопросы
- •Теоретическое введение
- •Определение кислотности квашенных овощей
- •Vрассол
- •Определение кислотности муки
- •Экспериментальная часть
- •Vрассол
- •Контрольные вопросы
- •Теоретическое введение
- •1. Определение кислотности молока
- •2.Определение кислотности хлеба
- •Экспериментальная часть
- •Данный опыт выполнить для пшеничного и ржаного хлеба. Сделать вывод о соответствии кислотности хлеба норме. Контрольные вопросы
- •Теоретическое введение
- •Экспериментальная часть
- •Контрольные вопросы
- •Теоретическое введение
- •Экспериментальная часть
- •Теоретическое введение
- •Экспериментальная часть
- •Контрольные вопросы
- •Теоретическое введение
- •Экспериментальная часть
- •Контрольные вопросы
- •Теоретическое введение
- •Экспериментальная часть
- •Контрольные вопросы
- •Теоретическое введение
- •Экспериментальная часть
- •Контрольные вопросы
- •Теоретическое введение
- •Экспериментальная часть
- •Контрольные вопросы
- •Теоретическое введение
- •Основные закономерности электролитной коагуляции:
- •Экспериментальная часть
- •Контрольные вопросы
- •Теоретическое введение
- •Экспериментальная часть
- •Контрольные вопросы
- •Теоретическое введение
- •Экспериментальная часть
- •Контрольные вопросы
- •Растворимость солей, кислот и оснований в воде
Теоретическое введение
К VI группе катионов относят: NН4+, К+, Na+. Группового реактива на VI группу катионов не существует. Катионы определяют с помощью частных реакций.
Частные реакции
1. Обнаружение катиона NН4+
1.1 Реакция с реактивом Несслера {K2[HgI4]+ KОН}:
NН4Cl + 2K2[HgI4] +4 KОН = [ОHg2 NН2]I ↓+7KI + KCl + 3Н2О
В присутствии солей аммония образуется желто-коричневое окрашивание.
1.2 Реакция с едкими щелочами NaОн или kон:
NН4Cl + NaОН = NН3 ↑+ NaCl + Н2О
Аммиак обнаруживают по запаху или по появлению синей окраски на универсальной индикаторной бумаге, смоченной водой.
2. Обнаружение катиона К+
2.1 Реакция с гексанитрокобальтатом (III) натрия
Na3[Со(NО2)6]:
2КCl + Na3[Со(NО2)6] =К2Na[Со(NО2)6] ↓+2 NaCl
Образуется ярко-желтый осадок.
Гексанитрокобальтат натрия может быть реактивом на катионы К+ в отсутствии катионов NН4+.
2.2 Микрокристаллоскопическая реакция со смесью нитритов.
Реакция проводится на предметном стекле. В присутствии ионов калия под микроскопом видны характерные черные кубические кристаллы К2Pb[Сu(NО2)6]. Аналогичная реакция характерна для солей аммония, поэтому катионы К+ со смесью нитритов определяют в отсутствие катиона NН4+.

Рис 2.Кристаллы К2РЬ[Сu(NО2)6] и (NН4)2РЬ[Сu(NО2)6]
3. Обнаружение катиона Na+
3.1 Реакция с гексагидроксиантимонатом (V) калия К[Sb(ОН)6]:
NaCl + К[Sb(ОН)6] = Na[Sb(ОН)6]↓+ КCl
Образуется белый кристаллический осадок натриевой соли
Экспериментальная часть.
Опыт 1. Взаимодействие реактива Несслера с катионом NН4+
Реактив Несслера - это щелочной раствор тетраиодомеркурата калия K2[HgI4] . Прибавить к 1 - 2 каплям раствора NН4Cl 1-2 капли раствора реактива Несслера. Образуется красно-бурый осадок иодида оксодимеркураммония. Составить уравнение реакции.
Ионы калия и натрия не взаимодействуют с реактивом Несслера и обнаружению катиона аммония не мешают. Но присутствие в растворе катионов, которые со щелочами образуют окрашенные осадки гилроксидов, например, ионов Ni2+, Сu2+, Fe2+ и других, затрудняет обнаружение NН4+ . В этом случае реакцию необходимо выполнять в газовой камере.
- гигель;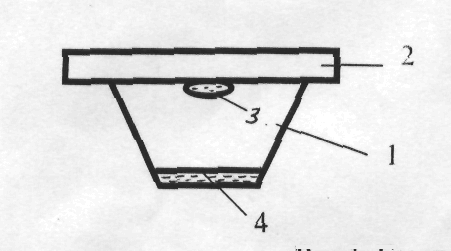
- покровное стекло;
- капля реактива Несслера;
- исследуемый раствор, NаОН.
Рис 3. Газовая камера
В фарфоровый тигель поместить 4-5 капель раствора NН4Сl и столько же раствора щелочи. Тигель накрыть стеклом, на внутренней поверхности которого находится капля реактива Несслера. Не более чем через одну минуту в этой капле появляется бурый осадок.
Опыт 2. Взаимодействие гидроксида натрия с катионом NН4+ . Поместить в пробирку 2 капли раствора NН4Сl и 5 капель раствора NаОН и подогреть содержимое пробирки. Выделяется аммиак Газообразный аммиак можно обнаружить:
по запаху;
по посинению смоченной водой красной лакмусовой бумажки, внесенной в пары исследуемого раствора.
Опыт 3. Взаимодействие гексанитрокобальтата натрия с катионами К+ и NН4+.
В одну пробирку поместить 2 капли раствора КСl, а в другую - 2 капли раствора NН4Сl, прибавив по 2 капли СН3СООН и СН3СООNa, 3-5 капель раствора Na3[Со(NО2)6] и перемешать. Наблюдается выпадение желтых осадков К2 Na [Со(NО2)6] и (NН4)2 Na[Со(NО2)6] . Составить уравнения реакций.
Гексанитрокобальтат натрия может быть реактивом на катионы К+, но в отсутствии катионов NН4+.
Опыт 4. Взаимодействие смеси нитритов натрия, меди, свинца
с катионами К+ (микрокристаллоскопическая реакция).
На предметное стекло поместить каплю раствора КС1, добавить каплю реактива смеси нитритов. Под микроскопом наблюдаются кристаллы черного цвета (см. рисунок 1).
Опыт 5. Взаимодействие с гексагидроксиантимонатом (V) калия
К[Sb(ОН)6](кислый пиросурьмянокислый калий) катиона Na+
Поместить в пробирку 2 капли раствора NaCl и 2 капли раствора К[Sb(ОН)6], потереть стеклянной палочкой о стенки' пробирки. Выпадает характерный белый осадок. Охлаждение раствора способствует выпадению осадка. Составить уравнение реакции.
Контрольные вопросы и задания
1. Каковы индивидуальные реактивы на катионы NН4+, К+, Na+. Приведите уравнения реакций.
2. Мешает ли катион NН4+ определению катионов К+ и Na+?
Лабораторная работа № 8
Анализ смеси катионов V и VI групп
Цель работы:
определить катионы V и VI групп в контрольном растворе.
Приборы и реактивы:
Микроскопы;
Набор реактивов в штативе;
Пробирки;
Стеклянные палочки;
Универсальная индикаторная бумага;
Предметные стекла;
Растворы солей:
сульфат меди;
хлорид кобальта;
хлорид никеля;
ацетат натрия - 0.5н;
тиосульфат натрия - кристаллический;
раствор гидроксида натрия;
раствор уксусной кислоты – 2н;
аммиак концентрированный и разбавленный;
раствор диметилглиоксима;
толуол;
гексацианоферрат (II) калия;
растворы смеси нитритов натрия, меди, свинца.
хлорид натрия;
ацетат натрия - 0.5н;
гексанитрокобальтиат натрия -- свежеприготовленный;
кислый пиросурьмянокислый калий – 1н (прозрачный);
раствор гидроксида натрия;
раствор уксусной кислоты – 2н;
аммиак разбавленный и концентрированны
реактив Несслера;
