
- •Билет №1
- •Вопрос 1: Показатель политропы в изотермическом, изобарном, изохорном, адиабатном и политропных процессах.
- •Показатель политропы:
- •Вопрос 2: Законы гидрогазодинамики. Физические свойства жидкостей (газов).
- •Билет №2
- •Вопрос 1: Дифференциальное уравнение равновесия Эйлера (вывод). Основное уравнение гидростатики. Дифференциальные уравнения равновесия Эйлера
- •После преобразования находим:
- •Таким образом, условия равновесия элементарного параллелепипеда выражаются системой уравнений:
- •Основное уравнение гидростатики
- •Вопрос 2: Уравнения теплоемкостей в изотермическом, изобарном, изохорном, адиабатном и политропных процессах.
- •43.Уравнения изменений энтальпии в изотермическом, изобарном, изохорном, адиабатном и политропных процессах.
- •3.Основные характеристики движения жидкости. Гидравлический радиус и эквивалентный диаметр.
- •4.Дифференциальное уравнение для установившегося и неустановившегося потока.
- •42.Уравнения изменений внутренней энергии в изотермическом, изобарном, изохорном, адиабатном и политропных процессах.
- •5.Режимы движения жидкостей и расход жидкости при ламинарном движении потока.
- •41.Уравнения количества теплоты, сообщаемое в адиабатном и политропном процессах.
- •6.Дифференциальное уравнение неразрывности потока. Практическое приложение.
- •Вопрос 2
- •Работа при адиабатическом процессе
- •Расчёт теплоты и работы политропных процессов сжатия газов
- •Вопрос 7
- •7. Дифференциальное уравнение движения идеальной жидкости (уравнение эйлера).
- •Вопрос 2
- •9.Вывод уравнения Бернулли. Практическое применение.
- •9.Вывод уравнения Бернулли. Практическое применение.
- •Вопрос 2
- •10.Теория подобия – метод научного обобщения экспериментов.
- •Вопрос 2
- •11. Условия и теория подобия.
- •Вопрос 2
- •36.Простейшие термодинамические процессы идеальных газов.
- •4Адиабатный процесс
- •5. Политропный процесс
- •Вопрос 13
- •12. Первая теорема подобия. Преобразование дифференциального уравнения в критериальное. Подобие начальных и граничных условий
- •Вопрос 2
- •35.Параметр состояния термодинамической системы – энтропия. Вывод.
- •13. Вторая теорема подобия. Пример использования.
- •Вопрос 2
- •34. Второй закон термодинамики. Основные постулаты, вытекающие изз второго закона термодинамики.
- •14. Третья теорема подобия. Раскрыть ее сущность.
- •Вопрос 2
- •33.Уравнение Майера.
- •Вопрос 16
- •15. Преобразование дифференциального уравнения Навье-Стокса в критериальное. Гидравлическое подобие
- •Для установившегося потока
- •Вопрос 2
- •32.Первый закон термодинамики. Раскрыть сущность.
- •16. Модифицированные и производные критерии подобия
- •Вопрос 2
- •30.Работа и теплота
- •28. Внутренняя энергия системы. Внутренняя энергия идеального газа.
- •29. Энтальпия идеального газа.
- •19. Гидравлическое сопротивление при движении жидкостей (газов) в трубах и каналах.
- •26. Смеси идеальных газов. Массовая и молярная концентрация. Парциальное давление. Закон Дальтона.
- •21. Сопротивление при свободном движении тел в газах и жидкостях
- •22. Осаждение частиц под действием сил тяжести и инерции. Примеры применения.
- •Основные понятия о науке газодинамике
11. Условия и теория подобия.
Один из основных принципов теории подобия заключается в выделении из класса явлений группы подобных явлений.
Подобными называют явления, для которых постоянны отношения характеризующих их сходственных величин.
Геометрическое
подобие: 
где a/, b/, c/ - размеры сторон одного треугольника, а размеры сходственных подобно ему треугольников составляют a/, b / и c/.
Коэффициент Кl является константой геометрического подобия.
Подобные фигуры отличаются друг от друга только масштабом и могут быть получены одна из другой умножением сходственных размеров одной из них на некоторый масштабный множитель, называемый константой подобия.
Подобие может быть охарактеризовано также величиной инвариантов подобия
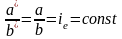 ,
,
где ie - инвариант геометрического подобия.
Геометрическое подобие - необходимое условие, но не достаточное. При подобии физических процессов должны быть подобны все основные физические величины, влияющие на процесс.
Поэтому процессы подобны только при условии совместного соблюдения геометрического и временного подобия, подобия полей физических величин, а также подобия начальных и граничных условий. Сформулируем эти условия на примере подобного движения вязкой жидкости в натуре и на модели (рисунок 2.18).

Рисунок 2.18 - К формулировке условий подобия потоков в натуре и в модели
Геометрическое подобие записывается как
 ,
(2.64)
,
(2.64)
где Кl - константа геометрического подобия.
При подобном движении сходственных точек их траектории в натуре и в модели также должны быть подобны. Это условие называют кинематическим подобием.
Временное подобие характеризуется тем, что сходственные частицы в геометрически подобных системах, двигаясь по геометрическим подобным траекториям, проходят геометрически подобные пути за промежутки времени, отношение которых является величиной постоянной, т.е.
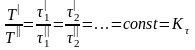 ,
(2.65)
,
(2.65)
где K - коэффициент временного подобия.
При соблюдении геометрического и временного подобия будет соблюдаться и подобие скоростей
 ,
(2.66)
,
(2.66)
где KW – константа скоростного подобия.
Подобие физических величин предполагает, что для сходственных точек натуры и модели при её замещении подобно в пространстве и времени (т.е. при соблюдении геометрического и временного подобия), отношения физических свойств являются величинами постоянными, т.е.
 ,
(2.67)
,
(2.67)
 и
т.д. (2.68)
и
т.д. (2.68)
Вопрос 2
36.Простейшие термодинамические процессы идеальных газов.
Термодинамические процессы: изохорный, изобарный, изотермический, адиабатный, политропный.
1.Изохорный процесс (v=const)
Такой процесс может совершаться рабочим телом, находящимся в цилиндре при неподвижном поршне, если к рабочему телу подводится теплота от источника теплоты (см. рис. 4.1) или отводится теплота от рабочего тела к холодильнику. При изохорном процессе выполняется условие dv=0 или v=const. Уравнение изохорного процесса получим из уравнения состояния идеального газа (см. &1.6) при v=const. В pv-координатах график процесса представляет собой прямую линию, параллельную оси p. Изохорный процесс может протекать с повышением давления (процесс 1-2) и с понижением (процесс 1-2’)
 Запишем
для точек 1 и 2 уравнения состояния:
p1·v=R·T1; p2·v=R·T2. Следовательно, для
изохорного процесса
Запишем
для точек 1 и 2 уравнения состояния:
p1·v=R·T1; p2·v=R·T2. Следовательно, для
изохорного процесса
![]() .
.
Приращение внутренней энергии газа
![]()
Работа газа :

То
есть:
![]()
2.Изобарный процесс (p=const)
В p-v координатах график процесса представляет собой прямую линию параллельную оси v (рис. 4.2). Изобарный процесс может протекать с увеличением объёма (процесс 1-2) и с уменьшением (процесс 1-2’). Запишем для точек 1 и 2 уравнения состояния: p·v1=R·T1; p·v2=R·T2.
 Следовательно,
для изобарного процесса:
Следовательно,
для изобарного процесса:
![]()
Приращение внутренней энергии газа:

Работа газа:

Энтропия газа:
![]()
3.Изотермический процесс (T=const)
В p-v координатах график процесса изображается равнобокой гиперболой (рис. 4.3). Изотермический процесс может протекать как с увеличением объёма (процесс 1-2), так и с уменьшением объёма (процесс 1-2’).
Рис. 4.3. График изотермического процесса в p-v координатах
Запишем для точек 1 и 2 уравнения состояния p1·v1=R·T; p2·v2=R·T. Следовательно, для изотермического процесса p1·v1=p2·v2=const.
Работа газа

Теплота, подводимая в процессе:
![]()
Изменение энтальпии газа Δi=Δu+Δ(p·v)=0.
Изменение энтропии газа:

