
Электрический ток в жидкостях. Законы электролиза.
1) Из жидкостей электрический ток проводят только электролиты-растворы солей, кислот и щелочей.
2) Распад молекул электролитов на ионы называется электролитической диссоциацией.
3) Электрическим током в жидкости называется направленное движение положительных ионов к катоду, а отрицательных ионов - к аноду.
4) Электропроводность электролитов обусловлена наличием в них положительных и отрицательных ионов (катионов и анионов).
5) В металлах атомы самого металла находятся в узлах кристаллической решётки и могут оттуда сдвинуться только тогда, когда решётка разрушится. А носителями электрического тока являются только электроны. В электролитах нет кристаллической решётки. Электролит представляет собой смесь нейтральных атомов и заряженных ионов вещества, образующего электролит. При приложении к электролиту электрического поля начинаю двигаться как электроны, так и заряженные ионы. Ионы обычно не вечные. Рано или поздно они нейтрализуются и превращаются в полноценные атомы или молекулы вещества. А поле-то их уже перенесло на новое место!!! Вот и происходит перенос вещества в электролитах под действием электрического поля.
6) Выделение на катоде вещества, входящего в состав электролита ,называется электролизом.
7) Первый закон Фарадея: масса вещества (m), выделившегося на катоде, прямо пропорциональна заряду(q), прошедшему через электролит.
m= k*I*∆t=k*q ,
8) [k]=кг/Кл– электрохимический эквивалент вещества численно равен массе выделившегося вещества, при переносе заряда в 1 Кл. k=moi/qoi
9) Объединённый закон Фарадея:
m= (1/F)*(M/n)*I*∆t=(1/F)*(M/n)*q
10) F=eNA=9,648*104Кл/моль – постоянная Фарадея численно равная заряду, который должен пойти через электролит, чтобы на электроде выделился 1 моль одновалентного вещества.
11).Применение электролиза: получение алюминия и бокситов; очистка металлов от примесей; получение водорода. Электрометаллургия. Гальванопластика. Гальваностегия- покрытие металлических изделий неокисляющимися металлами ( никелирование, хромирование ); гальванопластика- воспроизведение форм предметов в матрицах.
Электрический ток в газах.
1)Газ становится электропроводным в результате ионизации газов.
2) Распад атомов на положительные ионы и электроны называется ионизацией, обратный процесс- 3)рекомбинацией.
4)Носители тока в газах- отрицательные заряды
5) Электрическим током в газах называется направленное движение положительных ионов к катоду, отрицательных ионов и электронов к аноду.
6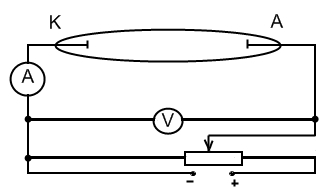 )
Газовый заряд-процесс протекания электр
тока через газ, протекающий под действием
ионизатора, называется несамостоятельным,
а без ионизатора - самостоятельным.
)
Газовый заряд-процесс протекания электр
тока через газ, протекающий под действием
ионизатора, называется несамостоятельным,
а без ионизатора - самостоятельным.
Особенности несамостоятельного разряда в газах:
А)в трубке возникает электр ток, т е происходит газовый разряд;
Б) ток достигает насыщении, если действие ионизатора прекратить, то прекратится и разряд, по этой причине разряд называют несамостоятельным.
