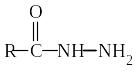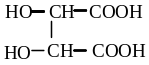лекция 6-7 - карбоновые кислоты, гидрокси и окс
...docЛекция № 6-7
КАРБОНОВЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
СПОСОБЫ ПОЛУЧЕНИЯ КАРБОНОВЫХ КИСЛОТ
.
Лекция № 6-7
ОСНОВНЫЕ ФУНКЦИОНАЛЬНЫЕ
ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ
Название производных |
Структурная формула |
Галогенангидриды (фторангидриды, хлорангидриды, бромангидриды, йодангидриды) |
|
Простые ангидриды |
|
Смешанные ангидриды |
|
Сложные эфиры |
|
Амиды (первичные, вторичные, третичные) |
|
Нитрилы |
|
Соли |
|
Азиды |
|
Гидразиды |
|
Гидроксамовые кислоты |
|
Ортоэфиры |
|
Надкислоты |
|
Перекиси кислот |
|
Амидины |
|
Лекция № 6-7
ВЗАИМНЫЕ ПРЕВРАЩЕНИЯ ФУНКЦИОНАЛЬНЫХ ПРОИЗВОДНЫХ КАРБОНОВЫХ КИСЛОТ

Лекция № 6-7
МЕХАНИЗМ РЕАКЦИИ ЭТЕРИФИКАЦИИ (AdN)
ПРОПИОНОВОЙ КИСЛОТЫ МЕТИЛОВЫМ СПИРТОМ
В ПРИСУТСТВИИ СЕРНОЙ КИСЛОТЫ
Реакция карбоновой кислоты со спиртом, катализируемая сильными кислотами, известна как реакция этерификации (реакция Фишера-Шпайера, 1895г.)
![]()
Стадия 1 - образование гидроксониевого иона:

Стадия 2 – нуклеофильное присоединение молекулы спирта к карбонильному атому углерода и изомеризация образовавшегося аддукта:

Стадия 3 – элиминирование молекулы воды и депротонирование продукта реакции:

Для повышения выхода сложного эфира необходим сдвиг равновесия вправо, что достигается удалением образующейся воды, добавлением веществ, ее связывающих, либо путем азеотропной отгонки с бензолом или толуолом. Скорость реакции этерификации зависит от природы кислоты, спирта и пространственных факторов. Более высокий выход достигается при участии первичных спиртов, труднее всего в реакцию вступают третичные спирты, алифатические карбоновые кислоты, замещенные в α-положении и орто-замещенные ароматические кислоты.
Лекция № 6-7
ПРЕВРАЩЕНИЯ ДИКАРБОНОВЫХ КИСЛОТ ПРИ НАГРЕВАНИИ
Кислота |
Формула |
Температура 0С |
Продукты реакции |
щавелевая |
|
а) 160-180
б) в прис. Н2SO4
|
НСООН + СО2
H2O + CO2 + CO |
малоновая |
|
140-160
160-180
180-200 |
CН3СООН + СО2
|
янтарная |
|
300 |
|
глутаровая |
|
300 |
|
адипиновая |
|
300 |
|
пимелиновая |
|
300 |
|
фталевая |
|
230 |
|
Лекция № 6-7
СИНТЕЗЫ НА ОСНОВЕ МАЛОНОВОГО ЭФИРА
а) монозамещенных уксусных кислот:


б) дизамещенных уксусных кислот:


в) янтарной кислоты — обработкой натриймалонового эфира йодом:

г) двухосновных кислот, используя алкилирование эфирами галогензамещенных кислот:


Лекция № 6-7
ГИДРОКСИ- И ОКСОКИСЛОТЫ
ВАЖНЕЙШИЕ ГИДРОКСИКИСЛОТЫ
Формула |
Название |
НО–СH2–COOH |
Гликолевая кислота, 2-гидроксиэтановая кислота |
|
Молочная кислота, 2-гидроксипропановая кислота |
|
Глицериновая кислота, 2,3-дигидроксипропановая кислота |
|
Тартроновая кислота, 2-гидроксипропандиовая кислота |
|
Яблочная кислота, 2-гидроксибутандиовая кислота |
|
Винная кислота, 2,3-дигидроксибутандиовая кислота |
|
Лимонная кислота, 3-гидрокси-3-карбоксипентандиовая кислота |
|
Салициловая кислота, 2-гидроксибензойная кислота (о-гидроксибензойная кислота) |
|
Анисовая кислота, 4-метоксибензойная кислота, (п-метоксибензойная кислота) |
|
Ванилиновая кислота, 3-метокси-4-гидроксибензойная кислота |
|
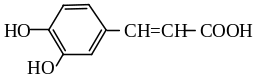
Кофейная кислота. 3-(3',4'-дигидрокси)фенил-2-пропеновая кислота. |
Лекция № 6-7
ХИМИЧЕСКИЕ РЕАКЦИИ ГИДРОКСИКИСЛОТ
В реакциях, характерных для карбоксильной и гидроксильной групп, могут затрагиваться как та, так и другая или обе группы одновременно. В последнем случае для проведения реакции по одной из групп используют методы защиты другой.
Реагент Функц. группа |
Na |
NaOH или Na2CO3 |
NH3 |
HBr |
CH3OH (HCl) |
PCl5 |
(CH3CO)2O |
COOH |
+ |
+ |
+ |
|
+ |
+ |
|
OH |
+ |
|
|
+ |
|
+ |
+ |
Фенолокислоты в отличие от спиртокислот при взаимодействии с гидроксидом натрия реагируют обеими функциональными группами. В качестве примера рассмотрим взаимодействие молочной кислоты с перечисленными выше реагентами:

Лекция № 6-7
ПРЕВРАЩЕНИЯ ГИДРОКСИКИСЛОТ ПРИ НАГРЕВАНИИ
Дегидратация при нагревании:
а) -гидроксикислоты образуют продукты межмолеку-лярной реакции лактиды,

α-гидроксипропионовая кислота лактид молочной кислоты
б) -гидроксикислоты превращаются в ,-непредельные кислоты,
t
CН3–СН2–СН(ОН)–СН2–СООН CН3–СН2–СН=СН–СООН
- Н2О
β-гидроксипентановая кислота α,β-непредельная кислота
в) - и -гидроксикислоты дают внутренние эфиры, называемые лактонами.

γ-гидроксимасляная кислота γ-бутиролактон

δ-гидроксикапроновая кислота δ-капролактон
Яблочная кислота при нагревании подвергается дегидратации и образует, как это характерно для β-гидроксикислот, непредельную кислоту:
CН (ОН)–СООН t СН–СООН
│ ║ + H2O
СН2–СООН СН–СООН
Винная кислота при нагревании теряет воду и декарбоксилируется, превращаясь в пировиноградную кислоту:

Лекция № 6-7
При нагревании лимонная кислота (как -гидроксикислоты) превращается в аконитовую кислоту, которая распадается далее на смесь итаконового и цитраконового ангидридов. В присутствии H2SO4 лимонная кислота, как -гидроксикислота, отщепляет муравьиную кислоту и образует ацетондикарбоновую кислоту.


лимонная кислота
Лекция № 6-7
СЛОЖНОЭФИРНАЯ КОНДЕНСАЦИЯ ПО КЛЯЙЗЕНУ
Конденсация сложных эфиров с соединениями, содержащими активную метиленовую группу (сложными эфирами, альдегидами, кетонами и др.), протекающая в присутствии оснований с образованием -дикарбонильных соединений.
Например, при самоконденсации сложных эфиров образуются -кетоэфиры:

Механизм реакции:
1 стадия:

2 стадия:


Лекция № 6-7
ХИМИЧЕСКИЕ РЕАКЦИИ АЦЕТОУКСУСНОГО ЭФИРА
Ацетоуксусный эфир в одних реакциях реагирует в виде кетонной формы, а в других – проявляет свойства енола, вследствие проявления веществом кето-енольной таутомерии:

Свойство некоторых веществ образовывать продукты реакций, соответствующие их различным таутомерным формам называется двойственной реакционной способностью.
СИНТЕЗЫ НА ОСНОВЕ АЦЕТОУКСУСНОГО ЭФИРА
Ацетоуксусный эфир содержит СН2-группу в -положении по отношению к двум электроноакцепторным группам, поэтому ее атомы водорода отщепляются в виде протона под действием оснований. Полученный натрийацетоуксусный эфир с галогеналканами вступает в реакцию С-алкилирования, причем алкилирование может быть проведено дважды:
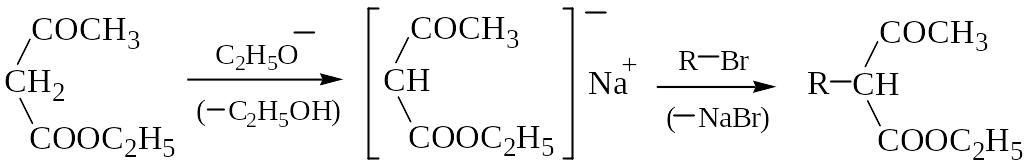
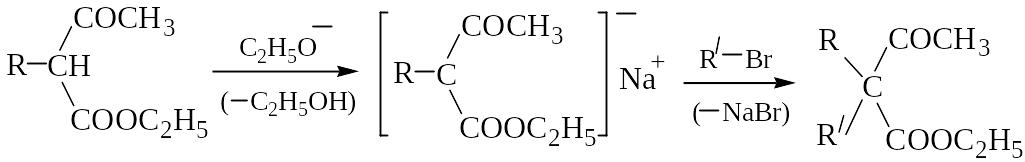
В ацетоуксусном эфире и его алкилпроизводных в зависимости от условий реакции осуществляется два типа разрывов СС-связи, называемых по классу получаемых продуктов кетонным (а) или кислотным (б) распадом:

Таким образом, на основе ацетоуксусного эфира могут быть синте- зированы:
а) кетоны общей формулы (кетонный распад);
![]()
б)
моно- и диалкилуксусные кислоты

(кислотный распад)