- •Лабораторная работа № 1. Изучение явления интерференции света
- •Краткие теоретические сведения.
- •Экспериментальная часть.
- •Ход работы.
- •Измерения.
- •Лабораторная работа №2.
- •Краткая теория
- •Экспериментальная часть Задание 1
- •Определение длин волн испускания
- •Краткие теоретические сведения.
- •Экспериментальная часть.
- •Задание 1. Градуировка монохроматора.
- •Задание 2. Определение длин волн испускания.
- •Задание 1
- •Задание 2
- •Задание 3
- •Задание 5
- •Задание 6
Экспериментальная часть Задание 1
№ п/п |
U, В |
I, А |
Температура, t0C |
Тср 0C |
Тист 0C |
Т, К |
|
|
||||||||
t1 |
t2 |
t3 |
t4 |
|||||||||||||
1 |
80 |
32 |
1570 |
1590 |
1550 |
1570 |
1570 |
1656 |
1929 |
4,63*10-8 |
0,81 |
|||||
2 |
100 |
36 |
1830 |
1850 |
1810 |
1830 |
1830 |
1942 |
2215 |
5,02*10-8 |
0,88 |
|||||
3 |
120 |
40 |
1900 |
1920 |
1890 |
1920 |
1920 |
2048 |
2351 |
5,23*10-8 |
0,92 |
|||||
4 |
140 |
43 |
2080 |
2100 |
2100 |
2110 |
2100 |
2254 |
2527 |
5,33*10-8 |
0,94 |
|||||
s=1,04∙10-4м2
Формула
для расчета
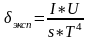
Р1=2,56 Вт; р2=3,6 Вт; р3=4,8 Вт; р4=6,02 Вт;
График зависимости P=f(T)
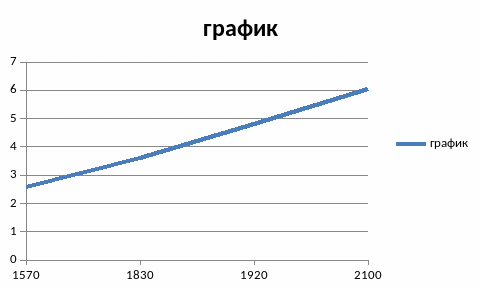
Вывод: Температура нити лампы накаливания зависит от потребляемой мощности. Чем больше мощность, тем больше температура и следовательно лампа светит ярче. Значение постоянной Стефана-Больцмана отличается от табличного значения. Коэффициенты незначительно отличаются друг от друга.
Лабораторная работа №3
Определение длин волн испускания
ЦЕЛЬ РАБОТЫ: изучить виды спектров, изучить спектры ртутной лампы и лампы накаливания, измерить длины волн испускания неоновой лампы.
Краткие теоретические сведения.
Уравне́ние Шрёдингера — уравнение, описывающее изменение в пространстве и во времени чистого состояния, задаваемого волновой функцией, в гамильтоновых квантовых системах.
Полосатый спектр - спектр, монохроматические составляющие которого образуют дискретные группы (полосы), состоящие из множества тесно расположенных линий.
Сплошной спектр, непрерывный спектр, спектр электромагнитного излучения, распределение энергии в котором характеризуется непрерывной функцией частоты излучения [j(n)] или длины его волны [f(l), см
Модель атома Бора где отрицательно заряженный электрон заключен в атомной оболочке, окружающей малое, положительно заряженное атомное ядро. Переход электрона с орбиты на орбиту сопровождается излучением или поглощением кванта электромагнитной энергии (hν)
Постулаты Бора — основные допущения, сформулированные Нильсом Бором в 1913 году для объяснения закономерности линейчатого спектра атома водорода и водородоподобных ионов (формула Бальмера-Ридберга) и квантового характера испускания и поглощения света.
Момент импульса электрона в водородоподобном атоме, находящемся в стационарном состоянии:
Ln = mr = nħ (n = 1, 2, 3,…),
Энергия электрона в водородоподобном атоме
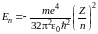 ,
,
Квантовые числа — энергетические параметры, определяющие состояние электрона и тип атомной орбитали, на которой он находится.
При́нцип Па́ули (принцип запрета) — один из фундаментальных принципов квантовой механики, согласно которому два и более тождественныхфермиона (частиц с полуцелым спином) не могут одновременно находиться в одном квантовом состоянии.

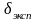 ,
Вт/м2×К4.
,
Вт/м2×К4.