
Ответы на вопросы части Иванисика
Оглавление
I-1. Термодинамічні системи. Оборотні та необоротні процеси. Особливості живих систем. 2
I-2. Використання калориметрів для вивчення теплопродукції живих організмів. Диференціальна скануючи мікрокалориметрія. 4
I-4. Стаціонарні стани. Теорема Пригожина 6
I-5. Використання оптичної мікроскопії для вивчення живих мікросистем: 8
I-6. Електронна мікроскопія. 9
I-8. Визначення маси макромолекул 12
I-9. Хімічні компоненти клітинних мембран. 15
I-10. Типи мембранного транспорту. 17
I-11. Рівняння Томаса. 19
I-12. Рівняння Нернста 21
I-13. Рівняння Гольдмана-Ходшкін-Котца 22
I-14. Будова нейронів та їх оболонок 23
I-15. Кабельна теорія поширення нервового імпульсу вздовж неміелізованого аксона нейронів 26
I-16. Математична модель Ходжкіна-Хакслі 28
I-17. Миелизированные волокна. Сальтаторный режим 31
I-18. Синоптична передача збуджень. Типи синапсів. Нейромедіатори 33
I-19. Поперечносмугасті скелетні м’язи: будова, молекулярний механізм скорочення 36
I-20.Нем’язові форми руху: бактеріальний «мотор», війки, джгутики, амебоїдний рух. 37
I-21.Сенсорні системи організму 40
I-22. Принципи кодування інформації у сенсорних системах 43
I-23.Око, сітківка, молекулярний механізм фото рецепції 45
Вопросы 3 и 7 — отсканированные!!!
I-1. Термодинамічні системи. Оборотні та необоротні процеси. Особливості живих систем.
Термодинамічна система (ТС) – частина простору з матеріальним вмістом, обмежена оболонкою. Область за межами оболонки – навколишнє середовище.
В залежності від зв’язку між термодинамічною системою і навколишнім середовищем виділяють три види систем:
Ізольовані – відсутній будь-який обмін з простором.
Замкнені – між термодинамічною системою і зовнішнім простором існує обмін енергією
Відкриті – між термодинамічною системою і зовнішнім простором існує як обмін енергією так і обмін речовиною.
Стан ТС характеризується набором параметрів
Екстенсивні (наприклад маса m, об’єм V)
Інтенсивні – не залежать від маси системи (тиск p, температура T, молярна концентрація n).
Зміна стану системи – зміна будь-якого з параметрів.
Процеси у термодинамічних системах:

Оборотні процеси проходять у стані термодинамічної рівноваги.
Реальні процеси в природі завжди необоротні.
Внутрішня
енергія однозначно
описує стан системи, являється функціє
стану системи і залежить від термодинамічних
параметрів
 .
.
Внутрішня енергія – сума потенціальної і кінетичної енергії всіх атомів і молекул системи. Її зміна не залежить від шляху переходу із одного стану ТС до іншого.
Внутрішню енергію в замкнутій ТС можна визначити, вимірюючи поглинуту теплоту та виконану роботу.

де: Q – теплота, отримана системою, W – виконана системою робота.
Зміна
внутрішньої енергії не залежить від
шляху переходу із одного стану ТС до
іншого.
 .
.
Тобто в замкненій системі ΔU = const, у ізольованій – ΔU = 0
При
сталому тискові (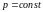 )
можна ввести нову функцію стану системи,
що буде її описувати однозначно.
)
можна ввести нову функцію стану системи,
що буде її описувати однозначно.
Ентальпія системи: H = U + pV
Загалом всі живі системи розглядаються при р = const
ΔH = ΔU + pΔV = Q – W + pΔV = |W = pΔV + Wk| = Q – Wk
Робота, виконана системою по зміні об'єму: WPV = pΔV. Всю іншу роботу прийнято називати корисною Wk:
W = pΔV + Wk
Отже ΔH = Q – Wk, якщо Wk = 0, то ΔH = Q – можна виміряти за допомогою калориметра. Тобто можна виміряти зміну ентальпії:
ΔQ = ΔH = -ΣпочHi + ΣкінцHi
Закон Гесса: Тепловиділення залежить не від послідовності хімічних реакцій, а від початкових і кінцевих продуктів реакції.
I-2. Використання калориметрів для вивчення теплопродукції живих організмів. Диференціальна скануючи мікрокалориметрія.
Закон Гесса:
тепловий
ефект Q
хімічної
реакції
не залежить від шляху реакції, а
визначається тільки різницею ентальпій
вихідних речовин і продуктів реакцій.

 -
сума
ентальпій всих продуктів реакції ;
-
сума
ентальпій всих продуктів реакції ;
 - сума ентальпій вихідних речовин.
- сума ентальпій вихідних речовин.
О скільки
зміна ентальпії (тепловмісту) системи
відповідає поглинутій або виділеній
теплоті, то її можна виміряти
за допомогою калориметра.
скільки
зміна ентальпії (тепловмісту) системи
відповідає поглинутій або виділеній
теплоті, то її можна виміряти
за допомогою калориметра.
Конструкція калориметра дає можливість повністю ліквідувати потік теплоти через стінки циліндрів, що накопичується всередині калориметра при перебуванні там людини чи тварини.
Потік теплоти :
 ,
,
оскільки

k-коефіцієнт теплопровідності
d-відстань між циліндрами
S-площа циліндрів
 -
температура на стінках
-
температура на стінках
При діяльності організму людини :

Калориметр дає можливість оцінювати дихальний коефіцієнт:
 ,
,
 – кількість
виділеного
– кількість
виділеного
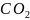
 -
кількість поглинутого
-
кількість поглинутого

Кожному δ відповідає свій енергетичний еквівалент q – кількість енергії, яка виділяється при поглинанні 1л
Вуглеводи
δ
= 1,00 q
= 21,0 кДж/л якщо
 >0 (теплота поглинається), то реакція
ендотермічна
>0 (теплота поглинається), то реакція
ендотермічна
білки δ = 0,80 q = 18,8 кДж/л якщо <0 (теплота поглинається), то реакція екзотермічна
жири δ = 0,71 q = 19,6 кДж/л
Д иференціальна
сканувальна мікрокалориметрія
дає важливу інформацію про структурну
організацію білків.
иференціальна
сканувальна мікрокалориметрія
дає важливу інформацію про структурну
організацію білків.
1 – буфер – контрольний зразок
2-зразок – зразок білкового препарату
Досліджуємо
зміну ентальпії
.
Вимірюємо
 -що
необхідна для того, щоб
-що
необхідна для того, щоб

Криві
плавлення білків зображуються як
температурні залежності теплоємності

Теплоємність буфера:

Теплоємність зразка:



Гіпотеза:
перехід
білкової молекули з нативного стану у
денатурований визначається на кривій
плавлення піком
 .
Якщо на кривій плавлення декілька піків
то в білку є структурні домени з різною
термостійкістю.
.
Якщо на кривій плавлення декілька піків
то в білку є структурні домени з різною
термостійкістю.
I-4. Стаціонарні стани. Теорема Пригожина
Основним критерієм рівноважної термодинаміки є прямування ентропії до максимального значення Smах, коли замкнута система набуває рівноважного стану. Найважливішим результатом лінійної нерівноважної термодинаміки стало визначення критерію переходу до стаціонарного стану у відкритій термодинамічній системі.
Розглянемо відкриту систему, в якій відбуваються два необоротних спряжених потоки — теплоти J1, і речовини J2. Дисипативну функцію запишемо так:
Ф = T dS/dt = J1 X1 + J2X2 >0,
а спряжені потоки
J1=L11X1+L12X2
J2= L2lX1+ L22X2
Тоді
T dS/dt = (L11X1+L12X2)X1 + (L2lX1+ L22X2)X2 =L11X12+L12X1X2+L21X1X2+L22X22
Враховуючи співвідношення взаємності Онзагера L12=L21, отримуємо
TdiS/dt = L11X12+2L12X1X2+L22X22>0
де L11>0, L22>0, Ll2>0. Нехай у відкритій системі встановиться стаціонарний стан у результаті того, що кількість речовини, яка надходить до системи, дорівнює кількості речовини, яка виходить з неї, тобто потік речовини J2=0. Оскільки T=const, дослідимо на екстремум diS/dt за Х2 при X1 = const:

Це відповідає експериментальній точці. Друга похідна від diS/dt:

Отже, екстремальна точка відповідає мінімуму функції diS/dt
Теорема Пригожина: у стаціонарному стані при фіксованих зовнішніх параметрах швидкість продукції ентропії у відкритій системі набуває мінімального значення

або локальна продукція ентропії у відкритій системі набуває мінімального значення
![]()
Теорема Пригожина про мінімум швидкості продукції ентропії в стаціонарному стані є кількісним критерієм еволюції відкритої системи: відкрита система прямує до стаціонарного стану, в якому розсіювання енергії здійснюється на мінімальному рівні.
I-5. Використання оптичної мікроскопії для вивчення живих мікросистем:
К літина
ссавців має розмір 10 – 20 мкм, і тому може
бути досліджена за допомогою оптичного
мікроскопа. Його роздільна здатність
визначається так:
δ = 0,61*(λ/А) → →0,25 мкм, де А – числова
апертура, що дорівнює А = n
sin(α/2),
де n
– показник заломлення, а α
– кутова апертура.
літина
ссавців має розмір 10 – 20 мкм, і тому може
бути досліджена за допомогою оптичного
мікроскопа. Його роздільна здатність
визначається так:
δ = 0,61*(λ/А) → →0,25 мкм, де А – числова
апертура, що дорівнює А = n
sin(α/2),
де n
– показник заломлення, а α
– кутова апертура.
К літини
є рефракційними об’єктами,
а тому показник заломлення у них є
змінним в межах одного об’єкта.
Розглянемо процес дослідження зразка:
Е’- хвиля, що пройшла (нульовий порядок
дифракції); Ер – хвиля, що розсіялася.
літини
є рефракційними об’єктами,
а тому показник заломлення у них є
змінним в межах одного об’єкта.
Розглянемо процес дослідження зразка:
Е’- хвиля, що пройшла (нульовий порядок
дифракції); Ер – хвиля, що розсіялася.
Ер = Е – Е’ = E0*sinφ - E0*sin(φ - δφ)=/враховуємо, що δφ ˂˂π/ = =2*( δφ/2)*cosφ

(1): Е’- хвиля, затримана відносно Е, (2): Ер – зсунута на π/2,
← График Иванисика
Дослідження проводяться за наступною схемою:
О тже,
(1)-нульовий порядок проходить і збирається
у фокусі, в результаті чого ми його
реєструємо і отримуємо інформацію про
об’єкт.
тже,
(1)-нульовий порядок проходить і збирається
у фокусі, в результаті чого ми його
реєструємо і отримуємо інформацію про
об’єкт.
В загалі,
оптичні методи дослідження дозволяють
аналізувати частинки розмірами долі
нм. Наприклад, молекулу фулерену С60 було
досліджено за допомогою He-Ne
лазера
(0,4 нм).
загалі,
оптичні методи дослідження дозволяють
аналізувати частинки розмірами долі
нм. Наприклад, молекулу фулерену С60 було
досліджено за допомогою He-Ne
лазера
(0,4 нм).
Також, використовують методику оптичного дослідження на основі ефекту Доплера: після опромінення досліджуваних частинок когерентним пучком на виході маємо некогерентне випромінювання, аналізуючи його будується картинка. Проте такими дослідженнями можна дослідити розміри молекули, але не її вид.
Для поращення роздільної здатності переходять до рентгенівського діапазону( λ = 0,00001 – 1нм). Зараз роздільна здатність цього методу складає приблизно δ ≈10 нм. В цьому випадку використовують дзеркальну оптику, є можливість працювати у режимі темного поля (реєструємо лише те світло, що дифрагувало). Але і в цьому випадку роздільна здатність обмежена наявністю аберацій, недосконалою оптикою, малим поглинанням тілом енергії квантів hν (погіршення фазового контрасту).
I-6. Електронна мікроскопія.
Електронна мікроскопія – метод морфологічного дослідження об'єктів за допомогою потоку електронів, що дозволяють вивчити структуру цих об'єктів на макромолекулярному і субклітинному рівнях.
На відміну від оптичного мікроскопа, в електронному використовують потоки електронів і магнітні чи електростатичні лінзи для формування зображення шляхом керування пучком електронів і концентрації його на окремих ділянках зображення подібно тому, як оптичний мікроскоп використовує скляні лінзи для фокусування світла на (чи повз) зображенні.
Види електронних мікроскопів
Просвічуючий (пучок просвічує предмет наскрізь);.
Растровий (скануючий);
Відбивальний (використовує пружно-розсіяні електрони);
Растровий просвічуючий
Фотоемісійний
(Перші три види взаємно доповнюють одне одного)
Електронный мікроскоп – прилад для спостереження і фотографування многократно (до 106 раз) збільшенного зображения об’єктів, в якому замість светлових променів використовуюються пучки електронів, прискоренних до великих енергій (30—100 кЕв и більше) в умовах глибокого вакууму. Електронні мікроскопи можуть збільшувати зображення до 1,5 млн. разів. Висока роздільна здатність електронних мікроскопів досягається за рахунок малої довжини хвилі електрона. В той час, як довжина хвилі видимого світла лежить в діапазоні від 400 до 800 нм, довжина хвилі електрона, прискореного у потенціалі 150 В, складає 0,1 нм.
Просвічуююча електронна мікроскопія
Б удову
електронного мікроскопа можна розглянути
на прикладі приладу, який працює на
пропускання.
удову
електронного мікроскопа можна розглянути
на прикладі приладу, який працює на
пропускання.
1 - електронна пушка; 2 - конденсор; 3 -зразок; 4, 5- об’єктив та його діафрагма; 6, 7- проміжна та проекційна лінзи; 8 -смотрове вікно; 9 - люмінесцентний екран; 10 - фотокамера з затвором; 11 - вакуумна система.
Пучок електронів, що емітуються розжареним катодом, формується в електронній гарматі і далі поширюється в вакуумі 10-6 мм рт. ст. Далі він фокусується першою та другою конденсорними лінзами, які створюють на об’єкті електронну «пляму» малих розмірів.
Після проходження крізь обєкт частина електронів розсіюється та затримується апертурною діафрагмою. Нерассеянные электроны проходят через отверстие диафрагмы и фокусируются объективом в предметной плоскости промежуточной линзы. Здесь формируется первое увеличенное изображение. Последующие линзы создают второе, третье и т. д. изображения. Последняя проекционная линза формирует изображение на флуоресцирующем экране, который светится под воздействием электронов. Увеличение Э. м. равно произведению увеличений всех линз.
В залежності від типу лінз, магнітних чи електростатичних, розрізнять магнітні й електростатичні мікроскопи.
Апертурна діафрагма об'єктива електронного мікроскопа дуже мала, складає соті долі міліметра.
Якщо пучок електронів від об'єкту потрапляє безпосередньо на екран, то об'єкт виглядатиме на ньому темним, а навколо утворюватиметься світлий фон. Таке зображення називається світлопольним. Якщо ж в апертуру об'єктивної лінзи потрапляє не основий пучок, а розсіяний, то утворюється темнопольне зображення (основний пучок електронів при цьому отклоняют або екранують). Темнопольне зображення контрастніше, ніж світлопольне, але роздільна здатність у нього менша.
Сканирующий электронный микроскоп (СЭМ)- микроскоп, который сканирует исследуемый образец электронным лучом. Измеряет интенсивность квантов, испускаемых образцом. Это могут быть вторичные электроны, отраженные электроны и т.д. Преобразует измеренную интенсивность в электрический сигнал. По сравнению с оптическими микроскопами характеризуется более высокими пространственным разрешением и глубиной резкости, а также возможностью проведения химического анализа на основе регистрации спектра рентгеновского излучения, генерируемого при облучении поверхности образца электронным пучком. Схема действия растрового электронного микроскопа: электроны, испускаемые электронной пушкой (нить накала обычно из вольфрама), ускоряются до энергии 2-40 кэВ; набор магнитных линз и отклоняющих катушек сканирования формирует электронный пучок малого диаметра, разворачиваемый в растр на поверхности образца. При облучении этой поверхности электронами возбуждаются три типа излучения, несущего полезную информацию: рентгеновские лучи, вторичные электроны и отраженные (обратнорассеянные) электроны. Пространственное разрешение сканирующего электронного микроскопа зависит от поперечного размера электронного пучка, который в свою очередь зависит от электронно-оптической системы, фокусирующей пучок. Разрешение также ограничено размером области взаимодействия электронного зонда с образцом, т. е. от материала мишени. Размер электронного зонда и размер области взаимодействия зонда с образцом намного больше расстояния между атомами мишени, таким образом, разрешение сканирующего электронного микроскопа не настолько велико, чтобы отображать атомарные масштабы, как это возможно, например, в просвечивающем электронном микроскопе.
 1
— первичный пучок электронов; 2 —
детектор вторичных электронов; 3
—детектор рентгеновского излучения;
4 — детектор отражённых электронов;
5 — детектор светового излучения; 6 —
детектор прошедших электронов; 7
—прибор для измерения наведённого на
объекте электрического потенциала; 8 —
прибор для измерения тока прошедших
через объект электронов; 9 — прибор для
измерения тока поглощенных в объекте
электронов.
1
— первичный пучок электронов; 2 —
детектор вторичных электронов; 3
—детектор рентгеновского излучения;
4 — детектор отражённых электронов;
5 — детектор светового излучения; 6 —
детектор прошедших электронов; 7
—прибор для измерения наведённого на
объекте электрического потенциала; 8 —
прибор для измерения тока прошедших
через объект электронов; 9 — прибор для
измерения тока поглощенных в объекте
электронов.
I-8. Визначення маси макромолекул
Три основні методи :
Седиментації(швидкості седиментації)
Седиментаційної рівноваги
Електрофорезу
І
 дейно
всі методи схожі : діють якоюсь силої і
дивляться як рухаються(або розподіляються)
частинки. Седиментація – осадження
частинок в рідині під дією гравітаційного
поля. Гравітаційне розділення в полі
Землі неможливе , оскільки теплової
енергії хватає щоб унеможливлювати
ефект на відстанях до
дейно
всі методи схожі : діють якоюсь силої і
дивляться як рухаються(або розподіляються)
частинки. Седиментація – осадження
частинок в рідині під дією гравітаційного
поля. Гравітаційне розділення в полі
Землі неможливе , оскільки теплової
енергії хватає щоб унеможливлювати
ефект на відстанях до Т
Т ому
використовується центрифуга (яка дає
прискорення до
ому
використовується центрифуга (яка дає
прискорення до
 ).
).
Метод
швидкості седиментації.
Позначки
 -
густина молекули,
-
густина молекули,
 -
густина рідини ,
-
густина рідини ,
 -
відстань від молекули до вісі обертання.
На молекулу діє дві сили : відцентрова
-
відстань від молекули до вісі обертання.
На молекулу діє дві сили : відцентрова
 і
виштовхувальна(Архімеда)
і
виштовхувальна(Архімеда) .
Молекула рухається з постійною(через
опір середовища) швидкістю
.
Молекула рухається з постійною(через
опір середовища) швидкістю
 ,
де
,
де
 -
параметр що характеризує рухливість
молекул.
-
параметр що характеризує рухливість
молекул.

В
цьому методі спостерігають за швидкістю
руху межі розділу
 .
Використовується
для макромолекул з малим коефіцієнтом
дифузії.
.
Використовується
для макромолекул з малим коефіцієнтом
дифузії.
Метод
седиментаційної рівноваги. Використовується
для важчих молекул(частинок).
Вимірюєтьсяконцентрацію молекул на
різних відстань від центра. Дифузійний
 і дрейфовий
і дрейфовий
 потоки
в рівновазі компенсують один одного:
потоки
в рівновазі компенсують один одного:

Проінтегрувавши
від
 до
до
 маємо:
маємо:

Де
 -концентрації
на відстанях
-концентрації
на відстанях
 відповідно.
відповідно.
Електрофорез. Використовує рух в електричному полі.

 -
рухливість в електричному полі. Білки
обробляють спец. препаратом(додецилсульфатнатрія),
який денатурує білок але не розщеплює
і прикріплює додаткові заряди до
молекули. Потім
поміщають в поліакриламідний гель в
якому і відбувається електрофорез.
Швидкість руху пропорційна заряду
молекули. Кількість зарядів пропорційна
довжині ланцюжка . Довжина ж пропорційна
масі. Таким чином всі поліпептиди мають
-
рухливість в електричному полі. Білки
обробляють спец. препаратом(додецилсульфатнатрія),
який денатурує білок але не розщеплює
і прикріплює додаткові заряди до
молекули. Потім
поміщають в поліакриламідний гель в
якому і відбувається електрофорез.
Швидкість руху пропорційна заряду
молекули. Кількість зарядів пропорційна
довжині ланцюжка . Довжина ж пропорційна
масі. Таким чином всі поліпептиди мають
 однаковий
питомий заряд і тому розділяються
обернено пропорційно логарифму їхньої
маси.
однаковий
питомий заряд і тому розділяються
обернено пропорційно логарифму їхньої
маси. .
Це емпіричний закон. Таким чином можна
знайти розподіл молекул по масі або
масу певної молекули. Аналогічно
робиться аналіз ДНК.
.
Це емпіричний закон. Таким чином можна
знайти розподіл молекул по масі або
масу певної молекули. Аналогічно
робиться аналіз ДНК.
I-9. Хімічні компоненти клітинних мембран.
В сі
живі клітини (як прокаріоти – прості
клітини, які не містять органел, так і
еукаріоти – клітини з органелами) мають
в своєму складі мембрани. Товщина
клітинної мембрани порядку 10 нм. Білки
і ліпіди складають основну частину
сухої маси клітинних мембран. Доля
вуглеводів зазвичай не перевищує 10-15%,
причому вони зв’язані або з білками
або з ліпідами. Вміст ліпідів коливається
в межах 25-75% по відношенню до вмісту
білків. До складу клітинних мембран
входять переважно ліпіди, що належать
до трьох класів : фосфоліпіди (в одному
з радикалів присутній залишок фосфорної
кислоти) – їх у мембрані найбільше,
сфінго- і гліколіпіди, а також стероїди.
Мембранні ліпіди мають порівняно
невелику полярну (заряджену дипольну)
голівку і довгі неполярні вуглеводневі
ланцюжки. Дипольна головка –
гідрофільна(розчинна в воді). Радикали
– гідрофобні (погано розчинні у воді).
сі
живі клітини (як прокаріоти – прості
клітини, які не містять органел, так і
еукаріоти – клітини з органелами) мають
в своєму складі мембрани. Товщина
клітинної мембрани порядку 10 нм. Білки
і ліпіди складають основну частину
сухої маси клітинних мембран. Доля
вуглеводів зазвичай не перевищує 10-15%,
причому вони зв’язані або з білками
або з ліпідами. Вміст ліпідів коливається
в межах 25-75% по відношенню до вмісту
білків. До складу клітинних мембран
входять переважно ліпіди, що належать
до трьох класів : фосфоліпіди (в одному
з радикалів присутній залишок фосфорної
кислоти) – їх у мембрані найбільше,
сфінго- і гліколіпіди, а також стероїди.
Мембранні ліпіди мають порівняно
невелику полярну (заряджену дипольну)
голівку і довгі неполярні вуглеводневі
ланцюжки. Дипольна головка –
гідрофільна(розчинна в воді). Радикали
– гідрофобні (погано розчинні у воді).
Ж ир
– складний ефір трьохатомного спирту
гліцерину (R-OH,
де R
– вуглеводневий радикал) і карбонових
кислот . Але жирів у мембрані
ир
– складний ефір трьохатомного спирту
гліцерину (R-OH,
де R
– вуглеводневий радикал) і карбонових
кислот . Але жирів у мембрані
немає, а є фосфоліпіди.
Жирні кислоти, що входять до складу ліпідів клітинних мембран мають 14-22 вуглецевих атоми. Вуглеводневі ланцюжки можуть бути або повністю насиченими, або містити 1-6 ненасичених зв’язків. Внаслідок того, що головка гідрофільна, а радикали гідрофобні, за наявності води (яка є також однією з основних складових клітинної мембрани) ліпідам енергетично вигідно «ховати» голівки і виставляти радикали.
Білковий склад клітинних мембран також дуже різноманітний. В основному це складні білки з молекулярною масою 10000-240000. Основну масу мембранних білків складають інтегровані білки – білки, сильно зв’язані з ліпідами мембран і сильно занурені в мембрани клітин (або зовсім пронизуючі їх). Зазвичай поліпептидні ланцюжки цих білків містять велику кількість неполярних амінокислотних залишків. Є також периферичні білки – ті, що зв’язані з мембраною порівняно слабо за рахунок не електростатичних взаємодій.
Вуглеводів у мембрані порівняно з білками і ліпідами невелика кількість. В основному вони приєднуються до білків, причому із зовнішньої сторони їх набагато більше, ніж всередині.
З усього вищесказаного, маємо, що клітинна мембрана має вигляд :

Це – рідинно-мозаїчна модель будови клітинної мембрани.
I-10. Типи мембранного транспорту.
1 ) Пасивний транспорт Дифузія нейтральний сполук
О писується
законом Фіка.
писується
законом Фіка.

Цей потік зростає коли збільшується концентрація як з зовн. так і внутр. сторони.
Дифузія йонів Закон Нерста-Планка:
 Знак
величини А пов’язаний з тим, якої
полярності йон. У будь-якому випадку
буде дифузія – навіть при
Знак
величини А пов’язаний з тим, якої
полярності йон. У будь-якому випадку
буде дифузія – навіть при
П олегшена
дифузія.
олегшена
дифузія.
Є

 білки, що забезпечують таку дифузію.
Білки перенощики. Інтегральний білок,
внаслідок структурних змін – захоплює
сполуку. Швидкодія до 103
с-1
білки, що забезпечують таку дифузію.
Білки перенощики. Інтегральний білок,
внаслідок структурних змін – захоплює
сполуку. Швидкодія до 103
с-1

Канальні білки відповідають за проникнення йонів. Утв. канал, по якому йон може вільно пересуватись. Пропускна здатність каналу залежить від потенціалу. Швидкодія до 106 йонів/сек
2) Активний транспорт
П ересування
речовин із затратою енергії.
ересування
речовин із затратою енергії.
Транспорт йонів
Білок
 -АТФаза
- або помпа, що перекачує іони.
-АТФаза
- або помпа, що перекачує іони.
Електрогенна помпа – переміщує заряди, сама створює різницю потенціалів.
3) Ендо- та екзоцитоз
Д
 озволяє
переносити молекули та фрагменти клітин.
Ендоцитоз – проникнення всередину
клітини за рахунок прогину мембрани.
Екзоцитоз – навпаки.
озволяє
переносити молекули та фрагменти клітин.
Ендоцитоз – проникнення всередину
клітини за рахунок прогину мембрани.
Екзоцитоз – навпаки.
I-11. Рівняння Томаса.
Стосується мембранного потенціалу спокою(калієвий рівноважний потенціал), його механізми, при обрахунку його величини. Мембранний потенціал спокою утворюється головним чином завдяки виходу К + з клітини через неселективні іонні канали. Витік з клітки позитивно заряджених іонів призводить до того, що внутрішня поверхня мембрани клітини заряджається негативно щодо зовнішньої. Мембранний потенціал, який виникає в результаті витоку К +, називають «рівноважних калієвий потенціалом» (Ек). Його можна розрахувати по рівнянню Нернста(питання №12). Але такий розрахунок не дає точне значення з наступних причин:
• надходження в клітину Na + та Cl-через неселективні іонні канали, при цьому надходження в клітину Cl-додатково гіперполяризує мембрану, а надходження Na + - додатково деполяризує її; внесок цих іонів у формування мембранного потенціалу невеликий, так як проникність неселективних каналів для Cl-і Na + в 2,5 і 25 рази нижче, ніж для К +.
• прямий електрогенний ефект Na + / К + іонного насосу, що виникає в тому випадку, якщо іонний насос працює асиметричною (На 2 іона, що надходять в клітину K + доводиться 3 іона Na +, що виносяться на зовнішнє середовище).
Саме формула Томаса враховує ці всі фактори:

 =
3/2
=
3/2
m - коефіцієнт електрогенності; С – концентрація; D – проникність;індекси in і out від повно всередині і зовні мембрани.
Тоді величина потенціалу спокою виходить близько-60-70мВ.
Як виводиться:
Розглянемо мембрану, крізь яку проходять тільки два види йонних струмів – відповідно калієвий всередину клітини та натрієвий назовні клітини.
Відомо що на 3 йони натрію з клітини припадає 2 йони каліє що потрапили до клітини, тобто співвідношення струмів буде:

У стаціонарному стані ці струми скомпенсовані:

Підставимо
вирази для струмів з рівняння Нернста-Планка

d(mD1C1+D2C2)+ (e/kT)(mD1 C1 +D2C2) dφ=0
(e/kT ) dφ=( - d(mD1C1+D2C2))/(mD1C1+ D2C2)
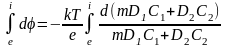 :
:
I-12. Рівняння Нернста
jn = - D(dc/dx) – DC(q/kT)( dφ/dx) – з-н. Нернста-Планка. - Р-ня. описує процес пасивного транспорту іонів в полі електрохімічного потенціалу.
 jni
= - Di(dci/dx) – DiCi
(qi/kT)(
dφ/dx).
jni
= - Di(dci/dx) – DiCi
(qi/kT)(
dφ/dx).
K+ : i=1; Na+ i=2. Позначимо активний: jA
(jA2 /jA1) = -3/2= - m, де m- деякий коефіцієнт.
jn2 = - jА2; jn1= - jА1 Звідси jn2 /jn1 = - m
m jn1 + jn2 =0
d(mD1C1+D2C2)+ (e/kT)(mD1 C1 +D2C2) dφ=0
(e/kT ) dφ=( - d(mD1C1+D2C2))/(mD1C1+ D2C2)
:
Δφ=kT/e ln
Показує зв’язок Δφ з концентрацією іонів двох типів (у випадку активного транспорту)- це р-ня Томаса.
Введемо коефіцієнти проникності для іонів. Pi=Di/Δxi
j(диф)= - D dc/dx ; jдиф Δx= - DΔC ΔC=C (i) -C (e)
 j(диф)=
-
D
ΔC/Δx,
D/Δx
= P.
j(диф)=
-
D
ΔC/Δx,
D/Δx
= P.
Δφ=kT/e ln((mp1С1(e)+p2C2(e))/(mp1C1(i)+p2C2(i)))
Якщо проникає лише якась одна речовина, тобто проникність для різних речовин –різна. P1:P2=1:0,04.
Тоді : Δφ=kT/e ln(С1(e)/С1 (i))- р-ня Нернста
Звідси СK+(e) = СK+(i) exp(e Δφ/kT)-екв. Р-ня. Больцмана
I-13. Рівняння Гольдмана-Ходшкін-Котца
Розглянемо випадок коли активний транспорт відсутній.
Закон Нернста-Планка:
 ;
де jiп
– потік пасивного транспорту і-го
елементу, D
– коеф.диф.,
С
– кнцентрація і-го
елементу, q
– заряд.
;
де jiп
– потік пасивного транспорту і-го
елементу, D
– коеф.диф.,
С
– кнцентрація і-го
елементу, q
– заряд.
Наближення постійного поля(Гольдман-Ходшкін-Котц):
 --
потенціал розподілений рівномірно.
--
потенціал розподілений рівномірно.
=>


 -
проникність,
-
проникність,
 - так позначимо безрозмірний потенціал.
- так позначимо безрозмірний потенціал.


Щоб урахувати всі потоки:
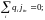 для
різних і-х
іонів.
для
різних і-х
іонів.
Отже через наближення маємо jiп лише через Ka+, Na+, Cl+ :
 --
Гольдман-Ходшкін-Котц;
--
Гольдман-Ходшкін-Котц;
I-14. Будова нейронів та їх оболонок
Центральная нервная система имеет клеточное строение. Единица – нервная клетка, нейрон. Нейрон имеет следующие основные свойства:
1. Участвует в обмене веществ и рассеивает энергию. Меняет внутреннее состояние с течением времени, реагирует на входные сигналы и формирует выходные воздействия и поэтому является активной динамической системой.
2. Имеет множество синапсов – контактов для передачи информации.
3. Нейрон взаимодействует путем обмена электрохимическими сигналами двух видов: электротоническими (с затуханием) и нервными импульсами (спайками), распространяющимися без затухания.
Биологический нейрон содержит следующие структурные единицы:
 Тело
клетки (т) — сома: содержит ядро (я),
митохондрии (обеспечивают клетку
энергией), другие органеллы, поддерживающие
жизнедеятельность клетки.
Тело
клетки (т) — сома: содержит ядро (я),
митохондрии (обеспечивают клетку
энергией), другие органеллы, поддерживающие
жизнедеятельность клетки.
Дендриты (д) – входные волокна, собирают информацию от других нейронов. Активность в дендритах меняется плавно. Длина их обычно не больше 1 мм.
Мембрана – поддерживает постоянный состав цитоплазмы внутри клетки, обеспечивает проведение нервных импульсов.
Цитоплазма — внутренняя среда клетки. Отличается концентрацией ионов K , Na , Ca и других веществ по сравнению с внеклеточной средой.
Аксон (а), один или ни одного у каждой клетки, – длинное, иногда больше метра, выходное нервное волокно клетки. Импульс генерируется в аксонном холмике (а.х.). Аксон обеспечивает проведение импульса и передачу воздействия на другие нейроны или мышечные волокна (мв). Ближе к концу аксон часто ветвится.
Синапс (с) – место контакта нервных волокон — передает возбуждение от клетки к клетке. Передача через синапс почти всегда однонаправленная. Различают пресинаптические и постсинаптические клетки — по направлению передачи импульса.
Шванновские клетки (шв.кл). Специфические клетки, почти целиком состоящие из миелина, органического изолирующего вещества. Плотно "обматывают" нервное волокно 250 слоями миелина. Неизолированные места нервного волокна между шванновскими клетками называются перехватами Ранвье (пР). За счет миелиновой изоляции скорость распространения нервных импульсов возрастает в 510 раз и уменьшаются затраты энергии на проведение импульсов. Миелинизированныеволокна встречаются только у высших животных.
В центральной нервной системе человека насчитывается от 100 до 1000 типов нервных клеток, в зависимости выбранной степени детализации. Они отличаются картиной дендритов, наличием и длиной аксона и распределением синапсов около клетки.
Клетки сильно связаны между собой. У нейрона может быть больше 1000 синапсов. Близкие по функциям клетки образуют скопления, шаровидные или параллельные слоистые. В мозгу выделены сотни скоплений. Кора головного мозга – тоже скопление. Толщина коры — 2 мм, площадь — около квадратного фута.
Мембрана. Мембранный потенциал.
Клеточная мембрана создает и поддерживает постоянную концентрацию веществ внутри клетки, механическую прочность клетки и транспортировку молекул и ионов в обоих направлениях. Для нервных волокон она обеспечивает проведение нервных импульсов по волокну.
Мембрана состоит из двух слоев молекул липидов (жиров). Молекулы липидов содержат полярную "голову" и два гидрофобных углеводородных "хвоста". Молекулы ориентированы "хвостами" внутрь мембраны. Такая конструкция оказывается стабильной и энергетически выгодной (по структуре она аналогична пленке мыльного пузыря). Молекулы белков взаимодействуют с такой двухслойной структурой. Белки с гидрофобными поверхностями взаимодействуют с "хвостами" липидов и встраиваются в саму мембрану, а с гидрофильными — соединяются с поверхностью мембраны. По химическому составу мембраны весьма разнообразны. Толщина мембраны около 10 нм.
В состав мембраны входит множество механизмов, необходимых для работы клетки. Мы будем рассматривать только те, что имеют отношение к передаче нервных сигналов.
Натриевый насос
Внутри клетки, в цитоплазме, преобладают ионы K+, снаружи — Na+. Активный мембранный транспорт, натриевый насос, переносит K+ внутрь, а Na+ — наружу. Такой перенос происходит в направлении роста электрохимического потенциала и требует затрат энергии. Для работы натриевого насоса используется энергия гидролиза АТФ (аденозинтрифосфата) — основного энергетического аккумулятора клетки. Механизм переноса использует белок*носитель, обозначим его C, образующий комплекс с ионами на одной стороне и отщепляющий эти ионы на противоположной стороне мембраны. Ни носитель, ни комплексы CK, CФNa с ионами Na+, K+: не покидают мембрану. В итоге через мембрану проходят потоки ионов K+ и Na+, направленные: K+ — внутрь клетки, Na+ — наружу.
В результате работы натриевого насоса концентрация K+ и Na+ становится неравновесной, но электрический потенциал мембраны не меняется, так как количество ионов K+, перенесенных внутр. клетки, совпадает с количеством ионов Na+, перенесенных наружу. Поэтому суммарный перенос заряда равен нулю и электрический потенциал цитоплазмы не меняется.
Калиевые каналы
В мембране существуют каналы, пропускающие только ионы K+ в обоих направлениях. Каналы являются управляемыми, и могут открываться или закрываться в зависимости от разности потенциалов между цитоплазмой и внешней средой, а также обладают инерционными свойствами. В состоянии покоя часть K+ каналов открыта. Из-за разницы концентраций K+ и Na+ на разных сторонах мембраны ионы K начинают диффундировать через K-каналы из цитоплазмы наружу. Этот процесс приводит к оттоку положительного заряда из клетки, и цитоплазма заряжается отрицательно. Возникают кулоновские силы, препятствующие дальнейшей диффузии ионов K+. Как только эти процессы уравновешивают друг друга, диффузия ионов K+ через K-каналы прекращается, и потенциал цитоплазмы достигает равновесного состояния - 70 мВ.
В состоянии покоя разница потенциалов на мембране определяется формулой Ходжкина*Катца:
![]()
где PK — проницаемость для мембраны для ионов K+, PK — концентрация K+ внутри клетки, ceK — снаружи, аналогично для других ионов. Формула выводится, исходя из однородности поля на мембране, если диффузионные токи IK и INa известны. Значение потенциала покоя 70..80 мВ, полученное по этой формуле, согласуется с экспериментальными значениями.
Калиевые каналы открываются при изменении потенциала в положительную сторону и остаються открытыми, пока потенциал сохраняет свое значение. Натриевые каналы Na-каналы аналогичны калиевым, но пропускают только ионы Na+. Отличаются также уровнем потенциала, открывающим канал, и инерционными характеристиками. В состоянии покоя Na-каналы закрыты. Натриевые каналы также открываются при изменении потенциала протоплазмы в положительную сторону. Закрываются сами по себе, через некоторое время после открытия. Закрывшись, находятся в состоянии рефрактерности в течение примерно 1 мс и не могут открыться снова до окончания рефрактерности.
I-15. Кабельна теорія поширення нервового імпульсу вздовж неміелізованого аксона нейронів

Клітина в стані спокою знаходиться в поляризованому стані.
В ивести
зі стану спокою її можна за допомогою
електричного поля, хім..сполук, механічним
способом.
ивести
зі стану спокою її можна за допомогою
електричного поля, хім..сполук, механічним
способом.
При цьому поляризація відновлюється протягом 1 мкс. Тому при збудженні клітини(аксона) по ньому побіжить імпульс.
Кабельна модель. (Запишемо телеграфічне рівняння):
 r=
50Om*cm
S=1mkm2
l=1cm
R= 5ГОм.
r=
50Om*cm
S=1mkm2
l=1cm
R= 5ГОм.

 ;
;
 ;
;

 Вираз
для
Вираз
для
 знайшли
Ходжкін і Хакелі.(тут V=
знайшли
Ходжкін і Хакелі.(тут V=
 )
)


 -
рівноважні потенціали. Альфа
і бета – коофіціенти, що вимірюються
експериментально.
-
рівноважні потенціали. Альфа
і бета – коофіціенти, що вимірюються
експериментально.
Впринципі
все. Однак, якщо ввести заміну
 і підставити в
тоді можна отримати
і підставити в
тоді можна отримати
 v
– швидкість поширення імпульсу. V=10-100
м/с.
v
– швидкість поширення імпульсу. V=10-100
м/с.
I-16. Математична модель Ходжкіна-Хакслі
Еквівалентна схема нервового волокна:
Х арактерні
значення параметрів:
арактерні
значення параметрів:
C=1мкФ/см2, EK=70мВ, ENa=30мВ.
Я к
відомо з курсу радіотехнічні кола та
сигнали, систему з розподіленими
параметрами можна описати шляхом
введення погонних параметрів (ємність,
опір на одиницю довжини). Нервове волокно
вданому розгляді не відрізняється від
довгої лінії. Отже запишемо телеграфні
рівняння:
к
відомо з курсу радіотехнічні кола та
сигнали, систему з розподіленими
параметрами можна описати шляхом
введення погонних параметрів (ємність,
опір на одиницю довжини). Нервове волокно
вданому розгляді не відрізняється від
довгої лінії. Отже запишемо телеграфні
рівняння:


Заслуга Ходжкіна-Хакслі полягае в тому, що вони на основі експериментальних досліджень запропонували модель:

 величини
провідностей для відповідних типів
іонів(max
для
К)
величини
провідностей для відповідних типів
іонів(max
для
К)
 змінюються
від 0 до 1, для них отримані емпірично
рівняння:
змінюються
від 0 до 1, для них отримані емпірично
рівняння:


Для
спрощення вихідного рівняння для
потенціалу перейдемо до супроводжуючої
системи координат, тобто шукатимемо
автомодельний розвязок(аНі7ов): Отримаємо:
Отримаємо: Розвяжемо
рівняння отримане рівняння: проаналізуємо
модель нейрона
Розвяжемо
рівняння отримане рівняння: проаналізуємо
модель нейрона



Будемо розглядати рівняння відносно іншої функції (це видно зі структури рівняня):
 Нову
функцію шукатимемо у вигляді:
Нову
функцію шукатимемо у вигляді:

Сталі знайдемо з граничних умов:
 Отримане
рівняння в достатній мірі описує
розповсюдження нервового імпульсу в
волокні. Оцінемо швидкість його поширення
(знайдемо швидкість руху максимуму
потенціалу описуваного формулою (*):
Отримане
рівняння в достатній мірі описує
розповсюдження нервового імпульсу в
волокні. Оцінемо швидкість його поширення
(знайдемо швидкість руху максимуму
потенціалу описуваного формулою (*):


Залежність швидкості від діаметра волокна:

Для
порівняння:

I-17. Миелизированные волокна. Сальтаторный режим
Н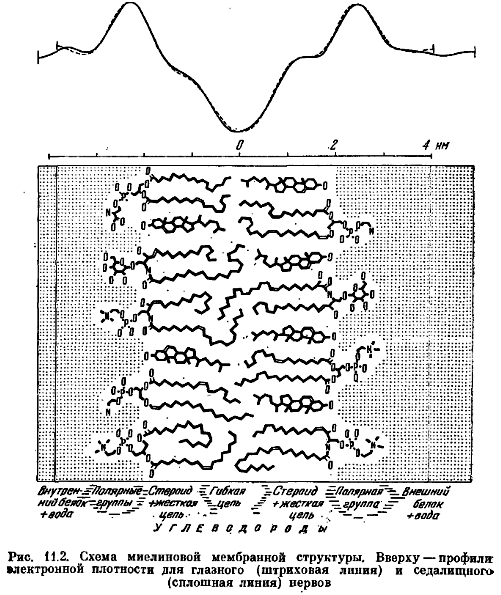
 а
рис. 11.1 представлена схема строения
нервной клетки – нейрона. Клетка получает
сообщения от многих других нейронов
через их тонкие ответвления, образующие
контакты – синапсы – с телом клетки и
его короткими отростками – дендритами.
Контакты с другими клетками образуются
не только в синапсах. Большая часть
поверхности нейрона покрыта прилегающими
к нему глиальными, или шванновскими
клетками. Из мембран шванновских клеток
образуется миелиновая оболочка
миелинизированных аксонов. Эта оболочка
прерывается через каждые 1-2 мм длины
аксона перехватами Ранвье, имеющими
протяженность около 1 мкм. В области
перехвата мембрана аксона контактирует
с окружающей средой. Существуют и
немиелинизированные аксоны. Миелиновая
оболочка аксона образована многократным
спиральным закручиванием мембраны
шванновской клетки вокруг аксона. Миелин
представляет собой многослойную
мембрану(до 250 слоев), защищающую мембрану
аксона от окружающей среды. На рис. 11.2
показана схема миелиновой мембранной
структуры, полученная методом
рентгенографии. Скорость распространения
импульса равна v=1–100
м/с, она меньше для немиелинизированных
и больше для миелинизированных аксонов.
Так, для миелинизированных волокон
кошки v=10–100
м/с, для гигантского аксона кальмара(диаметр
волокна 600 мкм!) v=25
м/с, для немиелинизированных волокон
кошки v=0,7–2,3
м/с. В миелинизированном аквоне проведение
импульса является сальтаторным, т.е.
происходит путем перескока импульса
от одного перехвата Ранвье к другому.
Калиевые и натриевые каналы открываются
и закрываются только в перехватах Ранвье
– миединизированные участки хорошо
изолированы. Миелин имеет малую емкость,
чем и объясняется большая скорость
проведения импульса. Схема сальтаторного
проведения импульса показана на рис.
11.10. Миелинизация, свойственная аксонам
позвоночных, обеспечила им эволюционное
преимущество, так как при той же скорости
проведения импульса миелинизированное
волокно может быть в 25 раз тоньше
немиелинизированного.
а
рис. 11.1 представлена схема строения
нервной клетки – нейрона. Клетка получает
сообщения от многих других нейронов
через их тонкие ответвления, образующие
контакты – синапсы – с телом клетки и
его короткими отростками – дендритами.
Контакты с другими клетками образуются
не только в синапсах. Большая часть
поверхности нейрона покрыта прилегающими
к нему глиальными, или шванновскими
клетками. Из мембран шванновских клеток
образуется миелиновая оболочка
миелинизированных аксонов. Эта оболочка
прерывается через каждые 1-2 мм длины
аксона перехватами Ранвье, имеющими
протяженность около 1 мкм. В области
перехвата мембрана аксона контактирует
с окружающей средой. Существуют и
немиелинизированные аксоны. Миелиновая
оболочка аксона образована многократным
спиральным закручиванием мембраны
шванновской клетки вокруг аксона. Миелин
представляет собой многослойную
мембрану(до 250 слоев), защищающую мембрану
аксона от окружающей среды. На рис. 11.2
показана схема миелиновой мембранной
структуры, полученная методом
рентгенографии. Скорость распространения
импульса равна v=1–100
м/с, она меньше для немиелинизированных
и больше для миелинизированных аксонов.
Так, для миелинизированных волокон
кошки v=10–100
м/с, для гигантского аксона кальмара(диаметр
волокна 600 мкм!) v=25
м/с, для немиелинизированных волокон
кошки v=0,7–2,3
м/с. В миелинизированном аквоне проведение
импульса является сальтаторным, т.е.
происходит путем перескока импульса
от одного перехвата Ранвье к другому.
Калиевые и натриевые каналы открываются
и закрываются только в перехватах Ранвье
– миединизированные участки хорошо
изолированы. Миелин имеет малую емкость,
чем и объясняется большая скорость
проведения импульса. Схема сальтаторного
проведения импульса показана на рис.
11.10. Миелинизация, свойственная аксонам
позвоночных, обеспечила им эволюционное
преимущество, так как при той же скорости
проведения импульса миелинизированное
волокно может быть в 25 раз тоньше
немиелинизированного. За один импульс в немиелинизированном
аксоне через 1 мкм2
поверхности
проходит около 20000 ионов Na+.
В миелинизированном аксоне за один
импульс через каждый перехват Ранвье
входит 6*106
ионов Na+.
Площадь мембраны в перехвата равна 20
мкм2,
значит, через 1 мкм2
проходит 300000 ионов Na+.
Плотность ионного тока в перехвате
примерно в 10 раз больше, чем в
немиелинизированных гигантских аксонах.
За один импульс в немиелинизированном
аксоне через 1 мкм2
поверхности
проходит около 20000 ионов Na+.
В миелинизированном аксоне за один
импульс через каждый перехват Ранвье
входит 6*106
ионов Na+.
Площадь мембраны в перехвата равна 20
мкм2,
значит, через 1 мкм2
проходит 300000 ионов Na+.
Плотность ионного тока в перехвате
примерно в 10 раз больше, чем в
немиелинизированных гигантских аксонах.
I-18. Синоптична передача збуджень. Типи синапсів. Нейромедіатори
Синaпс – специализированный контакт между нервными клетками (или нервными и другими возбудимыми клетками), обеспечивающий передачу возбуждения с сохранением его информационной значимости.
Классификация синапсов
По морфологическому принципу синапсы подразделяют на:
• нейро-мышечные (аксон нейрона контактирует с мышечной клеткой);
• нейро-секреторные (аксон нейрона контактирует с секреторной клеткой);
• нейро-нейрональные (аксон нейрона контактирует с другим нейроном):
• аксо-соматические (с телом другого нейрона), • аксо-аксональные (с аксоном другого нейрона), • аксо-дендритические (с дендритом другого нейрон).
По способу передачи возбуждения синапсы подразделяют на:
• электрические (возбуждение передается при помощи электрического тока);
• химические (возбуждение передается при помощи химического вещества):
По физиологическому эффекту синапсы подразделяют на:
• возбуждающие (деполяризуют постсинаптическую мембрану и вызывают возбуждение постсинаптической клетки);
• тормозные (гиперполяризуют постсинаптическую мембрану и вызывают торможение постсинаптической клетки).
Ультраструктура синапсов
Все синапсы имеют общий план строения.

Конечная часть аксона (синаптическое окончание), подходя к иннервируемой клетке, теряет миелиновую оболочку и образует на конце небольшое утолщение (синаптическую бляшку). Ту часть мембраны аксона, которая контактирует с иннервируемой клеткой, называют пресинаптической мембраной. Синаптическая щель – узкое пространство между пресинаптической мембраной и мембраной иннервируемой клетки, которое является непосредственным продолжением межклеточного пространства. Постсинаптическая мембрана – участок мембраны иннервируемой клетки, контактирующий с пресинаптической мембраной через синаптическую щель.
Особенности ультраструктуры электрического синапса:
• узкая (около 5 нм) синаптическая щель; • наличие поперечных канальцев, соединяющих пресинаптическую и постсинаптическую мембрану.
Особенности ультраструктуры химического синапса:
• широкая (20–50 нм) синаптическая щель; • наличие в синаптической бляшке синаптических пузырьков (везикул), заполненных химическим веществом (нейромедиатором), при помощи которого передается возбуждение; • в постсинаптической мембране имеются многочисленные хемочувствительные каналы (в возбуждающем синапсе – для Nа+ , в тормозном – для Cl – и К +), но отсутствуют потенциалчувствительные каналы.
Механизм передачи возбуждения в электрическом синапсе
Механизм проведения возбуждения аналогичен механизму проведения возбуждения в нервном волокне. Во время развития ПД (потенциала действия) происходит реверсия заряда пресинаптической мембраны. Электрический ток, возникающий между пресинаптической и постсинаптической мембраной, раздражает постсинаптическую мембрану и вызывает генерацию в ней ПД.
Этапы и механизмы передачи возбуждения в возбуждающем химическом синапсе
На пресинаптической мембране осуществляется трансформация электрического сигнала в химический, который на постсинаптической мембране снова трансформируется в электрический сигнал.
