
- •Введение: основные понятия и определения
- •Основы номенклатуры неорганических соединений можно изложить следующим образом:
- •1 Классы неорганических соединений
- •Растворимость солей, кислот и оснований в воде
- •2 Химическая термодинамика
- •3 Скорость химических реакций
- •3.1 Количественное определение скорости химической реакции
- •3.2 Влияние катализатора
- •4 Химическое равновесие
- •4.1 Понятие о химическом равновесии
- •4.2 Динамический характер и устойчивость химического равновесия
- •4.3 Константа химического равновесия
- •4.4 Положение равновесия и его зависимость от внешних факторов
- •4.4.1 Зависимость равновесия от концентрации
- •4.4.2 Зависимость равновесия от температуры
- •4.4.3 Влияние давления на равновесие
- •4.4.4 Влияние катализатора на равновесие
- •В выражение константы равновесия входят равновесные концентрации веществ:
- •5 Строение электронных оболочек атомов. Периодический закон д.И. Менделеева
- •6 Химическая связь и строение молекул
- •7 Растворы
- •7.1 Способы выражения концентрации растворов
- •7.2 Физико-химические свойства разбавленных растворов неэлектролитов. Давление пара растворов. Закон Рауля
- •7.2.1 Понижение температуры замерзания и повышение температуры кипения растворов (следствия из закона Рауля)
- •7.3 Растворы электролитов
- •7.4 Ионное произведение воды. Водородный показатель рН
- •8 Окислительно-восстановительные реакции
- •9 Гальванические элементы
- •9.1 Понятие об электродном потенциале
- •9.2 Гальванический элемент
- •10 Коррозия металлов
- •10.1 Защита от коррозии
- •11 Электролиз
- •11.1 Катодные процессы
- •11.2 Анодные процессы
- •12 Полимеры
- •12.1 Реакция полимеризации
- •12.2 Реакция поликонденсации
- •12.3 Полимерные материалы
- •13 Дисперсные системы
- •14 Химический анализ
- •Библиографический список
- •Содержание
- •Ризография ргупс.
4.4.2 Зависимость равновесия от температуры
Рассмотрим
зависимость химического равновесия от
температуры с помощью принципа Ле-Шателье.
Пусть наша реакция экзотермична, то
есть идет слева направо с выделением
тепла (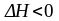 ).
Кстати, отметим, когда равновесие
установится, теплота не выделяется и
не поглощается системой, иначе бы
нарушился закон сохранения энергии
(первое начало термодинамики). При
нагревании системы в состоянии равновесия
её температура начнёт повышаться. Чтобы
скомпенсировать внешнее воздействие
– рост температуры (сдержать её
повышение), равновесие сдвинется влево
– в сторону противоположной реакции,
которая эндотермична (идет с поглощением
тепла
).
Кстати, отметим, когда равновесие
установится, теплота не выделяется и
не поглощается системой, иначе бы
нарушился закон сохранения энергии
(первое начало термодинамики). При
нагревании системы в состоянии равновесия
её температура начнёт повышаться. Чтобы
скомпенсировать внешнее воздействие
– рост температуры (сдержать её
повышение), равновесие сдвинется влево
– в сторону противоположной реакции,
которая эндотермична (идет с поглощением
тепла
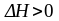 ).
Поглощение тепла позволит системе по
возможности сохранить своё состояние
– неизменность
температуры в равновесии. Если же эту
систему охлаждать и её температура
станет уменьшаться, равновесие, чтобы
скомпенсировать внешнее воздействие,
стремится в сторону экзотермической
реакции, то есть вправо. Последняя
реакция, выделяя тепло, приостановит
понижение температуры.
).
Поглощение тепла позволит системе по
возможности сохранить своё состояние
– неизменность
температуры в равновесии. Если же эту
систему охлаждать и её температура
станет уменьшаться, равновесие, чтобы
скомпенсировать внешнее воздействие,
стремится в сторону экзотермической
реакции, то есть вправо. Последняя
реакция, выделяя тепло, приостановит
понижение температуры.
Из
изложенного видно, что влияние
температуры на положение химического
равновесия подчиняется следующему
правилу: при повышении температуры
химическое равновесие смещается в
сторону эндотермической реакции, а при
понижении температуры – в сторону
экзотермической реакции. Примером
может служить реакция синтеза аммиака,
которая экзотермична (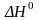 =
–92 кДж).
=
–92 кДж).
N2 + 3H2 Á 2 NH3; = –92 кДж.
Нагревание системы приведет к смещению положения равновесия влево, в сторону исходных веществ – водорода и азота, а охлаждение – вправо, в сторону образования аммиака.
4.4.3 Влияние давления на равновесие
Во
всех реакциях с участием газообразных
веществ (реагентов и продуктов),
сопровождающихся изменением общего
числа частиц (числа молей) при переходе
от реагентов к продуктам, на положение
равновесия оказывает влияние давление.
Продолжим рассмотрение реакции синтеза
аммиака, приведённой выше. При протекании
реакции слева направо из четырех частиц
(четырёх молей) – одной азота (одного
моля) и трех водорода (трёх молей),
образуются две частицы аммиака (два
моля). Таким образом, число частиц
уменьшается. Если увеличить давление
в системе, где имеется равновесие реакции
образования аммиака, число частиц в
единице объёма системы начнёт возрастать.
В соответствии с принципом Ле-Шателье,
равновесие сместится в сторону той
реакции, которая будет препятствовать
увеличению числа частиц в единице объёма
системы, то есть вправо, в сторону
образования аммиака, так как эта реакция
снижает число частиц в системе. Напротив,
при уменьшении давления в системе,
равновесие сместится влево, в сторону
образования исходных веществ. Эта
реакция увеличивает число частиц в
системе и компенсирует за счёт этого
уменьшение давления. Обобщая этот
результат, приходим к выводу: увеличение
давления смещает равновесие химической
реакции в сторону образования меньшего
числа частиц в газовой системе, а
уменьшение давления – в сторону
образования большего числа частиц. Если
же в результате гомогенной реакции в
газовой фазе общее число частиц не
изменяется, изменение давления в системе
не оказывает влияния на положение
равновесия. Этот
же вывод легко получить, рассматривая
выражение для константы химического
равновесия
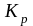 (4.5).
(4.5).
