
- •Внутрішня енергія ідеального газу. Робота газу при зміненні його об'єму. Перший закон термодинаміки. Адіабатичний процес. Теплові машини План
- •Основи термодинаміки. Внутрішня енергія тіла. Внутрішня енергія ідеального газу. Способи зміни внутрішньої енергії.
- •Перший закон термодинаміки. Робота газу при зміні його об'єму. Можливі дві форми передавання енергії від одного тіла до іншого, а, отже, і зміни внутрішньої енергії системи.
- •Перший закон термодинаміки - закон збереження і перетворення енергії, застосований до термодинамічних процесів.
- •Теплоємність. Теплоємністю тіла називається фізична величина, яка числово дорівнює кількості теплоти, яку потрібно надати тілу, щоб підвищити його температуру на один кельвін:
- •І зотермічний процес
Теплоємність. Теплоємністю тіла називається фізична величина, яка числово дорівнює кількості теплоти, яку потрібно надати тілу, щоб підвищити його температуру на один кельвін:
![]()
Значення
![]() Залежить від маси тіла, його хімічного
складу, термодинамічного стану і
виду процесу зміни стану тіла, в якому
надходить теплота
Залежить від маси тіла, його хімічного
складу, термодинамічного стану і
виду процесу зміни стану тіла, в якому
надходить теплота![]() .
.
Питомою
теплоємністю![]() називається
фізична величина, що числова дорівнює
кількості теплоти, яку слід надати
одиниці маси цієї речовини для підвищення
її температури на
називається
фізична величина, що числова дорівнює
кількості теплоти, яку слід надати
одиниці маси цієї речовини для підвищення
її температури на![]() :
:
![]()
Молярною
теплоємністю![]() називається фізична величина, яка
числово дорівнює кількості теплоти,
яку треба надати одному молю речовини
для підвищення його температури на
називається фізична величина, яка
числово дорівнює кількості теплоти,
яку треба надати одному молю речовини
для підвищення його температури на![]() :
:
![]()
![]()
де - кількість молей газу.
Між
молярною теплоємністю
![]() і питомою теплоємністю
і питомою теплоємністю![]() існує
співвідношення:
існує
співвідношення:![]()
Оскільки
величина теплоємності газу залежить
від умов, при яких йому надається
кількість теплоти, то розрізняють
теплоємність
при сталому об'ємі
![]() і
теплоємність при сталому тиску
і
теплоємність при сталому тиску![]() .
.
Якщо нагрівають газ, то згідно з першим законом термодинаміки
![]()
![]()
а для одного моля газу
Я![]()
![]() кщо
газ нагрівається при сталому об'ємі, то
надана газу теплота йде лише на збільшення
його внутрішньої енергії:
кщо
газ нагрівається при сталому об'ємі, то
надана газу теплота йде лише на збільшення
його внутрішньої енергії:
Я![]() кщо
газ нагрівається при постійному тиску,
то
кщо
газ нагрівається при постійному тиску,
то
Згідно з рівнянням Менделєєва-Клапейрона
![]()
В результаті
![]()
Отриманий
вираз називається рівнянням
Маєра.
Воно вказує на те, що![]() завжди
більше від
завжди
більше від![]() на величину універсальної газової
сталої. Це пояснюється тим, що під час
нагрівання газу при сталому тиску
потрібна додаткова кількість теплоти
на виконання роботи розширення газу.
на величину універсальної газової
сталої. Це пояснюється тим, що під час
нагрівання газу при сталому тиску
потрібна додаткова кількість теплоти
на виконання роботи розширення газу.
О![]()
![]() скільки ,
то
скільки ,
то
![]()
ЗАСТОСУВАННЯ ПЕРШОГО ЗАКОНУ ТЕРМОДИНАМІКИ ДО ІЗОПРОЦЕСІВ. Ізопроцесами в газах називаються процеси, при яких один із основних параметрів стану (
 )
зберігається
постійним.
Ізохорний
процес
(
)
зберігається
постійним.
Ізохорний
процес
( ).
).
При ізохорному процесі газ не виконує роботи над зовнішніми тілами:
![]()
Отже,
з першого закону термодинаміки
![]() для
ізохорного процесу
випливає, що
для
ізохорного процесу
випливає, що
![]() .
Оскільки
.
Оскільки
![]() ,
то для довільної маси газу
,
то для довільної маси газу
![]()
Ізобарний
процес
(![]() ).
).
Р![]() обота,
яку виконує
газ при ізобарному
розширенні від об'єму
обота,
яку виконує
газ при ізобарному
розширенні від об'єму
![]() до
до
![]() ,
дорівнює
,
дорівнює
д![]() е
використано рівняння Менделєєва-Кла-пейрона.
е
використано рівняння Менделєєва-Кла-пейрона.
При
ізобарному процесі при наданні
газу масою![]() кількості
теплоти
кількості
теплоти
його внутрішня енергія зростає на величину
![]()
Газ виконує роботу
![]()
І зотермічний процес
Робота газу при ізотермічному розширенні:
При
![]() внутрішня
енергія ідеального
газу не змінюється, тобто
внутрішня
енергія ідеального
газу не змінюється, тобто
![]()
т![]() обто
вся кількість теплоти, надана газу,
витрачається
на виконання ним роботи проти
зовнішніх сил:
обто
вся кількість теплоти, надана газу,
витрачається
на виконання ним роботи проти
зовнішніх сил:
Робота
розширення газу (![]() )
додатна.
У випадку стиску газу (процес 1-3)
робота
)
додатна.
У випадку стиску газу (процес 1-3)
робота![]() ,
що виконується газом, від'ємна, водночас
зовнішні сили виконують додатну
роботу
,
що виконується газом, від'ємна, водночас
зовнішні сили виконують додатну
роботу
![]() .
При цьому
.
При цьому![]() тобто теплота від газу відводиться.
тобто теплота від газу відводиться.
АДІАБАТНИЙ ПРОЦЕС. ЗАСТОСУВАННЯ ПЕРШОГО ЗАКОНУ ТЕРМОДИНАМІКИ ДО АДІАБАТНОГО ПРОЦЕСУ ІДЕАЛЬНОГО ГАЗУ.Адіабатний - це такий процес, який відбувається без обміну теплотою (
 )
між
термодинамічною системою і
середовищем.
)
між
термодинамічною системою і
середовищем.
При яких умовах можна реально здійснити адіабатний процес. Можливо в трьох випадках здійснити процес, який буде адіабатним.
В першому випадку необхідна адіабатна оболонка, теплопровідність якої дорівнює нулю. Такою оболонкою може служити посудина Дьюара. В такій посудині з подвійними посрібленими стінками, з простору між якими відкачано повітря, передачі теплоти через стінки практично не буде.
Другий
випадок
адіабатичних процесів
- це процеси, що відбуваються дуже
швидко.
При швидкому стиску газу затрачається
робота![]() ,
в наслідок чого збільшується
внутрішня енергія
,
в наслідок чого збільшується
внутрішня енергія![]() ,
що викликає
підвищення температури. При підвищенні
температури деяка кількість теплоти
,
що викликає
підвищення температури. При підвищенні
температури деяка кількість теплоти
![]() повинна
бути передана навколишньому
середовищі, що знаходиться при нижчій
температурі, але процес теплопередачі
вимагає деякого часу, тому при швидкому
стиску теплота не встигає поширитись
з даного об'єму.
повинна
бути передана навколишньому
середовищі, що знаходиться при нижчій
температурі, але процес теплопередачі
вимагає деякого часу, тому при швидкому
стиску теплота не встигає поширитись
з даного об'єму.
Третій випадок - це процеси, що відбуваються в дуже великих об'ємах газу, наприклад, в атмосфері. Якщо в атмосфері відбудеться зменшення тиску - розрідження, яке виникає внаслідок атмосферної діяльності, то кількість теплоти, яка повинна бути передана із навколишнього простору для того, щоб вирівняти температуру, яка понизилась внаслідок адіабатичного розширення, просто не встигне поширитися упродовж значного проміжку часу.
![]()
Цей вираз називається рівнянням Пуассона.
Д ля
переходу до змінних
ля
переходу до змінних![]() ,
,![]() виключимо з рівняння Пуассона за
допомогою рівняння Менделєєва-Клапейрона
тиск:
виключимо з рівняння Пуассона за
допомогою рівняння Менделєєва-Клапейрона
тиск:
Оскільки
об'єм
![]() ,
то, підставивши цей вираз в рівняння
,
то, підставивши цей вираз в рівняння
О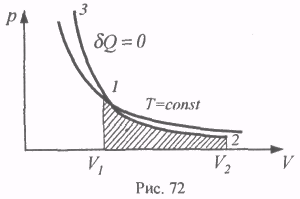 тже,
тже,![]()
Побудуємо графіки рівнянь:
1)
![]() (адіабата),
(адіабата),
2)
![]() (ізотерма)
(ізотерма)
Отже,
тангенс кута нахилу адіабати в
![]() разів
більший, ніж в ізотерми. Це пояснюється
тим, що при адіабатному стиску 1-3
тиск
газу збільшується не лише внаслідок
зменшення його об'єму, як при ізотермічному
стиску, але і підвищенням температури.
При адіабатному розширенні газу 1-2
його
температура знижується і тому тиск
зменшується швидше, ніж при ізотермічному
розширенні.
разів
більший, ніж в ізотерми. Це пояснюється
тим, що при адіабатному стиску 1-3
тиск
газу збільшується не лише внаслідок
зменшення його об'єму, як при ізотермічному
стиску, але і підвищенням температури.
При адіабатному розширенні газу 1-2
його
температура знижується і тому тиск
зменшується швидше, ніж при ізотермічному
розширенні.
КОЛОВИЙ ПРОЦЕС. ТЕПЛОВІ ДВИГУНИ І ХОЛОДИЛЬНІ МАШИНИ. ОБОРОТНІ І НЕОБОРОТНІ ПРОЦЕСИ. Коловим процесом (циклом) називається процес, при якому система, пройшовши через ряд станів, повертається у вихідний стан. На діаграмі процесів цикл зображається замкненою кривою.
Ц икл,
який виконує ідеальний газ, можна розбити
на процеси розширення (І
-2) і
стискання (2-/) газу (рис.81).
икл,
який виконує ідеальний газ, можна розбити
на процеси розширення (І
-2) і
стискання (2-/) газу (рис.81).
Р обота
розширення, яка визначається площею
фігури
обота
розширення, яка визначається площею
фігури
![]() ,
додатна
,
додатна![]() робота стискування, що визначається
площею фігури
робота стискування, що визначається
площею фігури
![]() ,
від'ємна
,
від'ємна![]() Робота, яка виконується газом за цикл
Робота, яка виконується газом за цикл
визначається
заштрихованою площею, що охоплюється
кривою![]()
Якщо
за цикл виконується додатна робота![]() (цикл
виконується за годинниковою стрілкою),
то він називається прямим.
(цикл
виконується за годинниковою стрілкою),
то він називається прямим.
Прямий цикл використовується в тепловому двигуні, в якому робоче тіло отримує енергію у формі теплоти від зовнішніх джерел і частину її віддає у формі роботи. Тепловий двигун складається з трьох частин: нагрівник, робоче тіло, холодильник (рис.).

![]()
Тепловий
двигун характеризується коефіцієнтом
корисної дії![]() ,
який дорівнює відношенню роботи
,
який дорівнює відношенню роботи![]() ,
яка виконана тілом за цикл роботи, до
кількості теплоти
,
яка виконана тілом за цикл роботи, до
кількості теплоти
![]() , що отримало тіло від нагрівника:
, що отримало тіло від нагрівника:
![]()
Зворотний цикл використовується в холодильних машинах - періодично діючих установках, в яких за рахунок роботи зовнішніх сил теплота переноситься до тіла з вищою температурою .
ЦИКЛ КАРНО І ЙОГО КОЕФІЦІЄНТ КОРИСНОЇ ДІЇ ДЛЯ ІДЕАЛЬНОГО ГАЗУ. Карно довів теорему: із всіх періодично діючих теплових машин, що мають однакові температури нагрівачів і холодильників, найбільший ККД мають оборотні машини; при цьому ККД оборотних машин, що працюють при однакових температурах нагрівачів і холодильників, дорівнюють один одному і не залежать від конструкції машини.
Цикл Карно складається з двох ізотерм і двох адіабат (рис.85).

При проходженні адіабатних ділянок циклу система повинна бути термоізольованою від навколишнього середовища.
![]()
Для циклу Карно ККД визначається лише температурами нагрівника і холодильника.
Формула коефіцієнта корисної дії реальної теплової машини має вигляд:
![]()
ДРУГИЙ ЗАКОН ТЕРМОДИНАМІКИ. Другий закон термодинаміки встановлює напрямок перебігу і характер процесів, що відбуваються в природі.
Згідно із Клаузіусом який дав одне з перших формулювань другого закону, теплота ніколи не може переходити сама собою від тіл з нижчою температурою до тіл з вищою температурою.
Фізичний зміст другого закону найбільш зрозуміло розкривається у формулюванні Планка: неможливо побудувати таку періодично діючу теплову машину, яка, отримавши ззовні деяку кількість теплоти при довільній температурі, цілком перетворювала би її в механічну роботу і при цьому поверталась би точно у вихідний стан.
Із формули к.к.д. теплової машини, що працює за циклом Карно,
![]()
випливає,
що
![]() дорівнювала би нулеві лише в тому
випадку, якби температуру робочого тіла
можна було би довести до температури
абсолютного нуля, яку повинен мати
холодильник. К.к.д. реальних теплових
машин завжди менший від одиниці.
дорівнювала би нулеві лише в тому
випадку, якби температуру робочого тіла
можна було би довести до температури
абсолютного нуля, яку повинен мати
холодильник. К.к.д. реальних теплових
машин завжди менший від одиниці.
Вираз для к.к.д. теплової машини, яка працює за циклом Карно, теж є одним з формулювань другого закону: коефіцієнт корисної дії ідеальної теплової машини визначається лише температурами нагрівника і холодильника.
Кельвін сформулював другий закон термодинаміки в такому вигляді: неможливо побудувати теплову машину, яка перетворювала би в роботу теплоту найбільш холодного з тіл, що є в системі.
Такою машиною могла би бути машина, яка перетворювала б в роботу теплоту води в океані. Якби відніманням теплоти і перетворенням її в роботу вдалось би понизити температуру всієї океанської води лише на 0,1 К, то можна було би приводити в рух усі машини і верстати на земній кулі упродовж 1500 років. Така машина була би еквівалентна вічному двигуну, тому її називають вічним двигуном другого роду, на відміну від вічного двигуна першого роду, який повинен створювати роботу з нічого, без затрати енергії.
Вічний двигун першого роду протирічить закону збереження енергії; вічний двигун другого роду не протирічить закону збереження енергії, але він протирічить другому закону термодинаміки.
Другий закон термодинаміки вказує на необоротність процесу перетворення однієї форми передачі енергії - роботи - у другу форму передачі енергії - теплоту
У тепловій машині, що працює за прямим циклом, виконується робота за рахунок підведеної від нагрівника теплоти. Але при цьому частина отриманої теплоти передасться холодильнику. Отже, робота за цикл не еквівалентна до підведеної теплоти.
.
