
Поправка ,
- обусловлена силами притяжения между молекулами.
- имеет размерность давления,
- и ее часто называют внутренним давлением.
Несколько сложнее учесть влияние сил взаимного притяжения молекул, которые очень быстро убывают с увеличением расстояния между молекулами.
Поэтому можно считать, что каждая
молекула взаимодействует лишь с теми
молекулами, которые находятся от нее
на расстояниях
![]() ,
,
где RM— радиус молекулярного действия, имеющий значение порядка 10 -9 м.
Сферу радиуса RM, построенную вокруг молекулы, называют сферой ее молекулярного действия.
Если молекула находится вдали от стенок сосуда, то вся сфера ее молекулярного действия заполнена другими молекулами, так что результирующая сила притяжения для рассматриваемой молекулы равна нулю.
Е
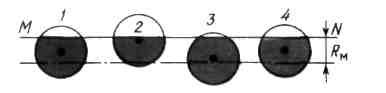 сли
молекулы, находятся вблизи стенки MN
сосуда (рис. 6.3).
сли
молекулы, находятся вблизи стенки MN
сосуда (рис. 6.3).
У них сферы молекулярного действия только частично находятся внутри газа (области, закрашенные на рис. 6.3).
Найдем равнодействующую сил притяжения, приложенных к произвольной молекуле К, находящейся в слое газа, пограничном со стенкой.
Для этого разобьем сферу молекулярного действия молекулы К на четыре области: а, б, г, д (рис. 6.4).
-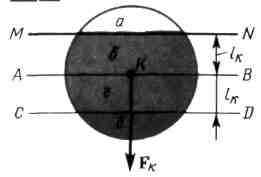 Плоскости АВ и CD
проведены параллельно поверхности
стенки MN,
Плоскости АВ и CD
проведены параллельно поверхности
стенки MN,
- плоскость CD симметрична поверхности стенки относительно диаметральной плоскости АВ.
Области б, г, д заполнены молекулами газа , область а - нет.
Силы, действующие на молекулу К со стороны молекул, находящихся в шаровых слоях
- б, г, взаимно уравновешиваются.
- Притяжение же молекулы К частицами, находящимися в шаровом сегменте д, ничем не компенсируется, так как в сегменте а молекул газа нет .
Очевидно, что результирующая сила Fk должна быть
направлена перпендикулярно стенке внутрь газа (рис. 6.4).
сила пропорциональна концентрации молекул газа:
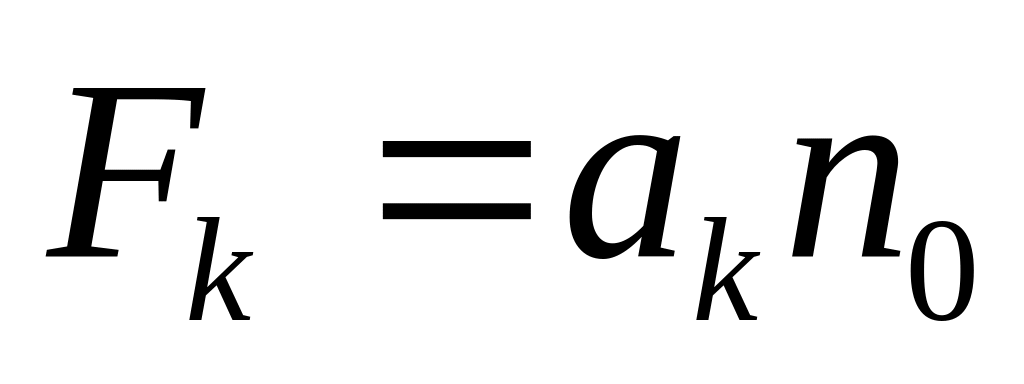 (6.10)
(6.10)
где коэффициент
![]() зависит
зависит
- от химической природы газа ,
- расстояния
![]() от
центра молекулы К до стенки сосуда.
от
центра молекулы К до стенки сосуда.
Если![]() ,
то области а, д исчезают
и Fk
= 0.
,
то области а, д исчезают
и Fk
= 0.
Таким образом, молекулы, отстоящие от стенок сосуда на расстояниях RM и больших, уже можно считать «внутренними».
Действие сил Fk приводит к тому, что в пограничном со стенкой слое газа молекулы
движутся по направлению к стенке замедленно.
ведут себя подобно шарам, которые прикреплены к пружинам и растягивают их в процессе движения за счет убыли своей кинетической энергии.
Поэтому удары молекул о стенки несколько смягчены.
Давление, производимое на стенки реальным газом , меньше , чем в случае идеального газа рид., имеющего ту же температуру Т и ту же концентрацию:
![]() (6.11),
(6.11),
где р*— давление, обусловленное действием сил взаимного притяжения молекул (внутреннее давление).
Внутри газа силы взаимного притяжения молекул не влияют на их движение, и давление газа равно рид.
У стенок оно меньше этого давления и равно р.
Добавочное давление р* производит на газ слой его молекул, граничащих со стенками.
Оно вызвано силами Fk и равно
![]() (6.12)
(6.12)
где сумма сил Fк распространена на все n молекул пограничного слоя газа,
S — площадь стенок сосуда.
Заменив Fk по формуле (6.10), получим
![]() или
или
![]() (6.13),
(6.13),
где![]() -
среднее значение коэффициента
для
всех молекул пограничного
слоя, зависящее только от химической
природы газа.
-
среднее значение коэффициента
для
всех молекул пограничного
слоя, зависящее только от химической
природы газа.
![]() - число молекул, заключенных в
пограничном слое,
- число молекул, заключенных в
пограничном слое,
Подставив это выражение в (6.13), получим
![]() (6.14),
(6.14),
Где
![]() (6.15),
(6.15),
Из уравнений (6.14) и (6.15) имеем
![]() (
6.16),
(
6.16),
Коэффициент
Ван-дер-Ваальса
![]() зависит
только от химической природы газа
зависит
только от химической природы газа
Из (6.16) и (6.11) получим выражение для давления внутри газа:
![]()
где р — давление газа на стенки сосуда.
Подставив в уравнение
Клапейрона — Менделеева
(![]() )
вместо
)
вместо
![]() и рид
вместо р,
получим уравнение состояния реальных
газов, которое было выведено нидерландским
физиком Я. Д- Ван-Дер-Ваальсом (1873) и
названо его именем:
и рид
вместо р,
получим уравнение состояния реальных
газов, которое было выведено нидерландским
физиком Я. Д- Ван-Дер-Ваальсом (1873) и
названо его именем:
В результате уравнение состояния одного моля реального газа приняло вид
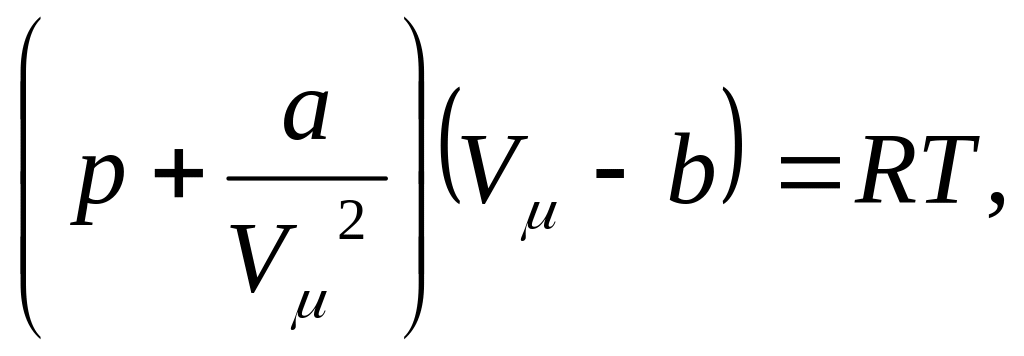 (1) -
уравнение
Ван-дер-Ваальса.
(1) -
уравнение
Ван-дер-Ваальса.
Здесь а и b — постоянные Ван-дер-Ваальса, для разных газов они имеют свои значения.
Если мы имеем дело не с одним, а с
![]() молями газа объемом V, то в уравнении
(1) следует сделать замену:
молями газа объемом V, то в уравнении
(1) следует сделать замену:
![]() .
.
Газ, подчиняющийся уравнению (1), называют ван-дер-ваальсовским.
Уравнение Ван-дер-Ваальса при большой простоте дает возможность качественно объяснить широкий круг явлений в газах и в жидкостях.
Пример: Найдем
давление, при котором плотность
углекислого газа с температурой Т= 300 К
равна
![]() =
500 г/л.
=
500 г/л.
Считая газ ван-дер-ваальсовским, представим (1) в виде
![]() (2)
(2)
Подставив
![]() и
и
![]() ,
получим:
,
получим:
![]() .
.
Для углекислого
газа а = 0,367 Па·м /моль , b
= 4,3·10 м /моль и
![]() = 44 г/моль. В результате подстановки
найдем р
= 44 г/моль. В результате подстановки
найдем р
![]() 80
атм. Расчет же по формуле состояния
идеального газа дает 280 атм. Различие
весьма значительное.
80
атм. Расчет же по формуле состояния
идеального газа дает 280 атм. Различие
весьма значительное.
