
- •Вопросы по дисплине общая химия
- •Постулаты эйнштейна
- •Получение
- •Оксиды Классификация
- •Получение
- •Кислоты
- •Классификация
- •Получение
- •1. Взаимодействие кислотного оксида с водой (для кислородсодержащих кислот):
- •Химические свойства
- •Классификация
- •Средние соли Получение
- •Химические свойства
- •Строение
- •Получение
Химические свойства
1. Термическое разложение.
CaCO3 CaO + CO2
2Cu(NO3)2 2CuO + 4NO2 + O2
NH4Cl NH3 + HCl
2. Гидролиз.
Al2S3 + 6H2O 2Al(OH)3 + 3H2S
FeCl3 + H2O Fe(OH)Cl2 + HCl
Na2S + H2O NaHS +NaOH
3. Обменные реакции с кислотами, основаниями и другими солями.
AgNO3 + HCl AgCl + HNO3
Fe(NO3)3 + 3NaOH Fe(OH)3 + 3NaNO3
CaCl2 + Na2SiO3 CaSiO3 + 2NaCl
4. Окислительно-восстановительные реакции, обусловленные свойствами катиона или аниона.
2KMnO4 + 16HCl 2MnCl2 + 2KCl + 5Cl2 + 8H2O
Кислые соли
Получение
1. Взаимодействие кислоты с недостатком основания.
KOH + H2SO4 KHSO4 + H2O
2. Взаимодействие основания с избытком кислотного оксида
Ca(OH)2 + 2CO2 Ca(HCO3)2
3. Взаимодействие средней соли с кислотой
Ca3(PO4)2 + 4H3PO4 3Ca(H2PO4)2
Химические свойства.
1. Термическое разложение с образованием средней соли
Ca(HCO3)2 CaCO3 + CO2 + H2O
2. Взаимодействие со щёлочью. Получение средней соли.
Ba(HCO3)2 + Ba(OH)2 2BaCO3 + 2H2O
Основные соли
Получение
1. Гидролиз солей, образованных слабым основанием и сильной кислотой
ZnCl2 + H2O [Zn(OH)]Cl + HCl
2. Добавление (по каплям) небольших количеств щелочей к растворам средних солей металлов
AlCl3 + 2NaOH [Al(OH)2]Cl + 2NaCl
3. Взаимодействие солей слабых кислот со средними солями
2MgCl2 + 2Na2CO3 + H2O [Mg(OH)]2CO3 + CO2 + 4NaCl
Химические свойства.
1. Термическое разложение.
[Cu(OH)]2CO3(малахит) 2CuO + CO2 + H2O
2. Взаимодействие с кислотой: образование средней соли.
Sn(OH)Cl + HCl SnCl2 + H2O
Комплексные соли
Строение
K4[Fe(CN)6] |
|
K4[Fe(CN)6] |
– Внешняя сфера |
K4[Fe(CN)6] |
– Внутренняя сфера |
K4[Fe(CN)6] |
– Комплексообразователь (центральный атом) |
K4[Fe(CN)6] |
– Координационное число |
K4[Fe(CN)6] |
– Лиганд |
Центральными атомами обычно служат ионы металлов больших периодов (Co, Ni, Pt, Hg, Ag, Cu); типичными лигандами являются OH-, CN-, NH3, CO, H2O; они связаны с центральным атомом донорно-акцепторной связью
Получение
Реакции солей с лигандами:
AgCl + 2NH3 [Ag(NH3)2]Cl
FeCl3 + 6KCN K3[Fe(CN)6] + 3KCl
Химические свойства.
1. Разрушение комплексов за счёт образования малорастворимых соединений:
2[Cu(NH3)2]Cl + K2S CuS + 2KCl + 4NH3
2. Обмен лигандами между внешней и внутренней сферами.
K2[CoCl4] + 6H2O [Co(H2O)6]Cl2 + 2KCl
Развитие представлении о строени атома.
Понятие атом (греч. «atomos» – неделимый) ввел Демокрит. У Демокрита атомы выступают в роли первоначала. Они неделимы, различаются по величине, весу, форме и находятся в вечном движении. После Демокрита учение об атомах было на много веков забыто. Возродил атомистическую теорию английский физик и химик Джон Дальтон. Он основывался на открытых в то время законах химии и экспериментальных данных о строении вещества. Таким образом, установил, что атомы одного элемента имеют одинаковые свойства, а разных элементов – различаются по свойствам. Дальтон ввел важную характеристику атома – атомную массу и для очень многих элементов были установлены ее относительные значения. В своем атомно-молекулярном учении Дальтон дает характеристику атому: «Атом неделим, вечен и неразрушим».
Модель строения атома Розерфорда.
Модель атома Резерфорда.
Билет №34 Опыты и явления, подтверждающие сложность строения атома. Модель атома Резерфорда. Ответ: В лаборатории Резерфорда были проведены следующие эксперименты. В качестве бомбардирующих частиц взяли тяжелые α–частицы, которые лучше всего подходили для изучения строения атома. Чтобы по возможности точнее исследовать единичные столкновения частиц с атомами мишени, было желательно, чтобы сама мишень была как можно тоньше. К счастью, золотая фольга обладает тем замечательным свойством, что путем расплющивания ее можно сделать исключительно тонкой, толщиной всего лишь в 400 атомов золота. В ранних экспериментах исследовались малые углы рассеяния и было обнаружено, что практически все частицы проходили через мишень, не отклоняясь, как если бы атомы мишени были совершенно прозрачны для бомбардирующих частиц (угол отклонения порядка одного градуса). Модель Резерфорда и рисунок модели Модель Резерфорда. Суть планетарной модели строения атома (Э.Резерфорд, 1911 г.) можно свести к следующим утверждениям: 1. В центре атома находится положительно заряженное ядро, занимающее ничтожную часть пространства внутри атома. 2. Весь положительный заряд и почти вся масса атома сосредоточены в его ядре (масса электрона равна 1/1823 а.е.м.). 3. Вокруг ядра вращаются электроны. Их число равно положительному заряду ядра. Эта модель оказалась очень наглядной и полезной для объяснения многих экспериментальных данных, но она сразу обнаружила и свои недостатки. В частности, электрон, двигаясь вокруг ядра с ускорением (на него действует центростремительная сила), должен был бы, согласно электромагнитной теории, непрерывно излучать энергию. Это привело бы к тому, что электрон должен был бы двигаться вокруг ядра по спирали и в конце концов упасть на него. Никаких доказательств того, что атомы непрерывно исчезают, не было, отсюда следовало, что модель Резерфорда в чемто ошибочна. |
Понятие атома.
Атом – наименьшая частица химического элемента, обуславливающая его свойства. Атом – электронейтральная микросистема состоящая из положительно заряженных ядер и электронных оболочек на еоторых распологаются электроны В ядре сосредочена почти вся масса атома . Ядро состаит протонов и нейтронов (N) связаны с зарядом ядра Z (заряд электрона – -1,602 * 10-19 Кл или 1 а.е.з) и массовым числом А (атомная масса) следующим соотношением
N=A-Z
Атомная единица массы (а.е.м) – величина , точно равная одной двенадцатой части (1/12) массы атома изотопа углерода.
Модель строения атома Бора.
В 1913 г. великий датский физик Нильс Бор применил принцип квантования при решении вопроса о строении атома и характеристике атомных спектров, устранив тем самым противоречия, которые возникали при планетарной модели атома Э. Резерфорда. Модель атома, предложенная Резерфордом в 1911 г., напоминала солнечную систему: в центре находится атомное ядро, а вокруг него но своим орбитам движутся электроны. Ядро имеет положительный заряд, а электроны — отрицательный. Вместо сил тяготения, действующего в Солнечной системе, в атоме действуют электрические силы. Электрический заряд ядра атома, численно равный порядковому номеру в периодической системе Менделеева, уравновешивается суммой зарядов электронов — атом электрически нейтрален. Неразрешимое противоречие этой модели заключалось в том, что электроны, чтобы не потерять устойчивость, должны двигаться вокруг ядра. В то же время они, согласно законам электродинамики, обязательно должны излучать электромагнитную энергию. Но в таком случае электроны очень быстро потеряли бы всю свою энергию и упали на ядро. Следующее противоречие связано с тем, что спектр излучения электрона должен быть непрерывным, так как электрон, приближаясь к ядру, менял бы свою частоту. Опыт же показывает, что атомы излучают свет только определенных частот. Именно поэтому атомные спектры называют линейчатыми. Другими словами, планетарная модель атома Резерфорда оказалась несовместимой с электродинамикой Дж. К. Максвелла. Модель атома Н. Бора, разрешавшая эти противоречия, базировалась на планетарной модели Э. Резерфорда и на разработанной им самим квантовой теории строения атома. Н. Бор выдвинул гипотезу строения атома, основанную на двух постулатах, совершенно несовместимых с классической физикой: 1) в каждом атоме существует несколько стационарных состояний (говоря языком планетарной модели, несколько стационарных орбит) электронов, двигаясь по которым электрон может существовать, не излучая; 2) при переходе электрона из одного стационарного состояния в другое атом излучает или поглощает порцию энергии. Постулаты Бора объясняют устойчивость атомов: находящиеся в стационарных состояниях электроны без внешней на то причины не излучают электромагнитной энергии. Теория атома Н. Бора позволяла дать точное описание атома водорода, состоящего из одного протона и одного электрона трудностями. Чем подробнее теоретики пытались описать движение электронов в атоме, определить их орбиты, тем большим было расхождение теоретических результатов с экспериментальными данными. Как стало ясно в ходе развития квантовой теории, эти расхождения главным образом были связаны с волновыми свойствами электрона. Т. е., следует учитывать, что электрон не точка и не твердый шарик, он обладает внутренней структурой, которая может изменяться в зависимости от его состояния. При этом детали внутренней структуры электрона неизвестны. Следовательно, точно описать структуру атома на основании представления об орбитах точечных электронов принципиально невозможно, поскольку таких орбит в действительности не существует. Вследствие своей волновой природы электроны и их заряды как бы размазаны по атому, однако не равномерно, а таким образом, что в некоторых точках усредненная по времени электронная плотность заряда больше, а в других — меньше. Теория Н. Бора представляет собой как бы пограничную полосу первого этапа развития современной физики. Это последнее усилие описать структуру атома на основе классической физики, дополняя ее лишь небольшим числом новых предположений. Введенные Бором постулаты ясно показали, что классическая физика не в состоянии объяснить даже самые простые опыты, связанные со структурой атома. Постулаты, чужеродные классической физике, нарушили ее цельность, но позволили объяснить лишь небольшой круг экспериментальных данных. Со временем выяснилось, что атомную модель Н. Бора не следует понимать буквально, как это было вначале. Процессы в атоме, в принципе, нельзя наглядно представить в виде механических моделей по аналогии с событиями в макромире. Даже понятия пространства и времени в существующей в макромире форме оказались неподходящими для описания микрофизических явлений. Атом физиков-теоретиков все больше и больше становился абстрактно-ненаблюдаемой суммой уравнений.
Теория планка.
ПЛАНКА ПОСТОЯННАЯ
h, одна из универсальных числовых констант природы, входящая во многие формулы и физические законы, описывающие поведение материи и энергии в масштабах микромира. Существование этой константы было установлено в 1900 профессором физики Берлинского университета М.Планком в работе, заложившей основы квантовой теории. Им же была дана предварительная оценка ее величины. Принятое в настоящее время значение постоянной Планка равно (6,6260755 ± 0,00023)*10 -34 Дж*с. Планк сделал это открытие, пытаясь найти теоретическое объяснение спектра излучения, испускаемого нагретыми телами. Такое излучение испускают все тела, состоящие из большого числа атомов, при любой температуре выше абсолютного нуля, однако оно становится заметным лишь при температурах, близких к температуре кипения воды 100° С и выше нее. Кроме того, оно охватывает весь спектр частот от радиочастотного диапазона до инфракрасной, видимой и ультрафиолетовой областей. В области видимого света излучение становится достаточно ярким лишь примерно при 550° С. Зависимость интенсивности излучения за единицу времени от частоты характеризуется спектральными распределениями, представленными на рис. 1 для нескольких значений температуры. Интенсивность излучения при данном значении частоты есть количество энергии, излучаемой в узкой полосе частот в окрестности данной частоты. Площадь кривой пропорциональна полной энергии, излучаемой на всех частотах. Как нетрудно видеть, эта площадь быстро увеличивается с повышением температуры
Пусталаты Бора.
основные допущения, сформулированные Нильсом Бором в 1913 году для объяснения закономерности линейчатого спектра атома водорода и водородоподобных ионов (формула Бальмера-Ридберга) и квантового характера испускания и поглощения света. Бор исходил из планетарной модели атома Резерфорда.
Электрон в атоме, не теряя энергии, двигается по определённым дискретным круговым орбитам для которых момент импульса квантуется:
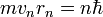 ,
где n —натуральные
числа,
а
,
где n —натуральные
числа,
а 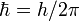 — постоянная
Планка.
Пребывание электрона на орбите определяет
энергию этих стационарных
состояний.
— постоянная
Планка.
Пребывание электрона на орбите определяет
энергию этих стационарных
состояний.При переходе электрона с орбиты (энергетический уровень) на орбиту излучается или поглощается квант энергии hν = En − Em, где En;Em — энергетические уровни, между которыми осуществляется переход. При переходе с верхнего уровня на нижний энергия излучается, при переходе с нижнего на верхний — поглощается.
Используя данные постулаты и законы классической механики, Бор предложил модель атома, ныне именуемую Боровской моделью атома[1]. В дальнейшем Зоммерфельдрасширил теорию Бора на случай эллиптических орбит. Её называют моделью Бора-Зоммерфельда.
Атомные спекры.
оптические
спектры, получающиеся при испускании
или поглощении электромагнитного
излучения свободными или слабо связанными
атомами (например, в газах или
парах). Являются линейчатыми, то есть
состоят из отдельных спектральных
линий, характеризуемых частотой излучения
v, которая соответствует квантовому
переходу между уровнями энергии
Ei и Ek атома
согласно соотношению: hv = Ei-Ek где h-постоянная
Планка. Спектральные линии можно
характеризовать также длиной волны ![]() =
c/v (с - скорость света), волновым числом
=
c/v (с - скорость света), волновым числом ![]() =
v/c и энергией фотона hv. Частоты спектральных
линий выражают в с -1,
длины волн - в нм и мкм, а также в А,
волновые числа - в см -1, энергии фотонов
- в эВ. Типичные атомные спектры наблюдаются
в видимой, УФ- и ближней ИК-областях
спектра. Спектры испускания, или
эмиссионные, получают при возбуждении
атомов различными способами (фотонами,
электронным ударом и т.д.), спектры
поглощения, или абсорбционные, - при
прохождении электромагнитного излучения,
обладающего непрерывным спектром, через
атомарные газы или пары.
Для наблюдения атомных спектров применяют
приборы с фотографической или
фотоэлектрической регистрацией.
Атомные
спектры обладают ярко выраженной
индивидуальностью: каждому элементу
соответствует свой спектр нейтрального
атома (так называемый дуговой спектр)
и свои спектры последовательно
образующихся положительныхионов (так
называемые искровые спектры). Линии в
этих спектрах обозначают римскими
цифрами, например линии FeI, FeII, FeIII в
спектрах железа соответствуют
спектрам Fe, Fe+,
Fe2+.
=
v/c и энергией фотона hv. Частоты спектральных
линий выражают в с -1,
длины волн - в нм и мкм, а также в А,
волновые числа - в см -1, энергии фотонов
- в эВ. Типичные атомные спектры наблюдаются
в видимой, УФ- и ближней ИК-областях
спектра. Спектры испускания, или
эмиссионные, получают при возбуждении
атомов различными способами (фотонами,
электронным ударом и т.д.), спектры
поглощения, или абсорбционные, - при
прохождении электромагнитного излучения,
обладающего непрерывным спектром, через
атомарные газы или пары.
Для наблюдения атомных спектров применяют
приборы с фотографической или
фотоэлектрической регистрацией.
Атомные
спектры обладают ярко выраженной
индивидуальностью: каждому элементу
соответствует свой спектр нейтрального
атома (так называемый дуговой спектр)
и свои спектры последовательно
образующихся положительныхионов (так
называемые искровые спектры). Линии в
этих спектрах обозначают римскими
цифрами, например линии FeI, FeII, FeIII в
спектрах железа соответствуют
спектрам Fe, Fe+,
Fe2+.
Принцып неопределенности (Гейзенберг)
Принцип Гейзенберга вообще играет в квантовой механике ключевую роль хотя бы потому, что достаточно наглядно объясняет, как и почему микромир отличается от знакомого нам материального мира. Чтобы понять этот принцип, задумайтесь для начала о том, что значит «измерить» какую бы то ни было величину. Чтобы отыскать, например, эту книгу, вы, войдя в комнату, окидываете ее взглядом, пока он не остановится на ней. На языке физики это означает, что вы провели визуальное измерение (нашли взглядом книгу) и получили результат — зафиксировали ее пространственные координаты (определили местоположение книги в комнате). На самом деле процесс измерения происходит гораздо сложнее: источник света (Солнце или лампа, например) испускает лучи, которые, пройдя некий путь в пространстве, взаимодействуют с книгой, отражаются от ее поверхности, после чего часть из них доходит до ваших глаз, проходя через хрусталик, фокусируется, попадает на сетчатку — и вы видите образ книги и определяете ее положение в пространстве. Ключ к измерению здесь — взаимодействие между светом и книгой. Так и при любом измерении, представьте себе, инструмент измерения (в данном случае, это свет) вступает во взаимодействие с объектом измерения (в данном случае, это книга)
уравнеие Шреденгера.
Уравне́ние Шрёдингера — уравнение, описывающее изменение в пространстве и во времени чистого состояния, задаваемого волновой функцией, в гамильтоновыхквантовых системах. Играет в квантовой механике такую же важную роль, как уравнение второго закона Ньютона в классической механике. Его можно назвать уравнением движения квантовой частицы. Установлено Эрвином Шрёдингером в 1926 году.
Уравнение Шрёдингера предназначено для частиц без спина, движущихся со скоростями много меньшими скорости света. В случае быстрых частиц и частиц со спином используются его обобщения (уравнение Клейна — Гордона, уравнение Паули, уравнение Дирака и др.)
В начале XX века учёные пришли к выводу, что между предсказаниями классической теории и экспериментальными данными об атомной структуре существует ряд расхождений. Открытие уравнения Шрёдингера последовало за революционным предположением де Бройля, что не только свету, но и вообще любым телам (в том числе и любым микрочастицам) присущи волновые свойства. Исторически окончательной формулировке уравнения Шрёдингера предшествовал длительный период развития физики. Оно является одним из фундаментальных законов физики, объясняющих физические явления. Квантовая теория, однако, не требует полного отказа от законов Ньютона, а лишь определяет границы применимости классической физики. Следовательно, уравнение Шрёдингера должно согласовываться с законами Ньютона в предельном случае. Это подтверждается при более глубоком анализе теории: если размер и масса тела становятся макроскопическими и точность слежения за его координатой много хуже стандартного квантового предела, прогнозы квантовой и классической теорий совпадают, потому что неопределённый путь объекта становится близким к однозначной траектории.
![]()
Квантовые числа (главное, побочное, магнитное , спиновое )
Квантовые числа — энергетические параметры, определяющие состояние электрона и тип атомной орбитали, на которой он находится.
Главное квaнтовое число n определяет общую энергию электрона и степень его удаления от ядра (номер энергетического уровня); оно принимает любые целочисленные значения, начиная с 1 (n = 1, 2, 3, . . .)
Орбитальное (побочное или азимутальное) квантовое число l определяет форму атомной орбитали. Оно может принимать целочисленные значения от 0 доn-1 (l = 0, 1, 2, 3,..., n-1). Каждому значению l соответствует орбиталь особой формы. Орбитали с l = 0 называются s-орбиталями, l = 1 – р-орбиталями (3 типа, отличающихся магнитным квантовым числом m), l = 2 – d-орбиталями (5 типов), l = 3 – f-орбиталями (7 типов).
Магнитное квантовое число m определяет ориентацию орбитали в пространстве относительно внешнего магнитного или электрического поля. Его значения изменяются от +l до -l, включая 0. Например, при l = 1 число m принимает 3 значения: +1, 0, -1, поэтому существуют 3 типа р-АО: рx, рy, рz.
Спиновое квантовое число s может принимать лишь два возможных значения +1/2 и -1/2. Они соответствуют двум возможным и противоположным друг другу направлениям собственного магнитного момента электрона, называемого спином (от англ. веретено). Для обозначения электронов с различными спинами используются символы:
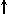 и
и  .
.
многоэлектронные атомы.
Теперь для полноты картины разберемся, как образуются атомы более сложных химических элементов, так называемые многоэлектронные атомы. Более того, мы попробуем проследить их историческое развитие, т.к. именно эта проблема всегда выходила на первый план, когда речь шла о направленной эволюции материи. Проблема изучения исторического развития атомных систем связана с тем, что само возникновение атомов предполагается случайным процессом. По современным представлениям атомы легких элементов образуются при столкновении элементарных частиц, которые могут захватить друг друга, образуя систему нескольких частиц. При столкновении легких атомов они могут объединиться и создать атом более тяжелого элемента. Процесс этот считается случайным, и образование различных атомов носит вероятностный характер. Проследить закономерности в таких процессах крайне сложно, т.к. можно использовать только статистические методы наблюдения.
В нашей концепции образование атомов закономерно и вполне отвечает процессу, который называется эволюцией материи. Эта закономерность следует из всех предшествующих шагов развития пространственной структуры. Рассматривая квантование хронооболочек нашей планеты, мы видели, что в результате была создана голограмма Земли, которую мы назвали интегральной структурой. Мы установили, что интегральная структура Земли задает структуру образующегося физического вакуума.
Причем следом за процессами дифференциации или квантования идут процессы интеграции или объединения. Поэтому программа развития предполагает обратный процесс «свертки» выделенной энергии внутри интегральной структуры, а результатом процесса обратной «свертки» энергии первого уровня реальности является конечный продукт эволюции в виде физического тела планеты.
Историческое развитие атомов начинается с образования структуры физического вакуума. На его основе формируется первый уровень реальности, который мы представили в виде семи подуровней, каждый из которых назвали также вакуумом, но только первого, второго и т.д. рода. Связано это с тем, что при создании материи в первую очередь формируется ее внутреннее пространство, которое, как оказалось в большей степени является пустотой, чем материей.
Первыми начинают создаваться атомы водорода, как структурные элементы нулевого уровня физического вакуума, затем атомы гелия. Появляются они уже сразу, можно сказать, в «готовом виде» в особых точках L=0, L=1, которые являются точками причины. В этом смысле особые точки пространства можно считать «окном» в реальный мир, через который в проявленный мир поступает вещество в виде корпускул водорода и гелия и пространство в виде ū, đ-бозонов. Обладая способностью накапливаться на одном уровне, эти бозоны создают некий структурный барьер вокруг особой точки, не позволяющее разлетаться проявленным атомам, причем đ-бозоны накапливаются на своем уровне, а ū-бозоны накапливаются на собственном уровне. В результате этого образуется потенциальное поле внутри некоторой замкнутой области, которая удерживает внутри себя корпускулярную материю. Основное отличие между этими типами бозонов состоит в том, что одни из них (đ-бозоны) формируют границу внешнего пространства в виде оболочки с антигравитационными свойствами, а другие (ū-бозоны) формируют границу внутреннего пространства в виде поверхности твердого тела, обладающей гравитационными силами.
По мере накопления бозоны начинают оказывать влияние на саму структуру пространственного континуума. И при достижение некоторой критической величины этих бозонов физический вакуум скачком перестраивает свою структуру. Это значит, что в замкнутой области пространства, определяемой границей бозонов, осуществляется фазовый переход, и вакуум становится структурой второго рода. При этом ближайшие области пространства, примыкающие к пространству физического вакуума второго рода, начинают испытывать с его стороны воздействие и также перестраивают свою структуру с нулевого на первый. В результате чего перестраивается не только одна область пространства, но и соседние с ней.
При формировании физического вакуума второго рода основным действующим принципом становится пятый принцип самоорганизации материи, который предполагает многократную дифференциацию любой индивидуальности. В нашем случае индивидуальностями являются кварты пространства, заполненные кварковыми тетрадами, в которых задействованы по два u,d-кварта. Следовательно, пятый принцип допускает возможность многократных дифференциаций u,d-квартов по корпускулярно-волновому принципу.
Теперь каждая образованная кварковая тетрада открывает новый способ творения дифференциальной материи, что определяется в виде интерференции дифференцированных порций энергий. Теперь уже кварковая тетрада в виде матрицы становится неким «окном», через которое поступает энергия в виде потока втекающего в систему времени. Поток времени здесь квантуется на некие порции энергии, которые далее представляют собой две тройки элементарных частиц (протона, нейтрона и пиона) и образующегося пространства в виде бозонов. В этом заключен смысл того, что время само как бы перестраивается в пространство и материю.
Принцып запрета Паули,
Австрийский физик Вольфганг Паули — один из нескольких европейских физиков-теоретиков, сформулировавших в конце 1920-х — начале 1930-х годов основные принципы и постулатыквантовой механики. Принцип, носящий его имя, является одним из основополагающих в этом разделе физической науки. Проще всего представить себе, в чем именно заключается принцип Паули, если сравнить электроны с автомобилями на многоярусной крытой стоянке. В каждый бокс помещается только одна машина, а после того, как все боксы на нижнем этаже стоянки заняты, автомобилям приходится в поисках свободного места заезжать на следующий этаж. Так же и электроны в атомах — на каждой орбите вокруг ядра их помещается не больше, чем там имеется «парковочных мест», а после того, как все места на орбите заняты, следующий электрон ищет себе место на более высокой орбите.
Далее, электроны ведут себя, условно говоря, так, будто они вращаются вокруг своей оси (то есть, обладают собственным моментом вращения, который в этом случае принято называть спиноми который может принимать лишь два значения: +1/2 или –1/2). Два электрона с противоположным спином могут занимать одно место на орбите. Это, как если бы в один бокс помещались одновременно машина с правым рулем и машина с левым рулем, а две машины с одинаковым расположением руля не помещались. Вот почему в первом ряду периодической системы Менделеева мы видим всего два атома (водород и гелий): на нижней орбите отведено всего одно сдвоенное место для электронов с противоположным спином. На следующей орбите помещается уже восемь электронов (четыре со спином –1/2, и четыре со спином +1/2), поэтому во втором ряду таблицы Менделеева мы видим уже восемь элементов. И так далее.
Внутри стареющих звезд температура настолько высока, что атомы в основном находятся в ионизированном состоянии, и электроны свободно перемещаются между ядрами. И здесь снова срабатывает принцип запрета Паули, но уже в видоизмененной форме. Теперь он гласит, что в определенном пространственном объеме может одновременно находиться не более двух электронов с противоположным спином и определенными интервалами предельно допустимых скоростей. Однако картина резко изменяется после того, как плотность вещества внутри звезды превысит пороговое значение порядка 107 кг/м3 (для сравнения — это в 10 000 раз выше плотности воды; спичечный коробок такого вещества весит около 100 тонн). При такой плотности принцип Паули начинает выражаться в стремительном росте внутреннего давления в звезде. Это дополнительное давление вырожденного электронного газа, и его проявлением становится тот факт, что гравитационный коллапс старой звезды останавливается после того, как она сжимается до размеров, сопоставимых с размерами Земли. Такие звезды называют белыми карликами, и это последняя стадия эволюции звезд с массой, близкой к массе Солнца (см. Предел Чандрасекара).
Выше я описал действие запрета Паули применительно к электронам, но он действует и в отношении любых элементарных частиц с полуцелым спиновым числом (1/2, 3/2, 5/2 и т. д.). В частности, спиновое число нейтрона равно, как и у электрона, 1/2. Это значит, что нейтронам, как и электронам, требуется определенное «жизненное пространство» вокруг себя. Если масса белого карлика превышает 1,4 массы Солнца (см. Предел Чандрасекара), силы гравитационного притяжения заставляют протоны и электроны внутри звезды попарно объединяться в нейтроны. Но тогда нейтроны, подобно электронам в белых карликах, начинают производить внутренне давление, которое называется давлением вырожденного нейтронного газа, и в этом случае гравитационный коллапс звезды останавливается на стадии образования нейтронной звезды, диаметр которой сопоставим с размерами большого города. Однако при еще большей массе звезды (начиная примерно с тридцатикратной массы Солнца) силы гравитации сламывают и сопротивление вырожденного нейтронного газа, и звезды коллапсируют дальше, превращаясь в черные дыры.
Принцип запрета Паули представляет собой яркий пример закона природы нового типа, и по мере развития компьютерных технологий такие «неявные» законы будут неизбежно играть всё большую роль. Законы этого типа принципиально отличаются от законов классической физики, таких какзаконы механики Ньютона, — они не предсказывают, что произойдет в системе. Вместо этого они определяют, чего в системе не может произойти. Именно их биолог и структурный теоретик Харольд Моровиц (Harold Morowitz, р. 1927) назвал «правилами отсечения»: такие правила, в частности, принцип запрета Паули сводятся к тому, что при решении самых сложных и комплексных проблем (а расчет орбит электронов в сложных атомов к таковым, несомненно, относится) следует запрограммировать компьютер таким образом, чтобы он даже не рассматривалзаведомо невозможные варианты решения. Тем самым такое правило отсекает от ствола возможных решений задачи заведомо мертвые ветви, оставляя лишь допустимые возможности для ее решения, благодаря чему время компьютерных расчетов сокращается до разумных пределов. Таким образом, правила, подобные принципу запрета Паули, становятся всё более важными, поскольку мы всё больше зависим от компьютеров в решении самых сложных и комплексных проблем.
Правило Гунда(хунда)
приближенные правила, определяющие относит. расположение энергетич. уровней атома. Получены Ф. Хундом в 1927 в результате анализа атомных спектров. Формулировка X. п. предполагает, что состояние многоэлектронного атома можно описать, указав т. наз. электронную конфигурацию - набор тех состояний, в к-рых находятся отдельные электроны. В общем случае данной электронной конфигурации отвечает неск. разных энергетич. состояний атома. Каждое из них в силу сферич. симметрии атома можно классифицировать по суммарному орбитальному моменту (квантовое число L = 0, 1, 2, ... отвечает соотв. состояниям S, Р, D-типов), суммарному спину (квантовое число S) и полному моменту импульса атома как целого (квантовое число J, к-рое при заданных L и S меняется от L + S до |L - S | с шагом 1). Напр., атом С в низших состояниях можно описать электронной конфигурацией Is22s22p2; общее число состояний, отвечающих такой конфигурации, с учетом вырожденности нек-рых уровней равно 15. При стандартном обозначении символом 2S+lLj состояния атома С - 1S0,3P0,3Р1, 3Р2, 1D2. Наиб. распространены след. X. п.: 1. Из состояний атома с заданной электронной конфигурацией ниже по энергии те, к-рые отвечают большим значениям S. 2. Из состояния атома с заданной конфигурацией и заданным спином S ниже по энергии те, к-рые отвечают большему значению L. С X. п. тесно связан важный для теории мол. орбиталей принцип заполнения: из неск. конфигураций молекулы ниже по энергии те, для к-рых сумма значений орбитальных энергий атомов меньше. X. п. ограничены в осн. низколежащими состояниями атомов при условии, что влияние электронной корреляции (взаимной обусловленности движений электронов) достаточно мало и не нарушает границ применимости одноконфигурационного приближения (см. Конфигурационного взаимодействия метод ). Основанием для выполнения первого правила является тесная связь между симметрией пространств. части волнoвой ф-ции атома и симметрией ее спиновой части, существующая согласно Паули принципу . По этой же причине первое X. п. обычно выполняется и для молекул. Второе X. п. имеет более ограниченную применимость и определяется в осн. тем, насколько значимо межэлектронное отталкивание в анализируемых состояниях. Это правило выполняется иногда и для линейных молекул (при замене L на модуль проекции момента кол-ва движения на ось молекулы). Для нек-рых типов состояний удается найти дополнит. правила, отвечающие изменению энергии атома при данной конфигурации и данных L и S в зависимости от J. Эти правила связаны со спин-орбитальным взаимодействием и др. тонкими эффектами. Напр., если в конфигурации есть лишь одна частично заполненная оболочка, то при заполнении оболочки менее чем на половину ("нормальный мультиплет") энергия растет с повышением J. В остальных случаях с ростом J энергия убывает ("обращенный мультиплет"). Так, для атома С описанные правила подтверждаются эксперим. значениями энергий возбуждения из основного состояния 3Р0: энергия перехода в, состояние 3Р1 равна 0,2 кДж/моль, в состояния 3Р2 - 0,5, 1D2 - 121,9, 1S0 - 259,0 кДж/моль. X. п. часто нарушаются, т. к. одноконфигурационные модели атомов и молекул довольно редко бывают надежны. С появлением прецизионных эксперим. данных о спектрах атомов они теряют свое значение. Лит.: Собельман И. И., Введение в теорию атомных спектров, М., 1977; Абаренков И.В., Братцев В. Ф., Тулуб А. В., Начала квантовой химии, М., 1989. В. И. Пупышев.
правило кличевского принцып наименьшй энерги.
В атоме каждый электрон располагается так, чтобы его энергия была минимальной (что отвечает наибольшей связи его с ядром).
Энергия электрона в основном определяется главным квантовым числом n и побочным квантовым числом l, поэтому сначала заполняются те подуровни, для которых сумма значений квантовых чисел n и l является наименьшей. Например, энергия электрона на подуровне 4s меньше, чем на подуровне 3d, так как в первом случае n + 1 = 4 + 0 = 4, а во втором n + l = 3 + 2 =5; на подуровне 5s (n + l = 5 + 0 = 5) энергия меньше, чем на 4d (n + l = 4 + 2 = 6); на 5р (n + l = 5 + 1 = 6) энергия меньше, чем на 4f (n + l = 4 + 3 = 7) и т.д.
В.М. Клечковский впервые в 1961 г. сформулировал общее положение, гласящее, что электрон занимает в основном состоянии уровень не с минимальным возможным значением n, а с наименьшим значением суммы n + l.
В том случае, когда для двух подуровней суммы значений n и l равны, сначала идет заполнение подуровня с меньшим значением n. Например, на подуровнях Зd, 4р, 5s сумма значений n и l равна 5. В этом случае происходит сначала заполнение подуровней с меньшими значениями n, т.е. Зd - 4р – 5s и т.д. В периодической системе элементов Менделеева последовательность заполнения электронами уровней и подуровней выглядит следующим образом
Современная формулировка Периодического закона .
Формулировка периодического закона, данная Д.И. Менделеевым, гласила: свойства химических элементов находятся в периодической зависимости от атомных масс этих элементов. Современная формулировка гласит: свойства химических элементов находятся в периодической зависимости от заряда ядра этих элементов. Такое уточнение потребовалось, поскольку к моменту установления Менделеевым периодического закона еще не было известно о строении атома. После выяснения строения атома и установления закономерностей размещения электронов по электронным уровням стало ясно, что периодическая повторяемость свойств элементов связана с повторяемостью строения электронных оболочек.
структура периодической таблицы Период группы , подгруппы семейства элементов .
Периоди́ческая систе́ма хими́ческих элеме́нтов (табли́ца Менделе́ева) — классификация химических элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. Система является графическим выражением периодического закона, установленного русским химиком Д. И. Менделеевым в 1869 году. Её первоначальный вариант был разработан Д. И. Менделеевым в 1869—1871 годах и устанавливал зависимость свойств элементов от их атомного веса (по-современному, от атомной массы). Всего предложено несколько сотен[1] вариантов изображения периодической системы (аналитических кривых, таблиц, геометрических фигур и т. п.). В современном варианте системы предполагается сведение элементов в двумерную таблицу, в которой каждый столбец (группа) определяет основные физико-химические свойства, а строки представляют собой периоды, в определённой мере подобные друг другу.
Своиства химических элементов.
Энергия ионизации
равна работе, затрачиваемой на удаление одного внеш. эл-на из атома (на ионизацию атома), находящегося в осн. энергетич. состоянии. Численно равна ионизационному потенциалу.- минимальная энергия, необходимая для отрыва электрона (ионизации) от атома, иона или молекулы, находящихся в основном энергетич. состоянии. Для нейтральных атомов Э. и. изменяется от 3,89 эВ (Cs) до 24,6 эВ (Не). Э. и. положит. ионов пропорциональна квадрату спектроскопического символа иона. Э. и. от-рицат. ионов характеризует сродство к электрону и изменяется в пределах от 0,03 до 3,5 эВ. Мин. энергия, к-рую необходимо затратить для удаления одного электрона с поверхности жидкости или твёрдого тела, наз. работой выхода. В. П. Шевелько.
сродство к электрону
способность нек-рых нейтральных атомов, молекул и свободных радикалов присоединять добавочные эл-ны, превращаясь в отрицат. ионы. Мерой этой способности служит положит. энергия С. к э. c, равная разности энергии нейтрального атома (молекулы) в основном состоянии и энергии осн. состояния отрицат. иона, образовавшегося после присоединения эл-на.
У большинства атомов С. к э. связано с тем, что их внеш. электронные оболочки не заполнены (см. АТОМ). Таковы атомы Н и элементов 1-й группы периодической системы элементов (имеющие лишь 1 внеш. s-эл-н), а также атомы элементов 3—7-й групп (неполное число р-эл-нов). Атомы с двумя внеш. s-эл-нами, как правило, не обладают С. к э. (щелочноземельные элементы, Hg и др.). Захват добавочного эл-на атомами Fe, Co и Ni, у к-рых в норм. состоянии тоже 2 внеш. s-эл-на, приводит, как принято считать, к заполнению свободного места на внутр. оболочке 3d.
Величина c точно определена лишь для немногих атомов (данные о c молекул и радикалов б. ч. недостаточно надёжны). Прямо измерить c атомов можно, напр., определив длину волны света l0, соответствующую т. н. порогу фотоотщепления (фотоотрыва) эл-на от отрицат. иона: c=hс/l0 (с — скорость света в вакууме). Этим методом были установлены величины c атомов С, О, S, I, Сl. Типичные значения c атомов (в эВ): Н — 0,754; С — 1,2; О - 1,46; S — 2,07—2,33; F — 3,40—3,62; Сl — 3,82; I — 3,08—3,23. Величины ОС молекул и радикалов колеблются в широких пределах. В ряде случаев они составляют доли эВ, но для NO2 c>3 эВ, для ОН c»2 эВ, для CN c>3 эВ.
- свойство атомов или молекул образовыватьпрочную связь с электроном, т. е. отрицательный ион. Характеристикойтакой связи является энергия сродства атомов или молекул к электрону -энергия связи электрона в соответствующем отрицат. ионе, к-рая обычнообозначается ЕА (electron affinity). Эта энергия равна разности энергиинейтрального атома (молекулы) в основном состоянии и энергии осн. <состояния образовавшегося отрицат. иона. У большинства атомов С. к э. связанос тем, что их внеш. электронные оболочки не заполнены (см. Атом). Втабл. приводятся значения энергии С. к э. атомов в осн. состоянии. Осн. <и наиб. точная часть этой информации получена при исследовании фотораспадаотрицат. ионов. В одном варианте этого метода отрицат. ионы разрушаютсяпод действием лазерного излучения данной длины волны, энергия связи электронаустанавливается по измерениям энергии освободившихся электронов. В др. <варианте данного метода для фоторазрушения отрицат. ионов используетсяизлучение перестраиваемого лазера, что позволяет определить положение порогафотораспада отрицат. иона, а по нему и энергию связи электрона. Фотоэлектронныйи лазерный методы определения энергии связи электрона в отрицат. ионе являютсяглавными и при исследовании молекулярных отрицат. ионов. В табл. указанкласс точности определения энергии С. к э.: О означает точность лучше 0,1%,1 -лучше 1%; 2 - лучше 3%; 3 - выше 10%; 4 - хуже 10%. Отрицат. ион Непостроен на метастабильном атоме Не. «Нет» в табл. означает, что стабильныйотрицат. ион данного элемента не образуется.
электроотрицательность
Только о небольшой части всех химических связей можно сказать, что они являются чисто ковалентными. В таких соединениях поделенная пара электронов всегда находится на одинаковом расстоянии от ядер обоих атомов. Это возможно тогда, когда между собой связаны одинаковые атомы. Например, из рассмотренных нами в этой главе молекул чисто ковалентными окажутся двухатомные молекулы водорода, кислорода, хлора, азота:
![]()
Когда между собой связываются разные атомы, поделенная пара химической связи всегда смещена к одному из атомов. К какому? Разумеется, к тому атому, который проявляет более сильные акцепторные свойства.
Допустим, при образовании двухатомной молекулы АБ электроны связи смещаются в сторону атома Б. В этом случае атом Б считается более электроотрицательным, чем атом А. С помощью формул Льюиса можно изобразить смещение пары электронов следующим образом:

Под электроотрицательностью (ЭО) понимают относительную способность атомов притягивать электроны при связывании с другими атомами. Электроотрицательность характеризует способность атома к поляризации химических связей.
атомные и ионные радиусы
А́ТОМНЫЕ РА́ДИУСЫ, характеристики, позволяющие приближенно оценивать межатомные (межъядерные) расстояния в молекулах и кристаллах. Под эффективным радиусом атома или иона понимается радиус сферы его действия, причем атом (ион) считается несжимаемым шаром. Используя планетарную модель атома, его представляют как ядро, вокруг которого по орбиталям (см. ОРБИТАЛИ)вращаются электроны. Последовательность элементов в Периодической системе Менделеева соответствует последовательности заполнения электронных оболочек. Эффективный радиус иона зависит от заполненности электронных оболочек, но он не равен радиусу наружной орбиты. Для определения эффективного радиуса представляют атомы (ионы) в структуре кристалла как соприкасающиеся жесткие шары, так что расстояние между их центрами равно сумме радиусов. Атомные и ионные радиусы определены экспериментально по рентгеновским измерениям межатомных расстояний и вычислены теоретически на основе квантово-механических представлений. Размеры ионных радиусов подчиняются следующим закономерностям: 1. Внутри одного вертикального ряда периодической системы радиусы ионов с одинаковым зарядом увеличиваются с возрастанием атомного номера, поскольку растет число электронных оболочек, а значит, и размер атома. 2. Для одного и того же элемента ионный радиус возрастает с увеличением отрицательного заряда и уменьшается с увеличением положительного заряда. Радиус аниона больше радиуса катиона, поскольку у аниона имеется избыток электронов, а у катиона – недостаток. Например, у Fe, Fe2+, Fe3+ эффективный радиус равен 0,126, 0,080 и 0,067 нм соответственно, у Si4-, Si, Si4+эффективный радиус равен 0,198, 0,118 и 0,040 нм. 3. Размеры атомов и ионов следуют периодичности системы Менделеева; исключения составляют элементы от № 57 (лантан) до №71 (лютеций), где радиусы атомов не увеличиваются, а равномерно уменьшаются (так называемое лантаноидное сжатие), и элементы от № 89 (актиний) и дальше (так называемое актиноидное сжатие). Атомный радиус химического элемента зависит от координационного числа (см. КООРДИНАЦИОННОЕ ЧИСЛО). Увеличение координационного числа всегда сопровождается увеличением межатомных расстояний. При этом относительная разность значений атомных радиусов, соответствующих двум разным координационным числам, не зависит от типа химической связи (при условии, что тип связи в структурах со сравниваемыми координационными числами одинаков). Изменение атомных радиусов с изменением координационного числа существенно сказывается на величине объемных изменений при полиморфных превращениях. Например, при охлаждении железа, его превращение из модификации с гранецентрированной кубической решеткой в модификацию с объемно-центрированной кубической решеткой имеющее место при 906 оС, должно сопровождаться увеличением объема на 9%, в действительности увеличение объема составляет 0,8%. Это связано с тем, что за счет изменения координационного числа от 12 до 8 атомный радиус железа уменьшается на 3%. Т. е., изменение атомных радиусов при полиморфных превращениях в значительной степени компенсируют те объемные изменения, которые должны были бы произойти, если бы при этом не менялся атомный радиус. Атомные радиусы элементов можно сопоставлять только при одинаковом координационном числе. Атомные (ионные) радиусы зависят также от типа химической связи. В кристаллах с металлической связью (см. МЕТАЛЛИЧЕСКАЯ СВЯЗЬ) атомный радиус определяется как половина межатомного расстояния между ближайшими атомами. В случае твердых растворов (см. ТВЕРДЫЕ РАСТВОРЫ) металлические атомные радиусы меняются сложным образом. Под ковалентными радиусами элементов с ковалентной связью понимают половину межатомного расстояния между ближайшими атомами, соединенными единичной ковалентной связью. Особенностью ковалентных радиусов является их постоянство в разных ковалентных структурах с одинаковыми координационными числами. Так, расстояния в одинарных связях С-С в алмазе и насыщенных углеводородах одинаковы и равны 0,154 нм. Ионные радиусы в веществах с ионной связью (см. ИОННАЯ СВЯЗЬ) не могут быть определены как полусумма расстояний между ближайшими ионами. Как правило, размеры катионов и анионов резко различаются. Кроме того, симметрия ионов отличается от сферической. Существует несколько подходов к оценке величины ионных радиусов. На основании этих подходов оценивают ионные радиусы элементов, а затем из экспериментально определенных межатомных расстояний определяют ионные радиусы других элементов. Ван-дер-ваальсовы радиусы определяют эффективные размеры атомов благородных газов. Кроме того, ван-дер-ваальсовыми атомными радиусами считают половину межъядерного расстояния между ближайшими одинаковыми атомами, не связанными между собой химической связью, т.е. принадлежащими разным молекулам (например, в молекулярных кристаллах). При использовании в расчетах и построениях величин атомных (ионных) радиусов их значения следует брать из таблиц, построенных по одной системе.
Понятие химической связи.
Под химической связью понимают результат взаимодействия атомов приводящее к образованию устойчивой молекулы. По современным представлениям химическая связь имеет электростатическое происхождение. В ее образовании принимает участие электроны внешнего энергетического уровня. Между электронами и ядрами взаимодействующих атомов возникают силы электростатического притяжения, которые удерживают атомы в виде молекулы. Обычно выделяют три типа химических связей: ковалентная, ионная, металлическая.
По своей сути ковалентная химическая связь является универсальной. Ионная связь можно рассматривать как предельный случай ковалентной полярной связи. Металлическая связь расценивается как разновидность ковалентной связи свойственной для металлов, т.к. механизм одинаков, но отличается некоторыми особенностями.
