
- •Механика
- •Молекулярная физика
- •Равномерное движение
- •Равномерное прямолинейное движение
- •1.5.3. Движение по произвольной траектории с постоянной тангенциальной составляющей вектора ускорения aτ.
- •Равноускоренное движение с изменяющейся тангенциальной составляющей ускорения
- •Прямолинейное равноускоренное движение
- •Виды движения твердого тела
- •4. Виды сил в механике. Силы упругости (закон Гука), трения, сопротивления среды. Сила тяжести и вес.
- •Замкнутая система тел. Закон сохранения импульса. Центр инерции механической системы и закон его движения. Движение тела переменной массы.
- •6.Законы Ньютона в неинерциальных системах отсчета. Силы инерции. Центробежная сила инерции, и ее влияние на вес тела на Земле. Сила Кориолиса. Принцип эквивалентности Эйнштейна.
- •Работа в механике. Работа постоянной и переменной сил. Графическое представление работы. Мощность.
- •8.Механическая энергия и ее виды. Кинетическая энергия и работа равнодействующей силы. Закон сохранения механической энергии.
- •Столкновение тел. Удар. Законы сохранения импульса и энергии при упругом и неупругом ударах. Вычисление скоростей соударяющихся тел. Потери механической энергии при неупругом ударе.
- •1 1.Момент инерции материальной точки и твердого тела. Вычисление момента инерции однородного диска. Теорема Штейнера. Свободные и главные оси вращения. Основной закон динамики вращательного движения.
- •Момент силы относительно точки и оси. Момент пары сил. Основной закон динамики вращательного движения.
- •Работа, совершаемая при вращении тела. Кинетическая энергия вращения. Сравнительный расчет скоростей центра масс шара и диска, скатывающихся с наклонной плоскости.
- •15. Колебательное движение. Виды колебаний. Гармонические колебания. Их уравнение, график, характеристики. Скорость, ускорение и энергия при гармонических колебаниях.
- •17.Затухающие колебания. Их уравнение, график и основные характеристики.
- •Вынужденные колебания. Резонанс.
- •Внешняя сила
- •Квазиупругая сила
- •Маятники. Уравнение движения физического маятника. Математический маятник. Приведенная длина физического маятника.
- •20.Волновой процесс, основное свойство волн. Упругие волны. Волновая поверхность и волновой фронт. Продольные и поперечные волны. Уравнение плоской и сферической бегущих волн. Волновое уравнение.
- •2 1.Уравнение плоской бегущей волны. Перенос энергии волной. Вектор Умова. Интенсивность волны. Затухающие волны.
- •22. Интерференция плоских волн. Стоячие волны. Расчет координат узлов и пучностей. Колебания струны
- •23. Суперпозиция волн близкой частоты. Волновой пакет. Групповая скорость волн. Дисперсия волн.
- •24. Звуковые волны. Эффект Доплера в акустике.
- •1 Моль — это количество вещества, в котором содержится столько же атомов, сколько их в 12 г углерода .
- •6. Адиабатический процесс. Первое начало термодинамики для адиабатического процесса. Политропные процессы.
- •Работа газа при изменении объема. Расчет работы, совершаемой газом в различных изопроцессах.
- •Работа моля газа при нагревании на 1 к
- •Столкновения молекул. Эффективный диаметр молекул, средняя длина свободного пробега.
- •10.Круговые процессы (циклы). Работа в круговом процессе. Тепловые и холодильные машины. Цикл Карно.
- •11.Явления переноса в термодинамически неравновесных системах. Вычисление коэффициентов теплопроводности, диффузии и внутреннего трения.
- •12.Взаимодействие молекул. Реальные газы. Уравнение Ван-дер-Ваальса. Изотермы Ван-дер-Ваальса и их анализ. Внутренняя энергия реального газа.
- •13. Поверхностное натяжение жидкостей. Давление под искривленной поверхностью. Смачивание. Капиллярные явления.
- •14. Ламинарное и турбулентное течение жидкости. Уравнение неразрывности струи. Уравнение Бернулли. Внутреннее трение. Движение тел в жидкостях и газах.
- •Твердые тела. Типы кристаллических твердых тел. Фазовые переходы в твердых телах. Диаграмма состояния. Тройная точка.
1 Моль — это количество вещества, в котором содержится столько же атомов, сколько их в 12 г углерода .
Количество атомов в 1 моле равно числу
Авогадро: ![]()
М![]()
![]() олярная
масса М - это
масса одного моля вещества в граммах.
олярная
масса М - это
масса одного моля вещества в граммах.
Молярная масса равна выраженной в граммах относительной атомной массе
Состояние характеризуется набором ТД-параметров.
Если все параметры имеют определенные значения, состояние равновесное.
Процесс сопровождается изменением ТД-параметров.
Равновесный процесс – это медленный переход между равновесными состояниями.
Если какой-то параметр не изменяется, то процесс называют изопроцессом.
Идеальный газ
Размеры молекул пренебрежи-мо малы;
Молекулы не взаимодействуют;
Столкновения – упругие.
Экспериментальные газовые законы
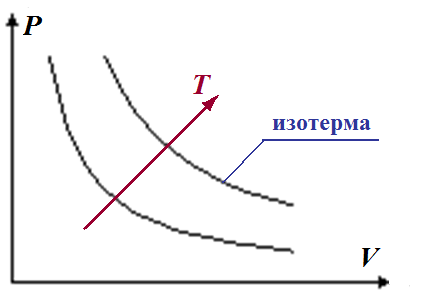
З![]() акон
Бойля-Мариотта для изотермического
процесса. T =
const.
акон
Бойля-Мариотта для изотермического
процесса. T =
const.
![]()
З![]() акон
Шарля для изохорного процесса.
акон
Шарля для изохорного процесса.
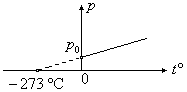
![]()
![]()
![]()
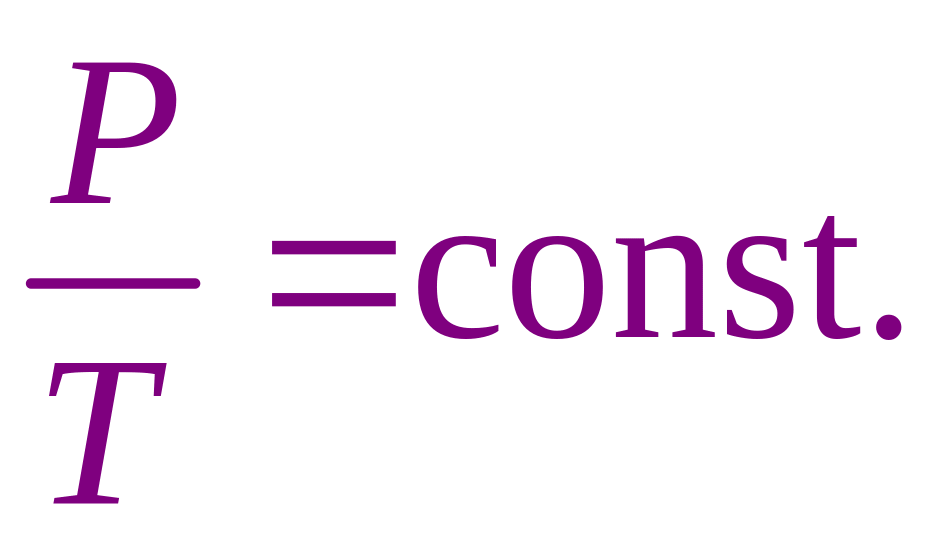
![]()
З![]()
![]() акон
Гей-Люссака для изобарного
процесса.
акон
Гей-Люссака для изобарного
процесса.
З![]()
![]() акон
Авогадро 1 киломоль любого газа
занимает при одинаковых условиях
одинаковый объем.
акон
Авогадро 1 киломоль любого газа
занимает при одинаковых условиях
одинаковый объем.
З![]() акон
Дальтона Давление смеси газов равно
сумме парциальных давлений
акон
Дальтона Давление смеси газов равно
сумме парциальных давлений
п![]() арциальные
давления (каждого газа в отдельности)
арциальные
давления (каждого газа в отдельности)
![]()

У![]() равнение
Менделеева-Клайперона
равнение
Менделеева-Клайперона
![]()
Основное уравнение МКТ
![]()
2. Число степеней свободы механической системы и молекулы газа. Распределение энергии по степеням свободы. Средняя энергия многоатомной молекулы. Внутренняя энергия идеального газа.
Число степеней свободы это число независимых координат, которые необходимо задать для определения положения тела в пространстве



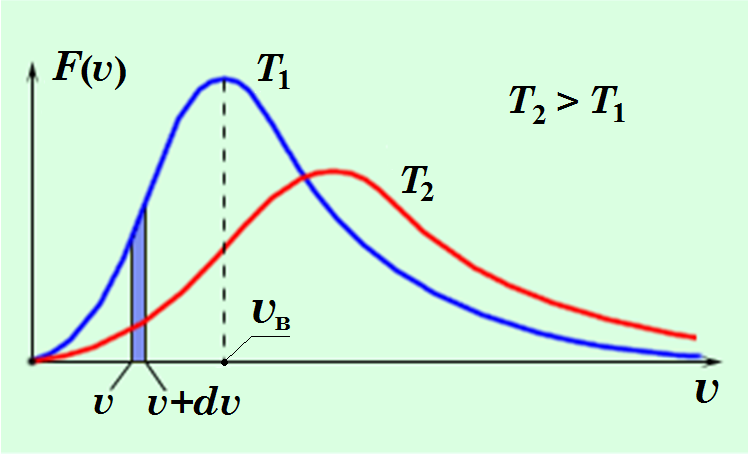
3.Распределение Максвелла скоростей и кинетических энергий молекул. Вероятностный характер законов распределения. Наиболее вероятная, среднеарифметическая и среднеквадратичная скорости молекул. Экспериментальная проверка распределения Максвелла.
Распределение Максвелла - У всех молекул разные скорости. При столкновениях эти скорости изменяются.
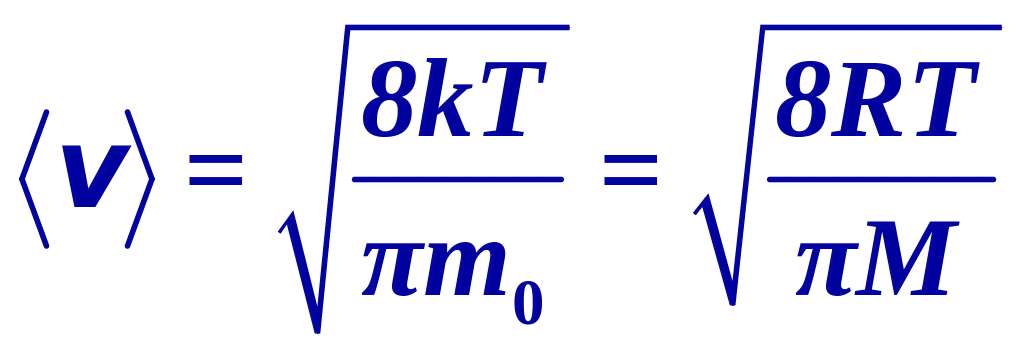
![]()
Средняя скорость молекул
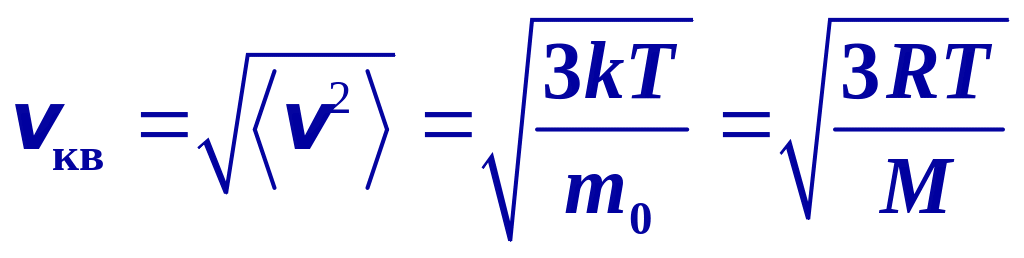
Среднеквадратичная скорость молекул
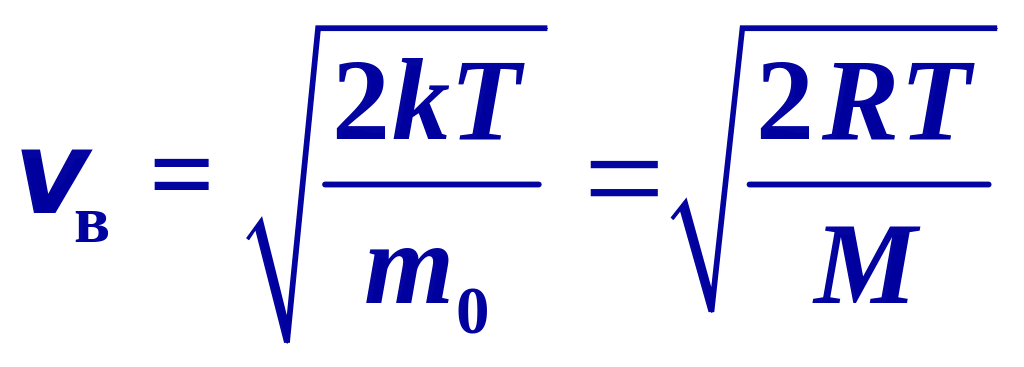
4![]() .
Распределение Больцмана молекул в
потенциальном поле сил. Изменение
концентрации молекул с высотой.
Барометрическая формула.
.
Распределение Больцмана молекул в
потенциальном поле сил. Изменение
концентрации молекул с высотой.
Барометрическая формула.
Распределение Больцмана
![]()
Изменение концентрации с высотой
![]()
Барометрическая формула показывает как давление меняется с высотой
5. Теплоемкость. Первое начало термодинамики и его применение для расчета отношения молярных теплоемкостей СP/CV.
Т еплоемкость
тела - это количество теплоты,
необходимое для нагревания тела на 1 К.
еплоемкость
тела - это количество теплоты,
необходимое для нагревания тела на 1 К.
![]()
Молярная теплоемкость – это количество теплоты, необходимое для нагревания одного моля вещества на 1 К.
![]()
![]()
![]()
Первое начало термодинамики
К
![]() оличество
теплоты, сообщенное системе, идет на
увеличение внутренней энергии системы
и на совершение системой работы над
внешними телами.
оличество
теплоты, сообщенное системе, идет на
увеличение внутренней энергии системы
и на совершение системой работы над
внешними телами.
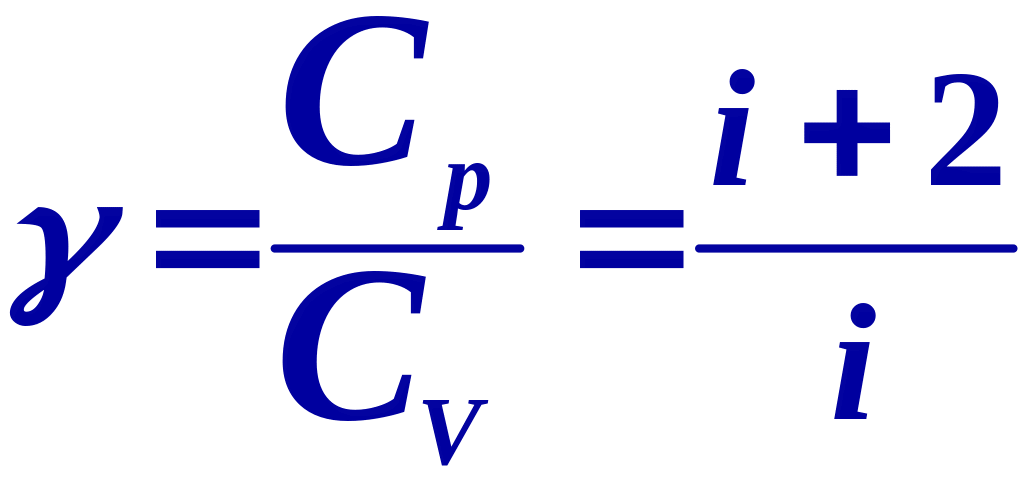
Коэффициент Пуассона
![]()
![]()
