
- •1. Кинематика материальной точки. Система отсчета. Траектория, перемещение, скорость, ускорение. Равномерное и равнопеременное прямолинейное движение.
- •2. Криволинейное движение. Нормальное и тангенсальное ускорения.
- •3. Движение точки по окружности. Угловые перемещение, ускорение, скорость. Связь между линейными и угловыми характеристиками.
- •4. Динамика материальной точки. Инерциальные системы отсчета и первый закон Ньютона.
- •5. Фундаментальные взаимодействия. Силы различной природы(упругие, гравитационные, трения). Второй закон Ньютона. Масса. Третий закон Ньютона.
- •6. Импульс системы материальных точек. Уравнение движения центра масс. Закон сохранения импульса.
- •7. Уравнение движения тела переменной массы ( уравнение Мещерского).
- •8. Момент импульса и момент силы. Уравнение моментов. Закон сохранения момента импульса. Гироскопические явления.
- •9. Вращение твердого тела вокруг неподвижной оси. Основной закон динамики вращательного движения абсолютно твердого тела. Момент инерции.
- •10. Расчет момента инерции тел простой формы. Теорема Штейнера.
- •11. Кинетическая энергия материальной точки и абсолютно твердого тела.
- •12. Работа переменной силы, мощность. Потенциальные и непотенциальные поля. Консервативные и диссипативные силы. Потенциальная энергия.
- •13. Закон всемирного тяготения. Поле тяготения, его напряженность и потенциальная энергия гравитационного взаимодействия.
- •14. Работа по перемещения тела в поле тяготения. Космические скорости.
- •15. Соударения тел. Упругое и неупругое взаимодействия.
- •16. Колебательное движение и его характеристики: смещение, амплитуда, фаза, циклическая частота, период, скорость, ускорение.
- •17. Векторные диаграммы для представления гармонических колебаний. Дифференциальное уравнение гармонических колебаний. Энергия колебательного движения.
- •18. Пружинный и физический маятники.
- •19. Сложение параллельных колебаний одинаковой и разной частоты. Биения. Сложения колебаний одинаковой частоты
- •Сложение колебаний разной частоты
- •20. Сложение взаимно перпендикулярных колебаний. Фигуры Лиссажу.
- •21. Свободные затухающие колебания. Характеристики затухания: коэффициент затухания, время релаксации, декремент затухания, добротность колебательной системы.
- •22 Вынужденные колебания. Резонанс.
- •24. Термодинамическая система параметры состояния термодинамической системы. Основные положения молекулярно-кинетической теории газов.
- •25. Закон равномерного распределения энергии по степеням свободы молекул. Основное уравнение молекулярно-кинетической теории газов.
- •26. Закон Максвелла распределения молекул по скоростям теплового движения. Барометрическая формула. Распределение Больцмана.
- •27. Среднее число столкновений и средняя длина свободного движения молекул.
- •28. Первый закон термодинамики. Работа, теплота, теплоемкость, ее виды.
- •29. Политропный процесс, его частные случаи: изобарный, изотермический, адиабатный, изохорный.
- •30. Второй закон термодинамики. Энтропия. Тепловые двигатели и холодильные машины. Цикл Карно.
27. Среднее число столкновений и средняя длина свободного движения молекул.
Молекулы газа, находясь в состоянии хао тического движения, непрерывно сталки ваются друг с другом. Между двумя по следовательными столкновениями молеку лы проходят некоторый путь l, который называется длиной свободного пробега. В общем случае длина пути между по следовательными столкновениями различ на, но так как мы имеем дело с огромным числом молекул и они находятся в бес порядочном движении, то можно говорить о средней длине свободного пробега моле кул <l>.
Минимальное расстояние, на которое сближаются при столкновении центры двух молекул, называется эффективным диаметром молекулы d (рис.68). Он за висит от скорости сталкивающихся моле кул, т. е. от температуры газа (несколько уменьшается с ростом температуры).
Так как за 1 с молекула проходит в среднем путь, равный средней арифметической скорости <v>, и если (z) —сред нее число столкновений, испытываемых одной молекулой газа за 1 с, то средняя длина свободного пробега

<l>=<v>/<z>.
Для определения <z> представим себе молекулу в виде шарика диаметром d, которая движется среди других «застыв ших» молекул. Эта молекула столкнется только с теми молекулами, центры кото рых находятся на расстояниях, рав ных или меньших d, т. е. лежат внутри «ломаного» цилиндра радиусом d.
Среднее число столкновений за 1 с равно числу молекул в объеме «ломано го» цилиндра:
<z>=nV,
где n — концентрация молекул, V = = d2<v> (<v> —средняя скорость мо лекулы или путь, пройденный ею за 1с). Таким образом, среднее число столкновений
<z>=nd2<v>.
Расчеты показывают, что при учете дви жения других молекул
![]()
Тогда средняя длина свободного про бега
![]()
т.е. (l) обратно пропорциональна кон центрации n молекул. С другой стороны, из (42.6) следует, что при постоянной температуре n пропорциональна давлению р.
Следовательно,

28. Первый закон термодинамики. Работа, теплота, теплоемкость, ее виды.
Допустим, что некоторая система (газ, заключенный в цилиндр под поршнем), обладая внутренней энергией U1, получи ла некоторое количество теплоты Q и, перейдя в новое состояние, характеризую щееся внутренней энергией U2, совершила работу А над внешней средой, т. е. против внешних сил. Количество теплоты считает ся положительным, когда оно подводится к системе, а работа — положительной, когда система совершает ее против внеш них сил. Опыт показывает, что в соответ ствии с законом сохранения энергии при любом способе перехода системы из перво го состояния во второе изменение внутрен ней энергии U=U2-U1 будет одинако вым и равным разности между количест вом теплоты Q, полученным системой, и работой А, совершенной системой про тив внешних сил:
U=Q-A,
или
Q=U+A. (51.1)
Уравнение (51.1) выражает первое начало термодинамики: теплота, сообщаемая системе, расходуется на изменение ее внутренней энергии и на совершение ею работы против внешних сил.
Выражение (51.1) в дифференциаль ной форме будет иметь вид
dQ=dU+dA,
где dU — бесконечно малое изменение внутренней энергии системы.
Работа
Для рассмотрения конкретных процессов найдем в общем виде внешнюю работу, совершаемую газом при изменении его объема. Рассмотрим, например, газ, на ходящийся под поршнем в цилиндриче ском сосуде (рис. 78). Если газ, расширя ясь, передвигает поршень на бесконечно малое расстояние dl, то производит над ним работу
A=Fdl=pSdl=pdV,
где S — площадь поршня, Sdl=dV— из менение объема системы. Таким образом,
A=pdV. (52.1)
Полную работу A, совершаемую газом при изменении его объема от V1 до V2, найдем

интегрированием формулы (52.1):

Результат интегрирования определяется характером зависимости между давлением и объемом газа. Найденное для работы выражение (52.2) справедливо при любых изменениях объема твердых, жидких и га зообразных тел.
Теплота
Теплота - один из двух, известных современному естествознанию, способов передачи энергии - мера передачи неупорядоченного движения. Количество переданной энергии называют количеством теплоты.
а) изохорный процесс (V=const)
б) изобарный процесс (p=const)
в) изотермическом (T=const)
Теплоёмкость тела (обозначается C) — физическая величина, определяющая отношение бесконечно малого количества теплоты ΔQ, полученного телом, к соответствующему приращению его температуры ΔT:
![]()
Единица измерения теплоёмкости в системе СИ — Дж/К.
Удельная теплоемкость вещества ве личина, равная количеству теплоты, не обходимому для нагревания 1 кг вещест ва на 1 К:
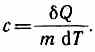
Единица удельной теплоемкости — джоуль на килограмм-кельвин (Дж/(кг•К)).
Молярная теплоемкость— величина, равная количеству теплоты, необходимому для нагревания 1 моля вещества на 1 К:
![]()
где v = m/M — количество вещества, вы ражающее число молей.
Единица молярной теплоемкости — джоуль на моль-кельвин (Дж/(моль•К)).
Удельная теплоемкость с связана с мо лярной Сm соотношением
Ст = сМ, (53.2)
где М — молярная масса вещества.
Понятие теплоёмкости определено как для веществ в различных агрегатных состояниях (твёрдых тел, жидкостей, газов), так и для ансамблей частиц и квазичастиц (в физике металлов, например, говорят о теплоёмкости электронного газа). Если речь идёт не о каком-либо теле, а о некотором веществе как таковом, то различают удельную теплоёмкость — теплоёмкость единицы массы этого вещества и молярную — теплоёмкость одного моля его.
Для примера, в молекулярно-кинетической теории газов показывается, что молярная теплоёмкость идеального газа с i степенями свободы при постоянном объеме равна:
![]()
А при постоянном давлении
![]()
