
- •Вопрос №21. Химия элементов s-блока. Электронные структуры атомов и катионов. Сравнение свойств ионов элементов 1а- и 2а-групп. Биологическая роль натрия, калия, магния, кальция.
- •Биологическая роль элементов. Химическое сходство и биологический антагонизм.
- •Вопрос №22.
- •Вопрос 23. Химия элементов p-блока
- •Поверхностное натяжение различных жидкостей на границе с воздухом при 293 к
- •Адсорбция на подвижной границе раздела фаз (на поверхности жидкости)
- •Титриметрический анализ
- •Вопрос 31
- •Вопрос№35
Вопрос 23. Химия элементов p-блока
p-блок в периодической таблице элементов — электронная оболочка атомов, валентные электроны которых с наивысшей энергией занимают p-орбиталь.
В p-блок входят последние шесть групп, исключая гелий (который находится в s-блоке). Данный блок содержит все неметаллы (исключая водород и гелий) и полуметаллы, а также некоторые металлы.
P-блок содержит в себе элементы, которые имеют различные свойства, как физические, так и механические. P-неметаллы — это, как правило, высокореакционные вещества, имеющие сильную электроотрицательность, p-металлы — умеренно активные металлы, причём их активность повышается к низу таблицы химических элементов.
24 Вопрос. Адсорбционные равновесия и …
Поверхностная энергия, приходящаяся на единицу площади поверхности (удельная поверхностная энергия), называется поверхностным натяжением ().
= Gs / S.
Единицы измерения поверхностного натяжения в СИ: Дж/м2 или Н/м, так как Дж = Нм.
Понятие о поверхностном натяжении (удельной поверхностной энергии) справедливо для любых гетерогенных систем, в том числе и для системы жидкость – жидкость, а также для твердого тела, граничащего с газом или жидкостью.
Поверхностное натяжение у разных жидкостей различно и зависит от природы жидкости, природы граничащей фазы, температуры, давления (если граничащая фаза газ), а также от природы и концентрации растворенных веществ.
Поверхностное натяжение различных жидкостей на границе с воздухом при 293 к
|
Жидкость |
Поверхностное натяжение , мДж/ м
|
Жидкость |
Поверхностное натяжение , мДж/ м |
|
Вода |
72,8 |
Хлороформ |
27,1 |
|
Глицерин |
64,7 |
Этанол |
22,3 |
|
Уксусная кислота |
27,6 |
Метанол |
22,6 |
|
Оливковое масло |
33,0 |
Сыворотка крови |
45,4 |
|
Бензол |
29,4 |
Фенол |
42,3 |
Адсорбция – самопроизвольное изменение концентрации растворенного вещества на границе раздела фаз. Адсорбция уменьшается с повышением температуры. Адсорбционное равновесие – равновесное распределение вещества между пограничным слоем и граничащими фазами. Является динамическим равновесиям и быстро устанавливается.
Адсорбция на подвижной границе раздела фаз (на поверхности жидкости)
Любая система в соответствии со вторым началом термодинамики стремится самопроизвольно перейти в такое состояние, при котором она обладает минимальным запасом энергии Гиббса. Следовательно, она стремится к минимуму поверхностной энергии Гиббса (Gs = S). Поэтому система, образованная одним компонентом, к примеру чистым растворителем ( = const при
Т = const), может понизить запас своей поверхностной энергии Гиббса в данных условиях только одним путем – принять форму, при которой поверхность раздела фаз минимальна.
Система, состоящая больше чем из одного компонента, помимо уменьшения площади поверхности, может понизить поверхностную энергию Гиббса и путем уменьшения поверхностного натяжения (), то есть путем перераспределения растворенного вещества между объемом жидкой фазы и поверхностным слоем. Рассмотрим возможные случаи распределения растворенного вещества в водном растворе (рис.4).
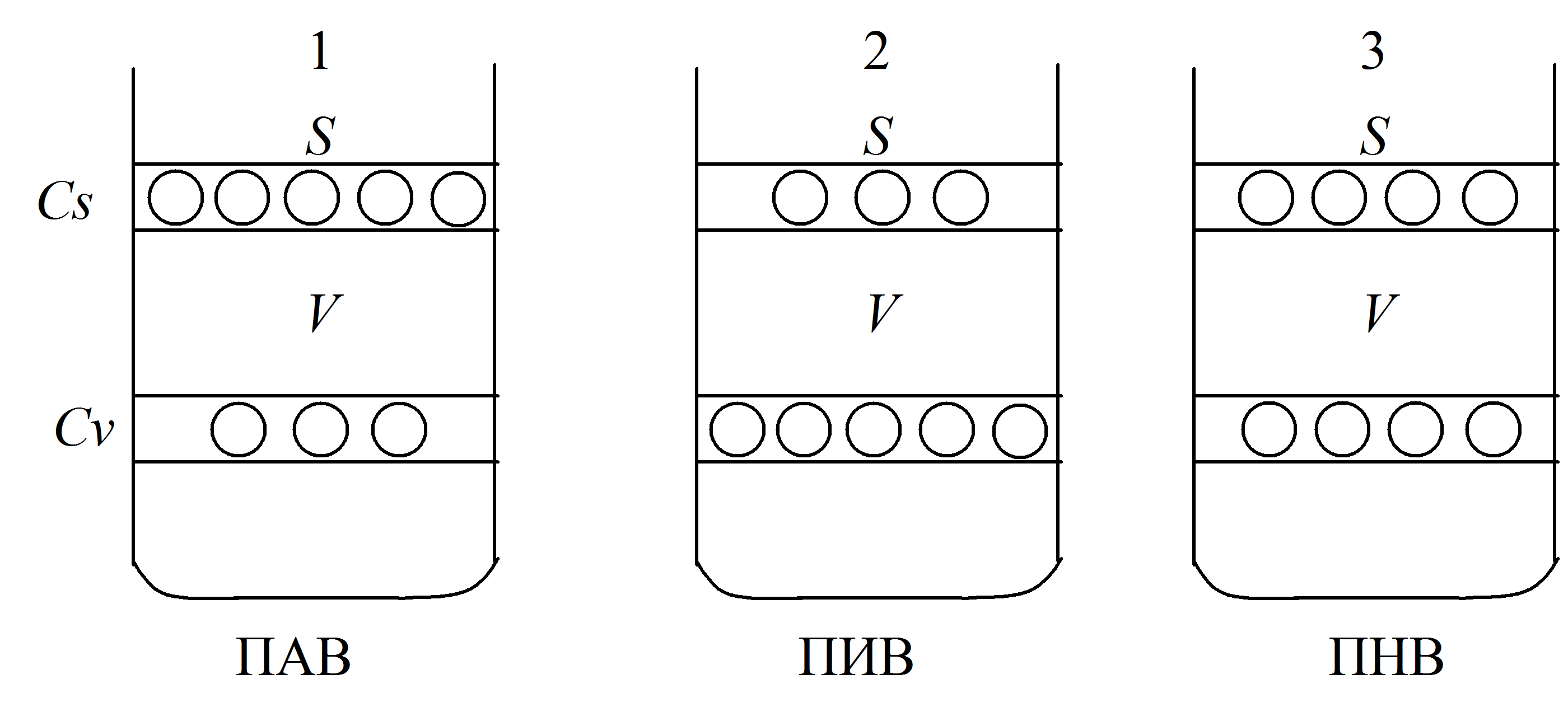
Рис.4 . Возможные случаи распределения растворенного вещества между
поверхностным слоем и объемом жидкой фазы (воды).
Сs – концентрация растворенного вещества в поверхностном слое;
Сv – концентрация растворенного вещества в объеме фазы
1. ПАВ уменьшают поверхностное натяжение растворителя (воды) и поэтому накапливаются в поверхностном слое (Сs>Сv), в связи с чем в системе уменьшается запас поверхностной энергии Гиббса. ПАВ должны обладать: а) поверхностным натяжением меньшим по сравнению с поверхностным натяжением растворителя, иначе накопление вещества в поверхностном слое было бы термодинамически невыгодно; б) сравнительно малой растворимостью (если бы они были хорошо растворимы, то стремились бы уйти с поверхности вглубь жидкости).
2. ПИВ увеличивают поверхностное натяжение растворителя (воды), поэтому накапливаются в объеме фазы (Сs<Сv), поскольку только в этом случае запас поверхностной энергии Гиббса в системе относительно уменьшается. ПИВ должны обладать следующими свойствами: а) их поверхностное натяжение должно быть больше поверхностного натяжения растворителя; иначе они будут стремиться самопроизвольно накапливаться в поверхностном слое; б) их растворимость должна быть высокой, так как лишь при этом условии они будут стремиться уйти с поверхности в объем.
3. ПНВ не изменяют поверхностное натяжение растворителя (воды), поэтому их концентрация в поверхностном слое такая же, как и в объеме фазы (Сs=Сv).
Ориентация молекул ПАВ в поверхностном слое.
Структура биологических мембран
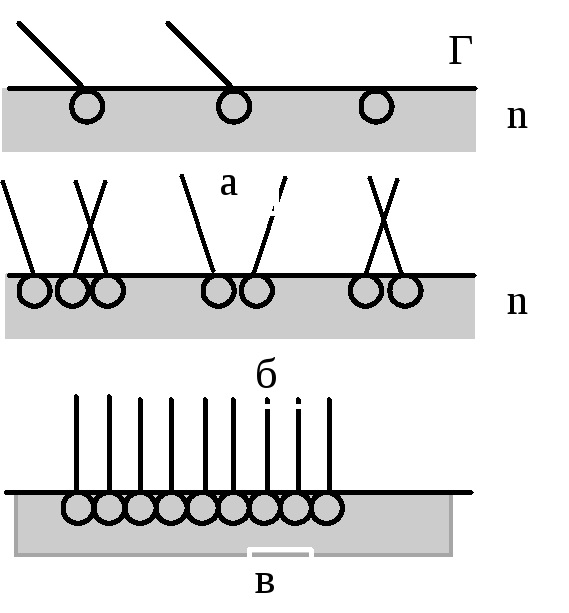
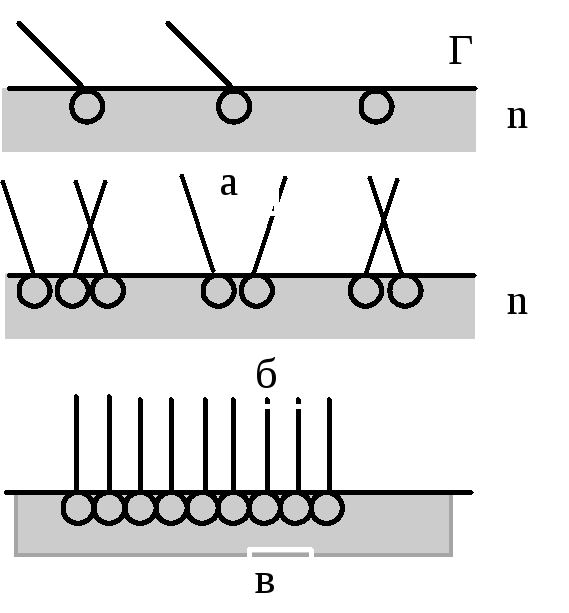
Молекулы ПАВ состоят из двух частей: полярной (гидрофильной) и неполярной (гидрофобной). При адсорбции полярная группа, обладающая большим сродством с полярной фазой (например, с водой) втягивается в нее. В то же время неполярная группа выталкивается в неполярную фазу (рис.8).
При малых концентрациях ПАВ углеводородные радикалы «лежат» на поверхности полярной жидкости, а полярные группировки погружены в нее (рис.8 а).
С увеличением концентрации ПАВ в растворе число молекул, находящихся в поверхностном слое, возрастает. Это приводит в пределе к образованию на граничной поверхности насыщенного мономолекулярного адсорбционного слоя (рис.8 б), в котором молекулы ПАВ предельно ориентированы. Данный слой образно называется молекулярным частоколом Лэнгмюра. Существованием мономолекулярного насыщенного слоя объясняется постоянство предельной адсорбции Г у органических веществ одного и того же гомологического ряда.
Представления об ориентации молекул ПАВ в насыщенном адсорбционном слое сыграли большую роль в развитии учения о структуре биологических мембран
Клеточные мембраны образованы главным образом молекулами двух типов: липидами и белками.
Липиды
нерастворимы в воде, но растворимы в
органических растворителях. Особенностью
мембранных липидов является то, что на
одном конце их молекулы есть полярные
группы (например, –СООН),
обладающие гидрофильными свойствами,
тогда как другой ее конец представляет
собой длинную углеводородную цепь с
гидрофобными свойствами. Липиды образуют
бимолекулярные пленки (толщиной около
70![]() ),
в которых полярные группы располагаются
на обеих поверхностях мембраны, а
неполярные погружены внутрь ее.
),
в которых полярные группы располагаются
на обеих поверхностях мембраны, а
неполярные погружены внутрь ее.
Молекулы белка могут располагаться вблизи внешней и внутренней поверхностей мембраны, а также проникать, частично или полностью, через всю ее толщину.
Обычно клеточные мембраны весьма прочны и обладают свойствами электрического изолятора. Биологические мембраны не являются жесткими структурами. Например, во многих случаях белки и липиды внутри мембран находятся в постоянном движении.
Дополнение к вопросу:
Значение поверхностных явлений в медицине. Вода – наиболее часто применяющийся растворитель. Она обладает большим поверхностным натяжением (72,75 мДж / м2 при 20 o С ), поэтому по отношению к ней многие вещества являются поверхностно-активными. Поверхностное натяжение биологических жидкостей (например, сыворотки крови – см. табл.1) меньше воды вследствие наличия в них ПАВ различной природы (кислоты жирного ряда, стероиды и др.). В результате эти вещества самопроизвольно накапливаются (адсорбируются) у стенок сосудов, клеточных мембран, что облегчает их проникновение сквозь эти мембраны.
Изменение поверхностного натяжения биологических жидкостей используется в диагностических целях. К примеру, поверхностное натяжение плазмы крови значительно изменяется при различных заболеваниях (анафилактический шок, рак и др.). С возрастом человека поверхностное натяжение сыворотки крови уменьшается.
Из многочисленных методов измерения поверхностного натяжения при биохимических, физиологических и клинических исследованиях чаще всего используют сталагмометрический метод (описан в экспериментальной работе.)
Вопрос №25. Классификация дисперсным систем: по степени дисперсности, по агрегатному состоянию фаз, по силе межмолекулярного взаимодействия между дисперсной фазой и дисперсионной средой. Природа коллоидного состояния. Молекулярно-кинетические свойства коллоидно- дисперсных систем.
Дисперсные системы - системы, состоящие из дисперсной фазы – совокупности раздробленных частиц и непрерывной дисперсионной среды, в которой во взвешенном состоянии находятся эти частицы.
Классификация д.с. 1. По степени дисперсности:
-
Грубодисперсные (размер частиц от 10-7 до 10-5 м)
-
Коллоидно-дисперсные (размер частиц от 10-9 до 10-7 м)
2. По агрегатному состоянию фаз:
Коллоидно-дисперсные:
-
Системы с твердой дисперсионной средой – солидозоли
-
Системы с жидкой дисперсионной средой - лиозоли (золи)
-
Системы с газообразной дисперсионной средой – аэрозоли
Грубо-дисперсные:
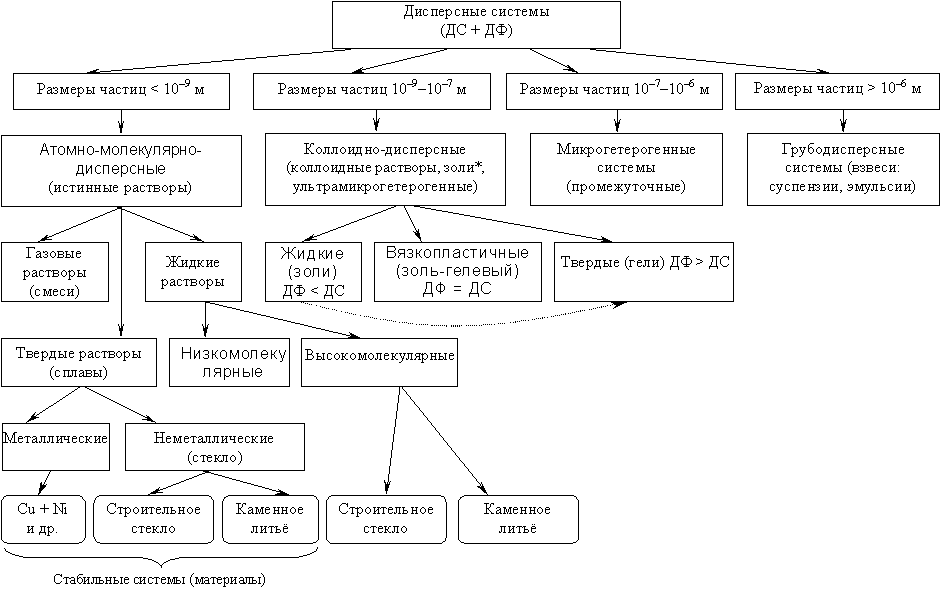
3. По интенсивности межмолекулярного взаимодействия:
-
Лиофобные – со слабым взаимодействием. Являются необратимыми: частицы дисперсионной фазы не способны самопроизвольно диспергироваться в дисперсионной среде. Характерны существенные отличия в химическом составе и строении граничащих фаз.(золи металлов, оксидов металлов, труднорастворимых солей в воде)
-
Лиофильные – с сильным взаимодействием. К ним относятся растворы высокомолекулярных веществ (мыло,алкалоиды,красители и т.д.)
Природа коллоидного состояния. Свойства коллоидно-дисперсных систем.
1. Все коллоидные растворы способны рассеивать свет или опалесцировать.
2. Диффузия частиц в коллоидных растворах протекает весьма медленно.
3. Коллоидные растворы имеют очень малое осмотическое давление, которое часто даже трудно обнаружить.
4. Коллоидные растворы способны к диализу, т. е. с помощью полупроницаемой перегородки (мембраны) могут быть отделены от растворенных в них примесей низкомолекулярных веществ. При диализе молекулы растворенного низкомолекулярного вещества проходят через мембрану, а коллоидные частицы, неспособные проникать через полупроницаемую перегородку остаются за ней в виде очищенного коллоидного раствора.
5. Коллоидные растворы агрегативно неустойчивы (лабильны) - т. е. коллоиднорастворенное вещество способно сравнительно легко выделяться из раствора (коагулировать) под влиянием незначительных внешних воздействий. В результате в коллоидном растворе образуется осадок (коагулят, коагулюм)
6. Коллоидные растворы обычно обнаруживают явление электрофореза
Вопрос №26. Оптические свойства – рассеивание света. Электрические свойства: электрофорез и электроосмос. Строение двойного электрического слоя.
Оптические свойства коллоидных растворов. Прохождение света через коллоидную систему вызывает три оптических эффекта: поглощение, отражение и рассеивание лучей. Поглощение свойственно всем системам, тогда как отражение более характерно для грубодисперсних систем (эмульсий и суспензий), где размер частиц больше, чем длина волны облучения. Поэтому, в отличие от молекулярных и ионных растворов, которые не имеют поверхности раздела фаз и оптически однородны, коллоидные растворы рассеивают свет. Это проявляется опалесценцией в виде голубоватого матового свечения при освещении боковым светом. При пропускании параллельного пучка света через коллоидный раствор наблюдается конус рассеянного света – эффект Тиндаля. По способности рассеивать свет можно определять концентрацию коллоидных частиц в растворе - метод нефелометрии.
Электрокинетические свойства коллоидных растворов.
Электроосмос – явление перемещения дисперсной среды (т.е. растворителя) относи-тельно неподвижной дисперсной фазы, которое можно наблюдать при прохождении электрического тока через U–образную стеклянную трубку, заполненную кварцевым песком и водой. В катодной части трубки наблюдается повышение уровня воды. Электрофорез – явление перемещения коллоидных частиц относительно дисперснойсреды (растворителя), под влиянием постоянного электрического тока. Так, при прохождении электрического тока через устройство из двух стеклянных трубок, установленных в увлажненную глину, от поверхности отрываются отрицательно заряженные частицы глины,которые перемещаются к аноду. Метод электрофореза широко применяется в меди-цине для разделения Больших молекул и даже клеток. Существует много вариантов: свободный электрофорез, электрофорез на бумаге, в агаровом и полиакриламидном гелях и др.
Строение коллоидных частиц.
Считают, что коллоидный раствор состоит из мицелл, которые образуются заряженными коллоидными частицами. Заряд возникает вследствие избирательной адсорбции ионов на поверхности частиц, или за счет ионизации поверхностных функциональных групп твердой фазы. В мицелле различают три составных части: ядро, адсорбционный слой ионов и диффузионный слой ионов. Ядро составляет основную массу мицеллы и является совокупностью нейтральных атомов или молекул, общим числом сотни и миллионы единиц. На ядре адсорбируются ионы (избирательная адсорбция) которые придают ему определенный заряд,поэтому их называют потенциалообразующими. Потенциал, возникающий на ядре, получилеще название электротермодинамического и он обуславливает дальнейшее присоединение кпотенциал-образующим ионам некоторого количества других ионов с противоположнымзнаком заряда. Такой двойной электрический слой, потенциало-образующих ионов, вместе с противоионами (ионами з противоположным знаком) составляет адсорбционный слой ионов. Часть противоионов слабо связана с потенциало-образующими ионами и свободно перемещается в растворителе, формируя диффузионный слой. Ядро вместе с адсорбционным и диф-фузионным слоями ионов и составляет мицеллу, которая в целом является электронейтраль-ной (тогда как сама коллоидная частица несет определенный заряд).
Вопрос№29
Электрохимический потенциал — физическая величина, связывающая химический потенциал (μ) и электрический потенциал (φ) некоторой электрохимической системы соотношением:
A = μ + e·φ
где А — работа, нарушающая электрохимическое равновесие системы; e — элементарный заряд частицы.
Для растворенного вещества:
μ = μ0 + R*T*lnC + z*F*φ
где
μ0 - Стандартный химический потенциал, зависящий от природы растворителя.
С - концентрация вещества
R - газовая постоянная
T - температура
z - валентность иона
F - число Фарадея
φ - электрический потенциал
Дисперсные системы, гетерогенные системы из двух или большего числа фаз с сильно развитой поверхностъю раздела между ними. Обычно одна из фаз образует непрерывную дисперсионную среду, в объеме которой распределена дисперсная фаза (или несколько дисперсных фаз) в виде мелких кристаллов. твердых аморфных частиц, капель или пузырьков. Дисперсные системы могут иметь и более сложное строение, например, представлять собой двухфазное образование, каждая из фаз которого, будучи непрерывной, проникает в объем другой фазы. К таким системам относятся твердые тела. пронизанные разветвленной системой каналов-пор, заполненных газом илижидкостью. некоторые микрогетерогенные полимерные композиции и др. Нередки случаи, когда дисперсионная среда "вырождается" до тончайших слоев (пленок), разделяющих частицы дисперсной фазы.
Основные типы дисперсных систем. По дисперсности, то есть размеру частиц дисперсной фазы или отношению общей площади межфазной поверхности к объему (или массе) дисперсной фазы (удельной поверхности), Дисперсные системы условно делят на грубодисперсные и тонко(высоко)дисперсные. Последние, по традиции, называемые коллоидно-дисперсными или просто коллоидными системами. В грубодисперсных системах частицы имеют размеры от 1 мкм и выше (удельная поверхность не более 1 м2/г), в коллоидных - от 1 нм до 1 мкм (удельная поверхность достигает сотен м2/г). Дисперсность оценивают по усредненному показателю (среднему размеру частиц, удельной поверхности) или дисперсному составу (см. Дисперсионный анализ). Тонкопористые тела характеризуют пористостью -понятием, аналогичным дисперсности.В свободнодисперсных системах сцепление между частицами дисперсной фазы отсутствует, каждая частица кинетически независима и при достаточно малых размерах участвует в интенсивном броуновском движении. Для структурированных (связнодисперсных) систем характерно наличие неупорядоченной пространственной сетки (каркаса), образованной частицами дисперсной фазы (см. Структурообразование в дисперсных системах). Особую группу составляют высококонцентрированные дисперсные системы, в которых частицы находятся в "стесненных" условиях как, например, в периодических коллоидных структурах. Механические свойства свободнодисперсных систем определяются главным образом свойствами дисперсионной среды, а связнодисперсных систем - также свойствами и числом контактов между частицами дисперсной фазы.
По агрегатному состоянию дисперсионной среды и дисперсной фазы выделяют следующие основные виды дисперсных систем: 1) аэродисперсные (газодисперсные) системы с газовой дисперсионной средой: аэрозоли (дымы, пыли. туманы), порошки. волокнистые материалы типа войлока. 2) Системы с жидкой дисперсионной средой; дисперсная фаза может быть твердой (грубодисперсные суспензии и пасты, высокодисперсные золи и гели), жидкой (грубодисперсные эмульсии, высокодисперсные микроэмульсии и латексы) или газовой (грубодисперсные газовыеэмульсии и пены). 3) Системы с твердой дисперсионной средой: стеклообразные или кристаллические тела с включениями мелких твердых частиц, капель жидкости или пузырьков газа, например, рубиновые стекла, минералытипа опала, разнообразные микропористые материалы. Отдельные группы дисперсных систем составляют многие металлические сплавы, горные породы, сложные композиционные и другие многофазные системы.
Лиофильные и лиофобные дисперсные системы с жидкой дисперсионной средой различаются в зависимости от того, насколько близки или различны по своим свойствам дисперсная фаза и дисперсионная среда. В лиофильных дисперсных системах межмолекулярные взаимодействия по обе стороны разделяющей фазы поверхности различаются незначительно, поэтому удельная свободная поверхностная энергия (для жидкости - поверхностное натяжение) чрезвычайно мала (обычно сотые доли мДж/м2), межфазная граница (поверхностный слой) может быть размыта и по толщине нередко соизмерима с размером частиц дисперсной фазы. Лиофильные дисперсные системы термодинамически равновесны, они всегда высокодисперсны, образуются самопроизвольно и при сохранении условий их возникновения могут существовать сколь угодно долго. Типичные лиофильные дисперсные системы -микроэмульсии. некоторые полимер-полимерные смеси, мицеллярные системы ПАВ, Дисперсные системы с жидкокристаллическими дисперсными фазами. К лиофильным дисперсным системам часто относят также набухающие и самопроизвольно диспергирующиеся в водной среде минералы группы монтмориллонита, например, бентонитовыеглины.
Следует отметить, что в прошлом "лиофильными коллоидами" называли растворы полимеров. то есть принципиально гомогенные системы. Однако в современной терминологии понятие "коллоид" относится только к микрогетерогенным системам; по отношению к гомогенным (однофазным) системам его не употребляют.
В лиофобных дисперсных системах межмолекулярное взаимодействие в дисперсионной среде и в дисперсной фазе существенно различно; удельная свободная поверхностная энергия (поверхностное натяжение) велика - от нескольких единиц до нескольких сотен (и тысяч) мДж/м2; граница фаз выражена достаточно четко. Лиофобные дисперсные системы термодинамически неравновесны; большой избыток свободной поверхностной энергии обусловливает протекание в них процессов перехода в более энергетически выгодное состояние. В изотермических условиях возможна коагуляция -сближение и объединение частиц, сохраняющих первоначальные форму и размеры, в плотные агрегаты, а также укрупнение первичных частиц вследствие коалесценции -слияния капель или пузырьков газа, собирательной рекристаллизации (в случае кристаллич. дисперсной фазы) или изотермич. перегонки (молекулярного переноса) вещества дисперсной фазы от мелких частиц к крупным (в случае дисперсных систем с жидкой дисперсионной средой - последний процесс называемый переконденсацией). Нестабилизованные и, следовательно, неустойчивые лиофобные дисперсные системы непрерывно изменяют свой дисперсный состав в сторону укрупнения частиц вплоть до полного расслоения на макрофазы. Однако стабилизованные лиофобные дисперсные системы могут сохранять дисперсность в течение длительного времени.
Образование дисперсных систем. Возможно двумя путями: диспергационным и конденсационным. Диспергирование макрофаз с образованием лиофильных дисперсных систем происходит самопроизвольно - для этого достаточно энергии теплового движения. Такой процесс осуществляется при значениях поверхностного натяжения s ниже некоторого критического значения sкр = bkТ/d2, где d - размер частиц дисперсной фазы, Т - абсолютная температура, k - постоянная Больцмана. b - безразмерный коэффициент, принимающий значения примерно 10-30.
Образование лиофобных дисперсных систем путем диспергирования стабильной макрофазы требует значительных энергетических затрат, определяемых суммарной площадью поверхности частиц дисперсной фазы. В реальных условиях на образование поверхности при измельчении твердых тел или при распылении и эмульгировании жидкостей приходится лишь небольшая часть (доли процента) подводимой к системе энергии; остальное расходуется на побочные процессы и рассеивается в окружающем пространстве (см. Диспергирование).
Конденсационный путь образования дисперсных систем связан с зарождением новой фазы (или новых фаз) в пересыщенной метастабильной исходной фазе - будущей дисперсионной среде. Для возникновения высокодисперсной системы необходимо, чтобы число зародышей новой фазы было достаточно большим, а скорость их роста не слишком велика. Кроме того, требуется наличие факторов, ограничивающих возможности чрезмерного разрастания и сцепления частиц дисперсной фазы. Переход первоначально стабильной гомогенной системы в метастабильное состояние может произойти в результате изменения термодинамических параметров состояния (давления, температуры, состава). Так образуются, например, природные и искусственные аэрозоли (туман - из переохлажденных водяных паров, дымы - из парогазовых смесей, выделяемых при неполном сгорании топлива), некоторые полимерные системы - из растворов при ухудшении "термодинамического качества" растворителя, органические золи металловпутем конденсации паров металла совместно с парами органической жидкости или при пропускании первых через слой органической жидкости, коллоидно-дисперсные поликристаллические тела (металлические сплавы. некоторые виды горных пород и искусственных неорганических материалов).
Возможно также образование дисперсных систем в результате химической реакции в гомогенной среде, если продукт реакции при данных условиях находится в агрегатном состоянии, отличном от "материнской" фазы, или практически не растворяется в ней. Примерами подобных систем могут служить аэрозоли с твердыми частицами NH4Cl (образуются при взаимодействии газообразных NH3 и НСl), аэрозоли с капельно-жидкими частицами H2SO4 (при взаимодействии SO3и водяного пара). В природе и технологических процессах часто образуются гидр.золи разного состава при гидролизесолей и др. соед., неустойчивых к действию воды. Окислительно-восстановительные реакции используют для получения золей Аu и Ag, разложение Na2S2O3 разбавленной серной или соляной кислотой - для получения гидрозоля элементарной серы. Хим. или термохим. разложения карбонатов, органических порофоров (порообразователей, вспенивающих агентов) и других соединений с выделением газообразных веществ в первоначально жидких средах лежит в основе промышленного производства многих пеноматериалов.
Устойчивость дисперсных систем характеризуется постоянством дисперсности (распределения частиц по размерам) и концентрации дисперсной фазы (числом частиц в единице объема). Наиболее сложна в теоретическом аспекте и важна в практическом отношении проблема устойчивости аэрозолей и жидких лиофобных дисперсных систем.
Различают седиментационную устойчивость и устойчивость к коагуляции (агрегативную устойчивость). Седиментационно устойчивы коллоидные системы с газовой и жидкой дисперсионной средой, в которых броуновское движение частиц препятствует оседанию; грубодисперсные системы с одинаковой плотностью составляющих их фаз; системы, скоростью седиментации в которых можно пренебречь из-за высокой вязкости среды.
В агрегативно устойчивых дисперсных системах непосредственно контакты между частицами не возникают, частицы сохраняют свою индивидуальность. При нарушении агрегативной устойчивости дисперсных систем частицы, сближаясь в процессе броуновского движения, соединяются необратимо или скорость агрегации становится значительно больше скорости дезагрегации. Между твердыми частицами возникают непосредственные точечные ("атомные") контакты, которые затем могут превратиться в фазовые (когезионные) контакты, а соприкосновение капель и пузырьков сопровождается их коалесценцией и быстрым сокращением суммарной площади межфазной поверхности. Для таких систем потеря агрегативной устойчивости означает также потерю седимeнтационной устойчивости.
В агрегативно устойчивых системах дисперсный состав может изменяться вследствие изотермич. перегонки - молекулярного переноса вещества дисперсной фазы от мелких частиц к более крупным. Этот процесс обусловлен зависимостью давления насыщенного пара (или концентрации насыщенного раствора) от кривизны поверхности раздела фаз.
Агрегативная устойчивость и длительное существование лиофобных дисперсных систем с сохранением их свойств обеспечивается стабилизацией. Для высокодисперсных систем с жидкой дисперсионной средой используют введение веществ - стабилизаторов (электролитов, ПАВ, полимеров. В теории устойчивости Дерягина-Ландау-Фервея-Овербека (теории ДЛФО) основная роль отводится ионно-электростатическому фактору стабилизации. Стабилизация обеспечивается электростатическим отталкиванием диффузных частей двойного электрического слоя, который образуется при адсорбции ионов электролита на поверхности частиц. При некотором расстоянии между частицами отталкивание диффузных слоев обусловливает наличие минимума на потенциальной кривой (дальний, или вторичный, минимум; смотри рисунок). Хотя этот минимум относительно неглубок, он может препятствовать дальнейшему сближению частиц, притягиваемых силами межмолекулярного взаимодействия. Ближний, или первичный, минимум соответствует прочному сцеплению частиц, при котором энергии теплового движения недостаточно для их разъединения. Сближаясь на расстояние, отвечающее этому минимуму, частицы объединяются в агрегаты, образование которых ведет к потере системой агрегативной устойчивости. При этом устойчивость системы к коагуляции определяется высотой энергетического барьера.
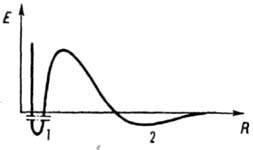
Зависимость энергии взаимодействия Е между частицами от расстояния R: 1 и 2 - ближний и дальний минимумы соответственно.
При введении в Дисперсные системы в качестве стабилизатора ПАВ фактором стабилизации может быть "термодинамическая упругость" пленок среды, разделяющей частицы. Стабилизация обеспечивается тем, что при сближении частиц, например, капель или газовых пузырей, происходит растяжение и утоньшение разделяющей их прослойки, содержащей ПАВ, и, как следствие, нарушение адсорбционного равновесия. Восстановление этого равновесия и приводит к повышению устойчивости прослойки среды, разделяющей частицы.
Гидродинамич. сопротивление вытеснению жидкой дисперсионной среды из прослойки между сближающимися частицами - один из кинетических факторов стабилизации дисперсных систем. Он особенно эффективен в системах с высоковязкой дисперсионной средой, а при застекловывании последней делает систему неограниченно устойчивой к агрегации частиц и коалесценции. Структурно-механический фактор стабилизации, по П. А. Ребиндеру, возникает при образовании на межфазной границе полимолекулярных защитных слоев из мицеллообразующих ПАВ, высокомолекулярных соединений, а иногда и тонких сплошных или дискретных фазовых пленок. Межфазный защитный слой должен обладать способностью сопротивляться деформациям и разрушению, достаточной подвижностью для "залечивания" возникших в нем дефектов и, что особенно важно, быть лиофилизованным с внешней стороны, обращенной в сторону дисперсионной среды. Если защитный слой недостаточно лиофилен, он, предохраняя частицы от коалесценции. не сможет предотвратить коагуляции. Структурно-механический барьер является, по существу, комплексным фактором стабилизации, который включает термодинамические, кинетические и структурные составляющие. Он универсален и способен обеспечить высокую агрегативную устойчивость любых дисперсных систем с жидкой дисперсионной средой, в том числе высококонцентрированных, наиболее важных в практическом отношении.
Основные свойства дисперсных систем определяются поверхностными явлениями: адсорбцией, образованием двойного электрического слоя и обусловленных им электрокинетических явлений, контактными взаимодействиями частиц дисперсной фазы. Размер частиц определяет оптические (светорассеяние и другие) и молекулярно-кинетические свойства (диффузия, термофорез, осмос и дрeubt).
Дисперсные системы повсеместно распространены в природе. Это - горные породы, грунты, почвы, атмосферные и гидросферные осадки, растительные и животные ткани. Дисперсные системы широко используют в технологических процессах; в виде дисперсных систем выпускается большинство промышленных продуктов и предметов бытового потребления. Высокодисперсные технические материалы (наполненные пластики, дисперсноупрочненные композиционные материалы) отличаются чрезвычайно большой прочностью. На высокоразвитых поверхностях интенсивно протекают гетерогенные и гетерогенно-каталитические химические процессы.
Учение о дисперсных систем и поверхностных явлениях в них составляет сущность коллоидной химии. Самостоятельный раздел коллоидной химии - физико-химическая механика - изучаeт закономерности структурообразования и механические свойства структурированных дисперсных систем и материалов в их связи с физико-химическими явлениями на межфазных границах.
Вопрос №30
