
- •Министерство образования и науки рф
- •1. Исследование адиабатного процесса.
- •2.Теплота и работа как формы передачи энергии. Аналитическое выражение и графическое изображение.
- •Исследование цикла двс с изохорным подводом тепла, его кпд.
- •4.Основное уравнение теплопередачи.
- •Рекуперативные теплообменные аппараты.
Министерство образования и науки рф
Тольяттинский государственный университет
Кафедра «Водоснабжение и водоотведение»
Контрольная работа
По дисциплине: Гидравлика и теплотехника
Вариант 21
Студентка: Шпрингер Д.С
Группа: ЗОСб-301
Преподаватель: Козина Л.Н.
Тольятти 2011
1. Исследование адиабатного процесса.
Адиабатным называется процесс, который протекает без теплообмена с окружающей средой (dq = 0).
В обратимых адиабатных процессах энтропия не изменяется (ds = 0, s = const), в необратимых - энтропия увеличивается (ds > 0).
Уравнение обратимого адиабатного процесса имеет вид
|
|
(4.43) |
где k – показатель адиабаты.
Для идеального газа
|
|
(4.44) |
Для одноатомного идеального газа показатель адиабаты не зависит от температуры:
|
|
Для двух-, трех- и многоатомных идеальных газов k = f(T), т.к. теплоемкость cv =f(T). С увеличением температуры показатель адиабаты убывает.
Если принять теплоемкость постоянной в соответствии молекулярно-кинетической теорией газов, то для двухатомных газов
|
|
для трех- и многоатомных газов:
|
|
Расчет адиабатных процессов двух-, трех- и многоатомных газов при значениях показателя адиабаты 1,4; 1,29 является приближенным, т.к. не учитывает зависимость теплоемкости от температуры.
Совместное решение (4.43) с уравнением состояния идеального газа pv = RT дает следующие связи параметров:
|
|
(4.45) |
|
|
(4.46) |
Для адиабатного процесса 1-2, в котором параметры изменяются от p1, v1, T1 до p2, v2, T2, на основании уравнений (4.43), (4.45), (4.46) можно получить следующие соотношения между параметрами:
|
|
(4.47) |
|
|
(4.48) |
|
|
(4.49) |
Совместное решение уравнений
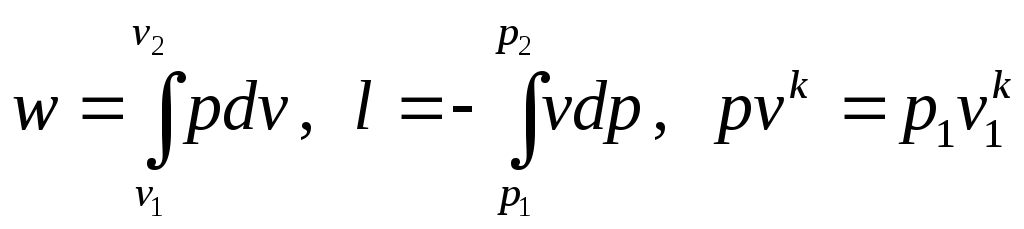
позволяет получить расчетные формулы для работы адиабатного процесса 1-2:
|
|
(4.50) |
|
|
(4.51) |
С учетом уравнения состояния pv = RT, а также соотношения (4.48) формулу (4.50) можно представить следующим образом:
|
|
(4.52) |
|
|
(4.53) |
По формулам (4.46) - (4.53) производят расчеты адиабатных процессов одноатомного идеального газа и приближенные расчеты двух-, трех- и многоатомных газов при значениях k = 1,4, k = 1,29.
Расчет адиабатных процессов с учетом зависимости k = f(T) по вышеприведенным формулам прост, если известны температуры T1 и T2. В противном случае используется метод последовательных приближений, что значительно усложняет расчет.
Более простым является табличный метод расчета адиабатного процесса идеального газа с учетом зависимости теплоемкости от температуры. В основе расчета лежат следующие уравнения:
|
|
(4.54) |
|
|
(4.55) |
|
|
(4.56) |
|
|
(4.57) |
Здесь
![]() - безразмерные величины, приведенные в
таблицах термодинамических свойств
газов [7], h, u - табличные значения
параметров.
- безразмерные величины, приведенные в
таблицах термодинамических свойств
газов [7], h, u - табличные значения
параметров.
О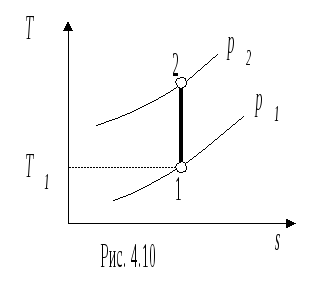
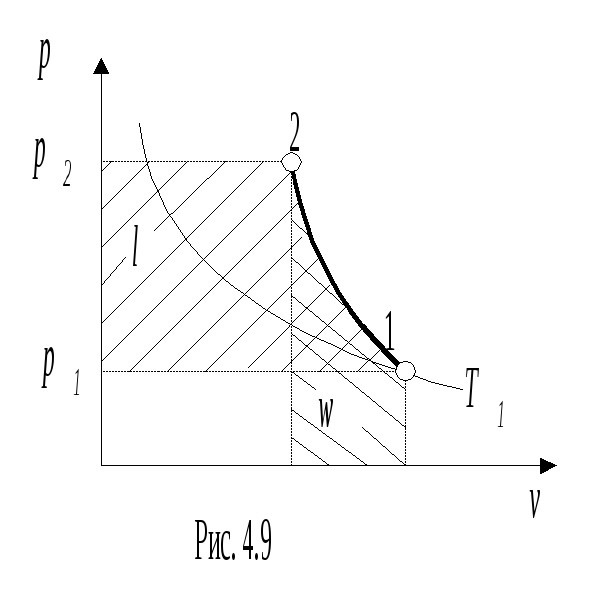 братимый
адиабатный процесс сжатия
идеального газа, построенный по исходным
параметрам p1, T1,
p2 в p-v- и T-s-
диаграммах, представлен на рис.4.9 и 4.10.
братимый
адиабатный процесс сжатия
идеального газа, построенный по исходным
параметрам p1, T1,
p2 в p-v- и T-s-
диаграммах, представлен на рис.4.9 и 4.10.
В p-v- диаграмме адиабата - несимметричная гипербола располагается круче изотермы, в T-s- диаграмме – изоэнтропа (s = const, q = 0).
Н
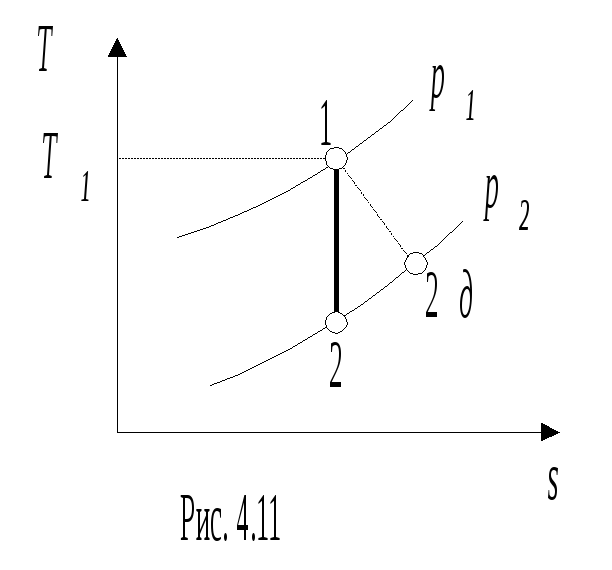 еобратимые
адиабатные процессы (1-2д), протекающие
с увеличением энтропии, показаны на
рис. 4.11, 4.12.
еобратимые
адиабатные процессы (1-2д), протекающие
с увеличением энтропии, показаны на
рис. 4.11, 4.12.
Работа необратимого адиабатного расширения (рис.4.11) равна
|
|
и она меньше работы обратимого процесса, вычисляемого по формуле
|
|
Напротив, работа необратимого адиабатного сжатия (рис. 4.12), равная
|
|
больше работы обратимого процесса
|
|
Дано: p1 = 50 бар, t1 = 480 0C, t2 = 100 0C.
Определить: w, l.
Расчет процесса с помощью таблиц
1. Определяют начальное состояние. При p1 = 50 бар температура насыщения ts = 263,9 0С. Поскольку t1 > ts, то рабочее тело является перегретым паром. Из табл. III находят
h1 = 3367,2 кДж/кг, v1 = 0,06644 м3/кг, s1 = 6,9158 кДж/кг.К.
Рассчитывают внутреннюю энергию:
u1 = h1 - p1.v1 = 3387,2 - 50.102.0,06644 = 3055 кДж/кг.
-
Определяют конечное состояние путем сравнения энтропии s2 = s1= 6,9158 кДж/(кг.К) с s и s, взятыми из табл. I по температуре t2 = 100 0С. Поскольку s < s < s, то конечное состояние рабочего тела - мокрый пар. Рассчитывают степень сухости и параметры мокрого пара:
|
|
|
|
|
|
|
|
-
Рассчитывают работу адиабатного процесса:
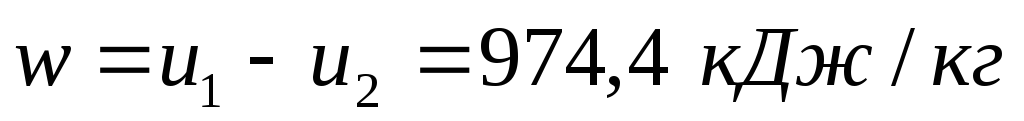 ,
,
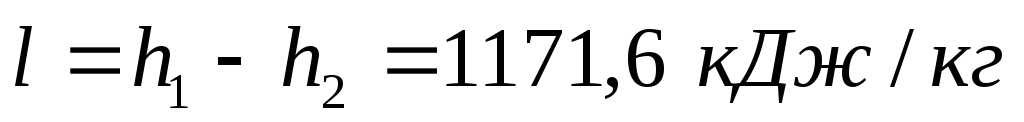
-
П
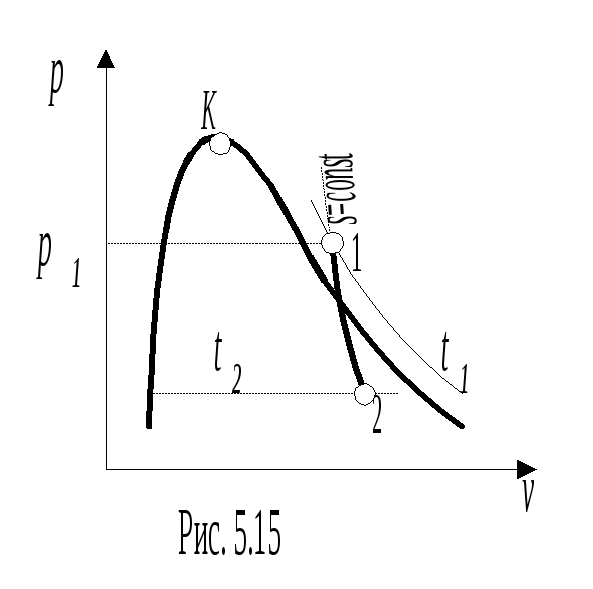
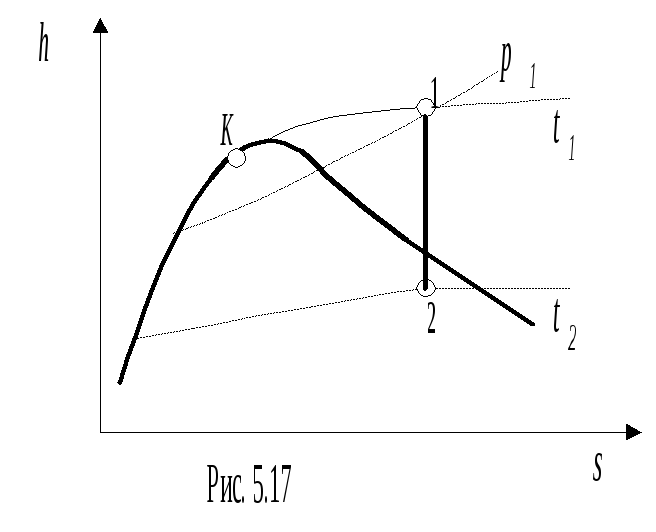
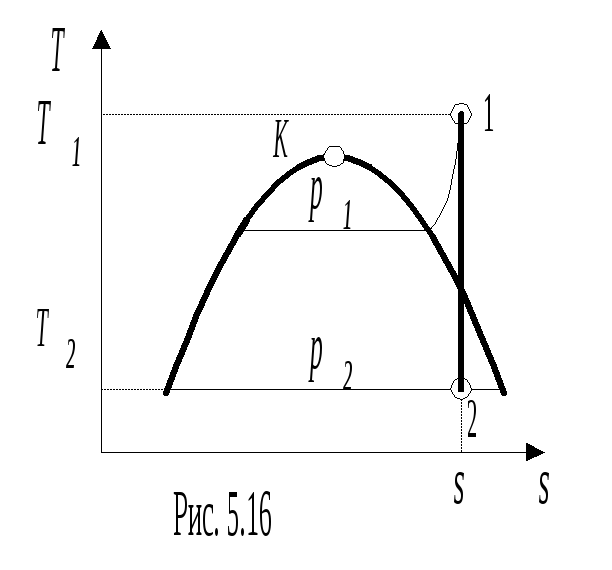 редставляют
процесс в диаграммах p - v, T - s, h
- s (рис. 5.15-5.17)
редставляют
процесс в диаграммах p - v, T - s, h
- s (рис. 5.15-5.17)
