
49 Водород
Водород → Гелий 1H Внешний вид простого вещества газ без цвета, вкуса и запаха
Свойства атома
Имя, символ, номер Водород / Hydrogenium (H), 1, Атомная масса(молярная масса)1,00794 а. е. м. (г/моль),Электронная конфигурация1s1,Радиус атома53 пм.
Химические свойства
Ковалентный радиус32 пм, Радиус иона54 (−1 e) пм, Электроотрицательность2,20 [1] (шкала Полинга),Степени окисления1,0, −1, Энергия ионизации(первый электрон)1311,3 кДж/моль (эВ),
Термодинамические свойства простого вещества
Плотность (при н. у.)0,0000899 (при 273K (0 °C)) г/см³, Температура плавления14,01 K, Температура кипения20,28 K, Теплота плавления0,117 кДж/моль, Теплота испарения0,904 кДж/моль, Молярная теплоёмкость14,235[2] Дж/(K·моль), Молярный объём14,1 см³/моль.
Кристаллическая решётка простого вещества
Структура решётки гексагональная
Параметры решётки a=3,780 c=6,167 Å, Отношение c/a1,631, Температура Дебая110 K,
Прочие характеристики
Теплопроводность(300 K) 0,1815 Вт/(м·К)
Водоро́д-первый элемент периодической системы элементов; обозначается символом H. Название представляет собой кальку с латинского: лат. Hydrogenium (от др.-греч. ὕδωρ-«вода» и γεννάω-«рождаю»)-«порождающий воду». Широко распространён в природе. Катион (и ядро) самого распространённого изотопа водорода 1H-протон.
Три изотопа водорода имеют собственные названия: 1H-протий (Н), 2H-дейтерий (D) и 3H-тритий (радиоактивен) (T).
Простое вещество водород-H2-лёгкий бесцветный газ. В смеси с воздухом или кислородом горюч и взрывоопасен. Нетоксичен[2]. Растворим в этаноле и ряде металлов: железе, никеле, палладии, платине.
Получение
Основная статья: Производство водорода
Промышленные способы получения простых веществ зависят от того, в каком виде соответствующий элемент находится в природе, то есть что может быть сырьём для его получения. Так, кислород, имеющийся в свободном состоянии, получают физическим способом-выделением из жидкого воздуха. Водород же практически весь находится в виде соединений, поэтому для его получения применяют химические методы. В частности, могут быть использованы реакции разложения. Одним из способов получения водорода служит реакция разложения воды электрическим током.
Основной промышленный способ получения водорода-реакция с водой метана, который входит в состав природного газа. Она проводится при высокой температуре:СН4 + 2Н2O = CO2↑ + 4Н2 −165 кДж
Один из лабораторных способов получения водорода, который иногда применяется и в промышленности,-разложение воды электротоком.
Обычно в лаборатории водород получают взаимодействием цинка с соляной кислотой.
В промышленности
1.Электролиз водных растворов солей:
2NaCl + 2H2O → H2↑ + 2NaOH + Cl2
2.Пропускание паров воды над раскаленным коксом при температуре около 1000 °C:
H2O + C ⇄ H2 + CO
3.Из природного газа.
Конверсия с водяным паром:
CH4 + H2O ⇄ CO + 3H2 (1000 °C)
Каталитическое окисление кислородом:2CH4 + O2 ⇄ 2CO + 4H2
4. Крекинг и риформинг углеводородов в процессе переработки нефти.
В лаборатории
1.Действие разбавленных кислот на металлы. Для проведения такой реакции чаще всего используют цинк и разбавленную соляную кислоту:Zn + 2HCl → ZnCl2 + H2↑
2.Взаимодействие кальция с водой:Ca + 2H2O → Ca(OH)2 + H2↑
3.Гидролиз гидридов:NaH + H2O → NaOH + H2↑
4.Действие щелочей на цинк или алюминий:
2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2↑
Zn + 2KOH + 2H2O → K2[Zn(OH)4] + H2↑
5.С помощью электролиза. При электролизе водных растворов щелочей или кислот на катоде происходит выделение водорода, например:2H3O+ + 2e− → H2↑ + 2H2O
Физические свойства: Водород-самый лёгкий газ, он легче воздуха в 14,5 раз. Очевидно, что чем меньше масса молекул, тем выше их скорость при одной и той же температуре. Как самые лёгкие, молекулы водорода движутся быстрее молекул любого другого газа и тем самым быстрее могут передавать теплоту от одного тела к другому. Отсюда следует, что водород обладает самой высокой теплопроводностью среди газообразных веществ. Его теплопроводность примерно в семь раз выше теплопроводности воздуха.
Молекула водорода двухатомна-Н2. При нормальных условиях-это газ без цвета, запаха и вкуса. Плотность 0,08987 г/л (н.у.), температура кипения −252,76 °C, удельная теплота сгорания 120.9×106 Дж/кг, малорастворим в воде-18,8 мл/л. Водород хорошо растворим во многих металлах (Ni, Pt, Pd и др.), особенно в палладии (850 объёмов на 1 объём Pd). С растворимостью водорода в металлах связана его способность диффундировать через них; диффузия через углеродистый сплав (например, сталь) иногда сопровождается разрушением сплава вследствие взаимодействия водорода с углеродом (так называемая декарбонизация). Практически не растворим в серебре.
Жидкий водород существует в очень узком интервале температур от −252,76 до −259,2 °C. Это бесцветная жидкость, очень лёгкая (плотность при −253 °C 0,0708 г/см³) и текучая (вязкость при −253 °C 13,8 спуаз). Критические параметры водорода очень низкие: температура −240,2 °C и давление 12,8 атм. Этим объясняются трудности при ожижении водорода. В жидком состоянии равновесный водород состоит из 99,79 % пара-Н2, 0,21 % орто-Н2.
Твердый водород, температура плавления −259,2 °C, плотность 0,0807 г/см³ (при −262 °C)-снегоподобная масса, кристаллы гексогональной сингонии, пространственная группа P6/mmc, параметры ячейки a=3,75 c=6,12. При высоком давлении водород переходит в металлическое состояние.
Молекулярный водород существует в двух спиновых формах (модификациях)-в виде орто- и параводорода. В молекуле ортоводорода o-H2 (т. пл. −259,10 °C, т. кип. −252,56 °C) ядерные спины направлены одинаково (параллельны), а у параводорода p-H2 (т. пл. −259,32 °C, т. кип. −252,89 °C)- противоположно друг другу (антипараллельны). Равновесная смесь o-H2 и p-H2 при заданной температуре называется равновесный водород e-H2.
Равновесная мольная концентрация пара-водорода
Разделить модификации водорода можно адсорбцией на активном угле при температуре жидкого азота. При очень низких температурах равновесие между ортоводородом и параводородом почти нацело сдвинуто в сторону последнего. При 80 К соотношение форм приблизительно 1:1. Десорбированный параводород при нагревании превращается в ортоводород вплоть до образования равновесной при комнатной температуре смеси (орто-пара: 75:25). Без катализатора превращение происходит медленно (в условиях межзвёздной среды — с характерными временами вплоть до космологических), что даёт возможность изучить свойства отдельных модификаций.
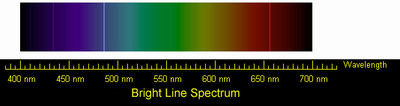 Спектр
излучения водорода
Спектр
излучения водорода
 Эмиссионный
спектр водорода
Эмиссионный
спектр водорода
Изотопы
Водород встречается в виде трёх изотопов, которые имеют индивидуальные названия: 1H — протий (Н), 2Н — дейтерий (D), 3Н — тритий (T; радиоактивный).
Протий и дейтерий являются стабильными изотопами с массовыми числами 1 и 2. Содержание их в природе соответственно составляет 99,9885 ± 0,0070 % и 0,0115 ± 0,0070 %[3]. Это соотношение может незначительно меняться в зависимости от источника и способа получения водорода.
Изотоп водорода 3Н (тритий) нестабилен. Его период полураспада составляет 12,32 лет[3]. Тритий содержится в природе в очень малых количествах.
В литературе[3] также приводятся данные об изотопах водорода с массовыми числами 4—7 и периодами полураспада 10−22—10−23 с.
Природный водород состоит из молекул H2 и HD (дейтероводород) в соотношении 3200:1. Содержание чистого дейтерийного водорода D2 ещё меньше. Отношение концентраций HD и D2, примерно, 6400:1.
Из всех изотопов химических элементов физические и химические свойства изотопов водорода отличаются друг от друга наиболее сильно. Это связано с наибольшим относительным изменением масс атомов[4].
Температура плавления,K Температура кипения,K Тройная точка,K / kPa Критическая точка,K / kPa Плотность жидкий / газ,кг/м³
H2 13,96 20,39 13,96 / 7,3 32,98 / 1,31 70,811 / 1,316
HD 16,65 22,13 16,6 / 12,8 35,91 / 1,48 114,0 / 1,802
HT 22,92 17,63 / 17,7 37,13 / 1,57 158,62 / 2,31
D2 18,65 23,67 18,73 / 17,1 38,35 / 1,67 162,50 / 2,23
DT 24.38 19,71 / 19,4 39,42 / 1,77 211,54 / 2,694
T2 20,63 25,04 20,62 / 21,6 40,44 / 1,85 260,17 / 3,136
Дейтерий и тритий также имеют орто- и парамодификации: p-D2, o-D2, p-T2, o-T2. Гетероизотопный водород (HD, HT, DT) не имеют орто- и парамодификаций.
Химические свойства
Молекулы водорода Н2 довольно прочны, и для того, чтобы водород мог вступить в реакцию, должна быть затрачена большая энергия:Н2 = 2Н − 432 кДж
Поэтому при обычных температурах водород реагирует только с очень активными металлами, например с кальцием, образуя гидрид кальция:Ca + Н2 = СаН2
и с единственным неметаллом-фтором, образуя фтороводород:F2 + H2 = 2HF
С большинством же металлов и неметаллов водород реагирует при повышенной температуре или при другом воздействии, например при освещении:О2 + 2Н2 = 2Н2О
Он может «отнимать» кислород от некоторых оксидов, например: CuO + Н2 = Cu + Н2O
Записанное уравнение отражает восстановительные свойства водорода.N2 + 3H2 → 2NH3
С галогенами образует галогеноводороды:
F2 + H2 → 2HF, реакция протекает со взрывом в темноте и при любой температуре,
Cl2 + H2 → 2HCl, реакция протекает со взрывом, только на свету.
С сажей взаимодействует при сильном нагревании: C + 2H2 → CH4
Взаимодействие со щелочными и щёлочноземельными металлами
При взаимодействии с активными металлами водород образует гидриды:
2Na + H2 → 2NaH
Ca + H2 → CaH2
Mg + H2 → MgH2
Гидриды -солеобразные, твёрдые вещества, легко гидролизуются:CaH2 + 2H2O → Ca(OH)2 + 2H2↑
Взаимодействие с оксидами металлов (как правило, d-элементов)
Оксиды восстанавливаются до металлов:
CuO + H2 → Cu + H2O
Fe2O3 + 3H2 → 2Fe + 3H2O
WO3 + 3H2 → W + 3H2O
Интересные факты
Водород — самое распространённое вещество во Вселенной (примерно 90 % всех атомов во вселенной)[8].
Водород — самый лёгкий газ. Масса 1 литра водорода в газообразном состоянии при нормальных условиях составляет всего 0,08988 грамм[8].
Хорватское название водорода — Vodik, ввел в употребление филолог Богослав Шулек.
51пероксид водорода
Перокси́д водоро́да (перекись водорода), H2O2 — простейший представитель пероксидов. Бесцветная жидкость с «металлическим» вкусом, неограниченно растворимая в воде, спирте и эфире. Концентрированные водные растворы взрывоопасны. Пероксид водорода является хорошим растворителем. Из воды выделяется в виде неустойчивого кристаллогидрата H2O2•2H2O.
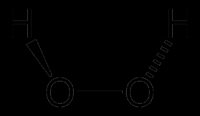
Молекула пероксида водорода имеет следующее строение: ………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………
Получение Пероксид водорода получаются в промышленности по реакции с участием органических веществ, в частности, каталитическим окислением изопропилового спирта: (CH3)2СН(ОН) + O2 → CH3C(O)CH3 + H2O2
Ценным побочным продуктом этой реакции является ацетон.
В лабораторных условиях для получения пероксида водорода используют реакцию
BaO2 + H2SO4 → H2O2 + BaSO4
Концентрирование и очистку пероксида водорода проводят осторожной перегонкой.
Химические свойства
Разлагается на кислород и воду при нагревании, под действием ультрафиолетового излучения, а также в присутствии ионов переходных металлов и серебра: 2Н2O2 → 2H2O + O2
Однако очень чистый пероксид водорода устойчив.
Пероксид водорода проявляет слабые кислотные свойства (К = 1,4·10-12). При действии концентрированного раствора Н2O2 на гидроксиды в ряде случаев можно выделить пероксиды металлов (Li2O2, MgO2 и др.): Н2O2 + 2NaOH → Na2O2 + 2H2O
Пероксидная группа -O-O- входит в состав многих веществ. Такие вещества называют пероксидами, или пероксидными соединениями. К ним относятся пероксиды металлов (Na2O2, BaO2 и др.), которые можно рассматривать как соли пероксида водорода. Кислоты, содержащие пероксидную группу, называют пероксокислотами, например, пероксомонофосфорная H3PO5 и пероксидосерная H2S2O8 кислоты.
Окислительно-восстановительные свойства
Пероксид водорода обладает окислительными, а также восстановительными свойствами. Он окисляет нитриты в нитраты, выделяет иод из иодидов металлов, расщепляет ненасыщенные соединения по месту двойных связей. Пероксид водорода восстанавливает соли золота и серебра, а также кислород при реакции с водным раствором перманганата калия в кислой среде.
При восстановлении Н2O2 образуется Н2O или ОН-, например: Н2О2 + 2КI + Н2SO4 = I2 + K2SO4 + 2H2O
При действии сильных окислителей H2O2 проявляет восстановительные свойства, выделяя свободный кислород: O22- — 2e- → O2
Реакцию KMnO4 с Н2O2 используют в химическом анализе для определения содержания Н2O2: 5H2O2 + 2KMnO4 + 3H2SO4</sup> → 5O2 + 2MnSO4 + K2SO4 + 8H2O
Окисление органических соединений пероксидом водорода (например, сульфидов и тиолов) целесообразно проводить в среде уксусной кислоты.
Биологические свойства
Перекись водорода относится к реактивным формам кислорода и при повышенном образовании в клетке вызывает оксидативный стресс. Некоторые ферменты, например глюкозоксидаза, образуют в ходе окислительно-восстановительной реакции пероксид водорода, который может играть защитную роль в качестве бактерицидного агента. В клетках млекопитающих нет ферментов, которые бы восстанавливали кислород до перекиси водорода. Однако несколько ферментных систем (ксантиноксидаза, НАД(Ф)H-оксидаза, циклоксигеназа и др.) продуцируют супероксид, который спонтанно или под действием супероксиддисмутазы превращается в перекись водорода.
Структура
Общие: Систематическое наименование Пероксид водорода Химическая формула H2O2 Отн. молек. масса 34,01 а. е. м. Молярная масса 34,01 г/моль Физические свойства Состояние (ст. усл.) жидкость Плотность 1.4 г/см³ Термические свойства Температура плавления −0,432 °C Температура кипения 150,2 °C Энтальпия образования (ст. усл.) -136.11 кДж/моль Химические свойства pKa 11.65 Растворимость в воде неограниченная г/100 мл Классификация Рег. номер CAS 7722-84-1 SMILES OO Регистрационный номер EC 231-765-0
50Вода
Вода́ (оксид водорода) — химическое вещество в виде прозрачной жидкости, не имеющей цвета (в малом объёме), запаха и вкуса (при нормальных условиях).
Химическая формула: Н2O.
В твёрдом состоянии называется льдом или снегом, а в газообразном — водяным паром. Около 71 % поверхности Земли покрыто водой (океаны, моря, озёра, реки, лёд).
Является хорошим сильнополярным растворителем. В природных условиях всегда содержит растворённые вещества (соли, газы).Вода имеет ключевое значение в создании и поддержании жизни на Земле, в химическом строении живых организмов, в формировании климата и погоды.
