- •Контрольное тестирование по физике
- •Де n1. Механика.
- •1. Кинематика поступательного и вращательного движения
- •2. Динамика поступательного движения
- •3. Динамика вращательного движения
- •4. Работа. Энергия
- •5. Законы сохранения в механике
- •6. Элементы специальной теории относительности
- •Де n2. Молекулярная (статистическая) физика и термодинамика.
- •7. Средняя энергия молекул
- •8. Распределения Максвелла и Больцмана
- •9. Первое начало термодинамики. Работа при изопроцессах
- •10. Второе начало термодинамики. Энтропия
- •Де n3. Электричество и магнетизм.
- •11. Электростатическое поле в вакууме
- •12. Законы постоянного тока
- •13. Магнитостатика
- •14. Электрические и магнитные свойства вещества
- •15. Явление электромагнитной индукции
- •16. Уравнения Максвелла
- •Де n4. Механические и электромагнитные колебания и волны.
- •17. Свободные и вынужденные колебания
- •18. Сложение гармонических колебаний
- •19. Волны. Уравнение волны
- •20. Энергия волны. Перенос энергии волной
- •Де n5. Волновая и квантовая оптика.
- •21. Интерференция и дифракция света
- •22. Поляризация и дисперсия света
- •23. Эффект Комптона. Световое давление
- •24. Тепловое излучение. Фотоэффект
- •Де n6. Квантовая физика и физика атома.
- •25. Дуализм свойств микрочастиц. Соотношение неопределенностей Гейзенберга
- •26. Спектр атома водорода. Правило отбора
- •27. Уравнение Шредингера (общие свойства)
- •28. Уравнение Шредингера (конкретные ситуации)
- •Де n7. Элементы ядерной физики и физики элементарных частиц.
- •29. Фундаментальные взаимодействия
- •30. Ядро. Элементарные частицы
- •31. Ядерные реакции.
- •32.Законы сохранения в ядерных реакциях
8. Распределения Максвелла и Больцмана
В трех одинаковых
сосудах при равных условиях находится
одинаковое количество водорода, гелия
и азота
 На
рисунке представлены графики функций
распределения молекул идеального газа
по скоростям (распределение Максвелла),
где
На
рисунке представлены графики функций
распределения молекул идеального газа
по скоростям (распределение Максвелла),
где
![]() –
доля молекул, скорости которых заключены
в интервале скоростей от
–
доля молекул, скорости которых заключены
в интервале скоростей от
![]() до
до
![]() в
расчете на единицу этого интервала.
в
расчете на единицу этого интервала.
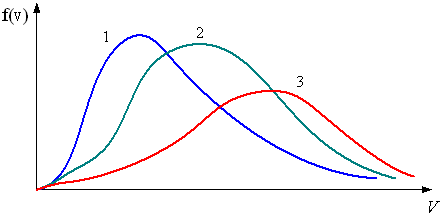 Для
этих функций верными являются утверждения,
что …
Для
этих функций верными являются утверждения,
что …
|
|
|
|
кривая 1 соответствует распределению по скоростям молекул азота |
|
|
|
|
кривая 3 соответствует распределению по скоростям молекул водорода |
|
|
|
|
кривая 1 соответствует распределению по скоростям молекул гелия |
|
|
|
|
кривая 2 соответствует распределению по скоростям молекул азота |
Решение:
Функция
Максвелла имеет вид
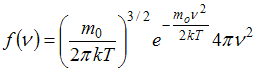 .
Полная
вероятность равна:
.
Полная
вероятность равна: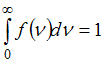 ,
то есть площадь, ограниченная кривой
распределения Максвелла, равна единице
и при изменении температуры не
изменяется. Из формулы наиболее вероятной
скорости
,
то есть площадь, ограниченная кривой
распределения Максвелла, равна единице
и при изменении температуры не
изменяется. Из формулы наиболее вероятной
скорости
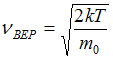 ,
при которой функция
,
при которой функция
![]() максимальна,
следует, что при повышении температуры
максимум функции сместится вправо,
следовательно, высота максимума
уменьшится. Если сравнивать распределения
Максвелла по скоростям различных газов
при одной и той же температуре, то при
увеличении массы молекулы газа максимум
функции сместится влево, следовательно,
высота максимума увеличится. Наибольшая
масса молекул у азота, меньше у гелия и
еще меньше у водорода.
максимальна,
следует, что при повышении температуры
максимум функции сместится вправо,
следовательно, высота максимума
уменьшится. Если сравнивать распределения
Максвелла по скоростям различных газов
при одной и той же температуре, то при
увеличении массы молекулы газа максимум
функции сместится влево, следовательно,
высота максимума увеличится. Наибольшая
масса молекул у азота, меньше у гелия и
еще меньше у водорода.
|
4. На
рисунке представлены графики функции
распределения молекул идеального
газа по скоростям (распределение
Максвелла), где
|
|
|
|
распределение 1 соответствует газу, имеющему большую массу молекул |
|
|
распределение 3 соответствует газу, имеющему большую температуру |
|
|
распределение 1 соответствует газу, имеющему меньшую массу молекул |
|
|
распределение 3 соответствует газу, имеющему меньшую температуру |
Решение: Функция Максвелла имеет
вид:
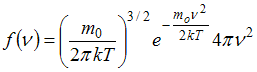 .
Полная вероятность равна:
.
Полная вероятность равна: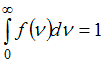 , то есть площадь, ограниченная кривой
распределения Максвелла, равна единице
и при изменении температуры не
изменяется. Из формулы наиболее вероятной
скорости
, то есть площадь, ограниченная кривой
распределения Максвелла, равна единице
и при изменении температуры не
изменяется. Из формулы наиболее вероятной
скорости
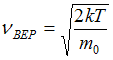 , при которой функция
, при которой функция
![]() максимальна, следует, что при повышении
температуры максимум функции сместится
вправо, следовательно, высота максимума
уменьшится. Если сравнивать распределения
Максвелла по скоростям различных газов
при одной и той же температуре, то при
увеличении массы молекулы газа максимум
функции сместится влево, следовательно,
высота максимума увеличится
максимальна, следует, что при повышении
температуры максимум функции сместится
вправо, следовательно, высота максимума
уменьшится. Если сравнивать распределения
Максвелла по скоростям различных газов
при одной и той же температуре, то при
увеличении массы молекулы газа максимум
функции сместится влево, следовательно,
высота максимума увеличится
5. На рисунке представлен график функции
распределения молекул идеального газа
по скоростям (распределение Максвелла),
где
![]() –
доля молекул, скорости которых заключены
в интервале скоростей от
–
доля молекул, скорости которых заключены
в интервале скоростей от
![]() до
до
![]() в
расчете на единицу этого интервала.
Д
в
расчете на единицу этого интервала.
Д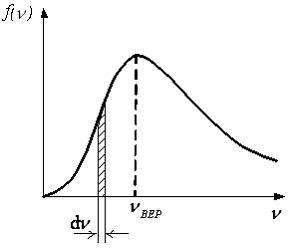 ля
этой функции неверным является
утверждение, что
ля
этой функции неверным является
утверждение, что
|
|
при понижении температуры величина максимума функции уменьшается |
|
|
при понижении температуры площадь под кривой уменьшается |
|
|
с ростом температуры наиболее вероятная скорость молекул увеличивается |
|
|
положение максимума кривой зависит не только от температуры, но и от природы газа |
Решение: Полная вероятность равна: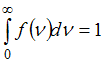 ,
то есть площадь, ограниченная кривой
распределения Максвелла, равна единице
и при изменении температуры не
изменяется. Из формулы наиболее вероятной
скорости
,
то есть площадь, ограниченная кривой
распределения Максвелла, равна единице
и при изменении температуры не
изменяется. Из формулы наиболее вероятной
скорости
 ,
при которой функция
,
при которой функция
![]() максимальна,
следует, что при повышении температуры
максимум функции сместится вправо,
следовательно, высота максимума
уменьшится.
максимальна,
следует, что при повышении температуры
максимум функции сместится вправо,
следовательно, высота максимума
уменьшится.
6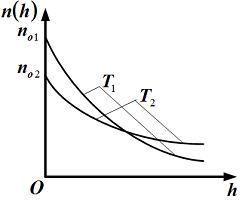 .
На рисунке представлены графики функций
распределения молекул идеального газа
.
На рисунке представлены графики функций
распределения молекул идеального газа
![]() во
внешнем однородном поле силы тяжести
от высоты
во
внешнем однородном поле силы тяжести
от высоты
![]() для
двух разных температур –
для
двух разных температур – ![]() (распределение
Больцмана).
Для этих функций верным
является утверждение, что
(распределение
Больцмана).
Для этих функций верным
является утверждение, что
|
|
температура
|
|
|
концентрация
молекул газа на «нулевом уровне»
|
|
|
температура
|
|
|
концентрация
молекул газа на «нулевом уровне»
|
Решение: Зависимость концентрации
молекул идеального газа от высоты
![]() для
некоторой температуры
для
некоторой температуры
![]() определяется
распределением Больцмана:
определяется
распределением Больцмана:
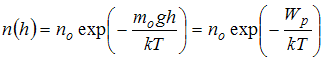 ,
где
,
где
![]() концентрация
молекул на высоте
концентрация
молекул на высоте
![]() ,
,
![]() масса
молекулы,
масса
молекулы,
![]() ускорение
свободного падения,
ускорение
свободного падения,
![]() постоянная
Больцмана. Из формулы следует, что при
постоянной температуре концентрация
газа больше там, где меньше потенциальная
энергия его молекул
постоянная
Больцмана. Из формулы следует, что при
постоянной температуре концентрация
газа больше там, где меньше потенциальная
энергия его молекул
![]() ,
и уменьшается с высотой по экспоненциальному
закону тем медленнее, чем больше
температура:
,
и уменьшается с высотой по экспоненциальному
закону тем медленнее, чем больше
температура:
![]() .
С повышением температуры из-за увеличения
энергии хаотического теплового движения
молекулы более равномерно распределяются
по высоте, и поэтому концентрация молекул
газа на «нулевом уровне»
.
С повышением температуры из-за увеличения
энергии хаотического теплового движения
молекулы более равномерно распределяются
по высоте, и поэтому концентрация молекул
газа на «нулевом уровне»
![]() уменьшается,
а на высоте
уменьшается,
а на высоте
![]() увеличивается.
увеличивается.
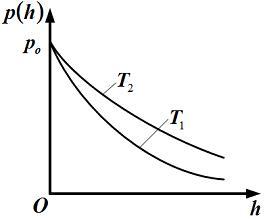
7. Зависимости давления
![]() идеального
газа во внешнем однородном поле силы
тяжести от высоты
идеального
газа во внешнем однородном поле силы
тяжести от высоты
![]() для
двух разных температур определяются
барометрической формулой и представлены
на рисунке.
Для этих функций неверным
является утверждение, что …
для
двух разных температур определяются
барометрической формулой и представлены
на рисунке.
Для этих функций неверным
является утверждение, что …
|
|
температура
|
|
|
давление газа на
высоте
|
|
|
температура
|
|
|
зависимость давления идеального газа от высоты определяется не только температурой газа, но и массой молекул |
Решение: Зависимость давления
идеального газа от высоты
![]() для
некоторой температуры
для
некоторой температуры
![]() определяется
барометрической формулой:
определяется
барометрической формулой:
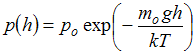 ,
где
,
где
![]() давление
на высоте
давление
на высоте ![]() ,
,
![]() масса
молекулы,
масса
молекулы,
![]() ускорение
свободного падения,
ускорение
свободного падения,
![]() постоянная
Больцмана. Из формулы следует, что при
постоянной температуре давление газа
уменьшается с высотой по экспоненциальному
закону тем медленнее, чем больше
температура
постоянная
Больцмана. Из формулы следует, что при
постоянной температуре давление газа
уменьшается с высотой по экспоненциальному
закону тем медленнее, чем больше
температура
![]() .
Давление
.
Давление
![]() определяется
весом всего газа и не меняется при
изменении температуры.
определяется
весом всего газа и не меняется при
изменении температуры.