
- •Билет № 31
- •Билет № 32
- •1. Водородные связи в органических молекулах. Участие водородных связей в формировании вторичной структуры белков и нуклеиновых кислот.
- •2. Фенолокислоты. Способы введения гидрокси- и карбоксигруппы в ароматическое ядро. Эфиры и соли салициловой кислоты, их медицинское значение. Паск.
- •3. Окислительно-восстановительные реакции моносахаридов. Биологическая роль.
- •Вопрос 3
- •1. Пространственное строение органических молекул. Конфигурации и конформации. Примеры.
- •2. Органические соединения, содержащие только связи с-с и с-н: алканы, циклоалканы. Строение и реакционная способность.
- •Реакции радикального замещения Галогенирование
- •Билет № 35
- •4. Напишите формулу карбонильного соединения, которое обесцвечивает бромную воду (в присутствии железа), нитруется и восстанавливает серебро из аммиачного раствора серебра
- •4. Напишите структурную формулу аминокислоты состава c6h13o2n, если известно, что она взаимодействует с 1 молем формалина и на титрование продукта реакции идет эквивалентно 1 моль NaOh.
- •1. Кислотности органических соединений по Бренстеду-Лоури. О-н и s-h "кислоты".
- •2. Органические соединения, содержащие карбонильную группу: альдегиды, кетоны. Строение и реакционная способность. Реакции, приводящие к образованию карбонильной группы.
- •Билет № 38
- •1. Классификация органических реакций по механизму, примеры.
- •2. Многоатомные спирты и многоатомные фенолы. Строение и реакционная способность. Качественные реакции.
- •3. Фосфолипиды. Строение, гидролиз, биологическая роль.
- •4. Осуществите превращения: 2,2-диметилпропан → 1,1-дихлор-2,2-диметилпропан → 2,2‑диметилпропаналь → гидросульфитное производное 2,2-диметилпропаналя.
- •3. Лактоза и мальтоза. Их строение и свойства, α- и β-гликозидная связь.
- •4. Составьте и назовите пептиды из аланина, серина, пролина.
Вопрос 3
САХАРОЗА
![]()
C12H20O9-OH
-OH + Cu(OH)2=сахарат меди( раствор ярко-синего цвета)
Гидролиз
=глюкоза+фруктоза
Гидролиз сахарозы сопровождается изменением знака уд. вращения р-ра и потому наз. инверсией.
4. Осуществите превращения: анилин → парасульфоанилин → белый стрептоцид.
Аналин+H2SO4=парасулфоанлин
+HNO3=Белый стрептоцид(В пара положении SO2-NH2)
БИЛЕТ № 34
1. Пространственное строение органических молекул. Конфигурации и конформации. Примеры.
Конформация молекулы определяется как любое относительное расположение атомов молекулы в пространстве, которое может быть достигнуто без нарушения целостности молекулы. Конформационные переходы возникают вследствие стереохимической нежесткости большинства молекул, когда происходит свободное вращение вокруг простых s -связей или деформация валентных углов. Важно, что одна конформация превращается в другую без разрыва существующих в молекуле валентных связей.
Конфигурация - это стереохимическая особенность данного расположения атомов в пространстве данной молекулы.
Стр 57 учебник
2. Органические соединения, содержащие только связи с-с и с-н: алканы, циклоалканы. Строение и реакционная способность.
Алканы – алифатические (ациклические) предельные углеводороды, в которых атомы углерода связаны между собой простыми (одинарными) связями в неразветвленные или разветвленные цепи.
Простейшие представители алканов:
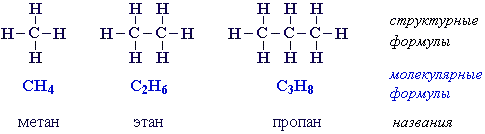
Модели молекул:
При сравнении этих соединений видно, что они отличаются друг от друга на группу -СН2- (метилен). Добавляя к пропану еще одну группу -СН2-, получим бутан С4Н10, затем алканы С5Н12, С6Н14 и т.д.
Теперь можно вывести общую формулу алканов. Число атомов углерода в ряду алканов примем за n, тогда число атомов водорода составит величину 2n+2. Следовательно, состав алканов соответствует общей формуле CnH2n+2. Поэтому часто используется такое определение:
-
Алканы - углеводороды, состав которых выражается общей формулой CnH2n+2, где n – число атомов углерода.
Реакции радикального замещения Галогенирование
Галогенирование алканов протекает по радикальному механизму.
Галогенирование — это одна из реакций замещения. Галогенирование алканов подчиняется правилу Марковникова — в первую очередь галогенируется наименее гидрированый атом углерода. Галогенирование алканов проходит поэтапно — за один этап галогенируется не более одного атома водорода.
CH4 + Cl2 → CH3Cl + HCl (хлорметан)
CH3Cl + Cl2 → CH2Cl2 + HCl (дихлорметан)
CH2Cl2 + Cl2 → CHCl3 + HCl (трихлорметан)
CHCl3 + Cl2 → CCl4 + HCl (тетрахлорметан).
Под действием света молекула хлора распадается на атомы, затем они атакуют молекулы метана, отрывая у них атом водорода, в результате этого образуются метильные радикалы СН3, которые сталкиваются с молекулами хлора, разрушая их и образуя новые радикалы.
Нитрование (реакция Коновалова)
RH + HNO3 = RNO2 + H2O
Реакции окисления
Горение
Основным химическим свойством предельных углеводородов, определяющих их использование в качестве топлива, является реакция горения. Пример:
CH4 + 2O2 → CO2 + 2H2O + Q
Каталитическое окисление
Могут образовываться спирты, альдегиды, карбоновые кислоты.
Термические превращения алканов
Разложение
Реакции разложения происходят лишь под влиянием больших температур. Повышение температуры приводит к разрыву углеродной связи и образованию свободных радикалов.
Примеры:
CH4 → C + 2H2 (t > 1000 °C)
C2H6 → 2C + 3H2
Дегидрирование
Условия протекания: 400—600 °C, катализаторы — Pt, Ni, Al2O3, Cr2O3
а)CH3-CH3 → CH2=CH2 + H2 (этан → этен)
б)CH3-CH2-CH3 → CH2=CH-CH3 + H2 (пропан → пропен)
в)CH3-CH2-CH2-CH3 → CH2=CH-CH=CH2 + H2 (бутан → бутадиен-1,3)
в')CH3-CH2-CH2-CH3 → CH2=C=CH-CH3 + H2 (бутан → бутадиен-1,2) (ЭТО - ОДНА РЕАКЦИЯ!)
Изомеризация
Под действием катализатора (например, AlCl3) происходит изомеризация алкана: например, бутан (C4H10), взаимодействуя с хлоридом алюминия (AlCl3), превращается из н-бутана в 2-метилпропан.
Циклоалканы - циклические насыщенные углеводороды, по химическим свойствам близки к предельным углеводородам.
Все атомы углерода в молекулах циклоалканов имеют sp3-гибридизацию. Однако величины углов между гибридными орбиталями в циклопентане, циклобутане и особенно в циклопропане не 109°28', а меньше из-за геометрии, поэтому малые циклы неустойчивы.
Для циклоалканов характерны все хим. Р-ии насыщенных УВ: замещения, отщепления, разложения, окисления. + р-ии присоединения
Циклопропан+Н2=пропан
3. Лактоза и мальтоза. Их строение и свойства, α- и ß-гликозидная связь.
Лактоза
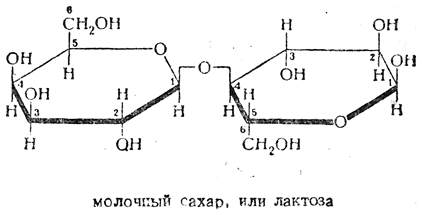
B-1, 4 – гликозидная связь
Мальтоза
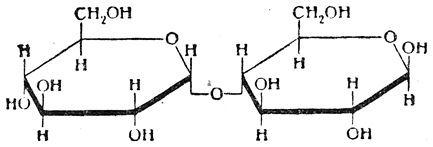
А-1,4-гликозидная связь
+ Cu(OH)2, Ag2O
4. Осуществите превращения: триолеилглицерин → тристеарилглицерин → стеарат натрия.
CH2-O-CO-C17H33
![]()
CH-O-CO-C17H33+C17H35Cooh=
![]()
CH2-O-CO-C17H33
= тристеарилглицерин+NaOH
