
1ПОНЯТИЕ ЭКОЛОГИЧЕСКОГО НОРМИРОВАНИЯ
.pdf
механическая пыль — образуется в результате измельчения продукта в ходе технологического процесса;
возгоны — образуются в результате объёмной конденсации паров веществ при охлаждении газа, пропускаемого через технологический аппарат, установку или агрегат;
летучая зола — содержащийся в дымовом газе во взвешенном состоянии несгораемый остаток топлива, образуется из его минеральных примесей при горении;
промышленная сажа — входящий в состав промышленного выброса твёрдый высокодисперсный углерод, образуется при неполном сгорании или термическом разложении углеводородов.
Основными источниками антропогенных аэрозольных загрязнений воздуха являются теплоэлектростанции , потребляющие уголь. Сжигание каменного угля, производство цемента и выплавка чугуна дают суммарный выброс пыли в атмосферу, равный 170 млн тонн в год.
Последствия
К последствиям загрязнения атмосферы Земли можно отнести парниковый эффект, кислотные дожди, смог, туман и озоновые дыры. Астрономы утверждают, что прозрачность атмосферы уменьшилась за последнее время.
Моделирование изменений климата и загрязненности воздуха, связанных с индустриальным развитием человечества, показало, что ежегодно примерно 470 000 смертей может быть связано с воздействием атмосферного озона и примерно 2 миллиона - с загрязнением воздуха высокодисперсными фракциями.
13. ПРОБЛЕМА СМОГОВ. ВИДВ СМОГОВ.
Смог (от англ. Smoky fog, буквально — «Дымовой туман») — чрезмерное загрязнение воздуха вредными веществами, выделенными в результате работы промышленных производств, транспортом и теплопроизводящими установками при определённых погодных условиях.[1]
Первоначально под смогом подразумевался дым, образованный сжиганием большого количества угля (смешение дыма и диоксида серы SO2). В 1950-х гг. в Калифорнии ХаагенСмит впервые описал новый тип смога — фотохимический, который является результатом смешения в воздухе следующих загрязняющих веществ:
оксиды азота, например, диоксид азота (продукты горения ископаемого топлива);
тропосферный (приземный) озон;
летучие органические вещества (пары́бензина, растворителей, пестицидов и других химикатов);
перекиси нитратов.

Все перечисленные химикаты обычно обладают высокой химической активностью и легко окисляются, поэтому фотохимический смог считается одной из основных проблем современной цивилизации.
Смог может образовываться практически при любых природных и климатических условиях в крупных городах и индустриальных центрах с сильным загрязнением воздуха. Наиболее вреден смог в тёплые периоды года, в солнечную безветренную погоду, когда верхние слои воздуха достаточно тёплые, чтобы останавливать вертикальную циркуляцию воздушных масс. Это явление часто встречается в городах, защищённых от ветров естественными преградами, например, холмами илигорами.
Густонаселённые города, подверженные смогу: Лондон, ЛосАнджелес, Мехико, Афины, Гонконг, Пекин, Москва и т. д.
Большое число производств в континентальной части Китая так сильно загрязнили воздух, что небоскрёбы Гонконга скрыты за плотной завесой смога.
Лондон[править | править вики-текст]
Колонна Нельсона во время великого смога1952 года.
Проблема задымления Лондона существовала уже в Средние века. В 1306
году английский король Эдуард I издал указ, запрещающий использовать уголь в городе из-за сильного дыма, создаваемого им при горении. В 1661 году английский писатель Джон Эвелин в своёмпамфлете «Fumifugium» (букв. «окуривание») предложил жечь ароматические полена вместо угля и перенести часть производств за пределы Лондона.
Смог стал неотъемлемой частью Лондона в конце XIX века и получил название «pea-souper» (то есть похожий на гороховый суп — густой и жёлтый).
От Великого смога 1952 года скончалось более 4000 человек, ещё 8000 человек погибло в последующие несколько месяцев, причём британское правительство первое время отказывалось признать факт того, что эти смерти стали последствием смога от обильного сжигания угля, приписывая их эпидемии гриппа.
В настоящее время в Лондоне такие сильные смоги стали частью прошлого из-за активной политики по защите окружающей среды.
Москва[
Смог над Москвой 7 августа 2010 г. Полдень.
В августе 2002 г. из-за торфяных пожаров в Подмосковье Москву заволокло дымом. Дым стоял несколько недель.
В июле—августе 2010 г. из-за природной аномалии, не свойственной данной местности (сильная жара 35—39 град., отсутствие больших дождей, юго-восточный слабый ветер из Средней Азии…), ситуация в Москве повторилась. Дым распространился в радиусе 100 км от Москвы. Дневная видимость снижалась до 100 метров. В воздухе чувствовался запах гари. По заявлению Санэпиднадзора, ПДК угарного газа была превышена в 6,6 раза, взвешенных веществ в 2,2 раза, концентрация углеводородов составляла 6,2 миллиграмм на кубический метр. Детальнее в статье Смог в Москве (2010).
Санкт-Петербург
8 августа 2010 г. над всем Санкт-Петербургом также заволокло дымом от подмосковных торфяных пожаров (практически впервые в таком масштабе). Ощущался запах
гари, резало глаза и першило в горле. Видимость — до 100—300 метров. И это несмотря на небольшой, но постоянный ветер днем и на сильный ветер предшествующей ночью. Температура воздуха — +36 °C.
Алматы
Смог над Алматы. Вид с гор.
На правой части снимка проглядываеттелевышка на горе Кок-тюбе
Алматы характеризуется довольно сложной экологической ситуацией из-за своего расположения в предгорной котловине. Как и имеющие подобные характеристики рельефа Афины и Лос-Анджелес, Алматы страдает из-за сильной загазованности воздуха,
дефицита строительных площадок в городской черте, стремлением населения жить ближе к центру города, а не на его окраинах, некоторой перенаселённости, массовой миграции

сельского населения в город. Над городом постоянно висит серый смог. Более 80 % загрязнения воздуха в городе приходится на автотранспорт. По последним данным, в Алматы имеются 800 тысяч автомашин.
Воздействие на здоровье
Смог является большой проблемой во многих мегаполисах мира. Он особенно опасен для детей, пожилых людей и людей с пороками сердца и лёгких, больных бронхитом, астмой, эмфиземой. Смог может стать причиной одышки, затруднения и
остановки дыхания, бессонницы, головных болей, кашля. Также он вызывает воспаление слизистых оболочек глаз, носа и гортани, снижение иммунитета. Во время смога часто повышается количество госпитализаций, рецидивов и смертей от респираторных и сердечных заболеваний.
Природные случаи
Смог также образуется при извержениях вулканов, когда в воздухе достигается высокая концентрация сернистого газа. Такой вулканический смог называется англ. vog.
Горящие леса в Индонезии создают дымку, похожую на смог, распространяющуюся на территорию Малайзии, Филиппин, Сингапура и Таиланда.
Ледяной смог (аляскинскоготипа) – сочетаниегазообразныхзагрязнителей, пылевыхчастицкристалловльда, возникающихпри замерзаниикапельтуманаипараотопительныхсистем.
Влажный смог (лондонскоготипа) - сочетаниегазообразныхзагрязнителей(восновномсернистогоангилрида), пылевыхчастиц капельтумана.
Фотохимический смог (лос-анджелескоготипа, сухой) – вторичноезагрязнениевоздуха, возникающееврезультатеразложениязагрязняющихвещест всолнечнымилучами, особенноультрафиолетовыми. Главныйядовитыйкомпонентфотохими ческогосмога– озон, дополнительнымиегосоставляющимислужатугарныйгаз, окислыазота, зотнаякислот аидр.
14. ПРОБЛЕМА КИСЛОТНЫХ ОСАЖДЕН ИЙ.
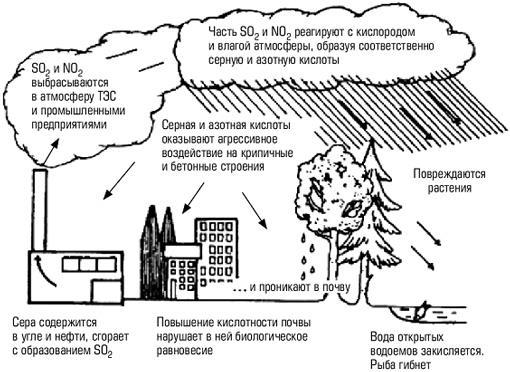
Основная причина выпадения кислотных дождей — наличие в атмосфере за счет промышленных выбросов оксидов серы и азота, хлористого водорода и других кислотообразующих соединений. В результате дождь и снег оказываются подкисленными. Образование кислотных дождей и их воздействие на окружающую среду показано на рис. 1 и
2.
Присутствие в воздухе заметных количеств, например, аммиака или ионов кальция приводит к выпадению не кислых, а щелочных осадков. Однако их также принято называть кислотными, поскольку они при попадании на почву или в водоем меняют их кислотность.
Максимальная зарегистрированная кислотность осадков в Западной Европе — с рН = 2,3, в Китае — с РН = 2,25. Автором учебного пособия на экспериментальной базе Экологического центра РАН в Подмосковье в 1990 г. был зарегистрирован дождь с рН = 2,15.
Подкисление природной среды отрицательно отражается на состоянии экосистем. В этом случае из почвы выщелачиваются не только питательные вещества, но и токсичные металлы, например свинец, алюминий и др.
В подкисленной воде увеличивается растворимость алюминия. В озерах это приводит к заболеванию и гибели рыб, к замедлению развития фитопланктона и водорослей. Кислотные дожди разрушают облицовочные материалы (мрамор, известняки др.), значительно снижают срок службы железобетонных конструкций.
Таким образом, окисление природной среды — одна из важнейших экологических проблем, требующая решения в ближайшем будущем.
Рис. 1. Образование кислотных дождей и их воздействие на окружающую среду
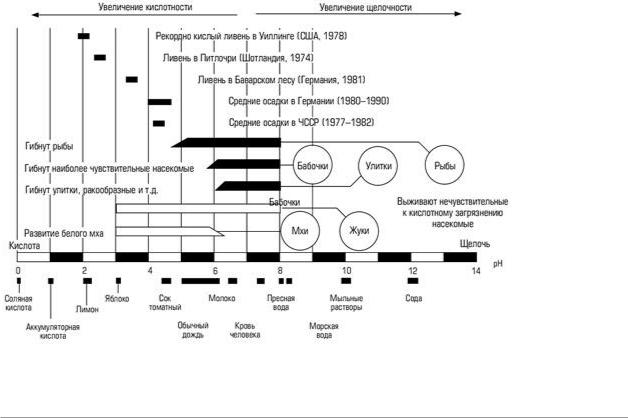
Рис. 2. Ориентировочная кислотность дождевой воды и некоторых веществ в единицах рН
ПРОБЛЕМА КИСЛОТНЫХ ОСАДКОВ
Развитие промышленности, транспорта, освоение новых источников энергии приводят к тому, что количество промышленных выбросов постоянно увеличивается. Это связано главным образом с использованием горючих ископаемых на тепловых электростанциях, промышленных предприятиях, в двигателях автомобилей и в системах отопления жилых домов.
Врезультате сжигания ископаемого топлива в атмосферу Земли поступают соединения
азота, серы, хлора, других элементов. Среди них преобладают оксиды серы — S02 и азота — NOx (N20, N02). Соединяясь с частицами воды, оксиды серы и азота образуют серную (H2SO4) и азотную (HNO3) кислоты различной концентрации.
В1883 г. шведский ученый С. Аррениус ввел в обращение два термина — «кислота» и
«основание». Он назвал кислотами вещества, которые при растворении в воде образуют свободные положительно заряженные ионы водорода (Н+), а основаниями — вещества, которые при растворении в воде образуют свободные отрицательно заряженные гидроксидионы (ОН-).
Водные растворы могут иметь рН (показатель кислотности воды, или показатель степени концентрации ионов водорода) от 0 до 14. Нейтральные растворы имеют рН 7,0, кислая среда характеризуется значениями рН меньше 7,0, щелочная — больше 7,0 (рис. 3).
В среде с рН 6,0 гибнут такие виды рыб, как лосось, форель, плотва и пресноводные креветки. При рН 5,5 погибают лонные бактерии, которые разлагают органические вещества и листья, и органический мусор начинает скапливаться на дне. Затем гибнет планктон — крошечные одноклеточные водоросли и простейшие беспозвоночные, которые составляют основу пищевой цепи водоема. Когда кислотность достигает рН 4,5, погибает вся рыба, большинство лягушек и насекомых, выживают только некоторые виды пресноводных беспозвоночных.
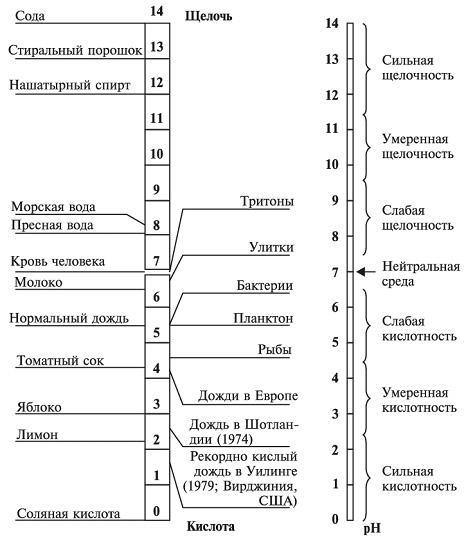
Рис. 3. Шкала кислотности (рН)
Установлено, что на долю техногенных выбросов, связанных со сжиганием ископаемого угля, приходится около 60-70 % их общего количества, на долю нефтепродуктов — 20-30 %, на остальные производственные процессы — 10 %. 40 % выбросов NOx составляют выхлопные газы автомобилей.
Последствия кислотных дождей
Атмосферные осадки, характеризующиеся сильнокислой реакцией (обычно рН<5,6), получили название кислотных (кислых) дождей. Впервые этот термин был введен британским химиком Р.Э. Смитом в 1872 г. Занимаясь вопросами загрязнения г. Манчестера, Смит доказал, что дым и пары содержат вещества, вызывающие серьезные изменения в химическом составе дождя, и что эти изменения можно заметить не только вблизи источника их выделения, но и на большом расстоянии от него. Он также обнаружил некоторые вредные последствия кислотных дождей: обесцвечивание тканей, коррозию металлических поверхностей, разрушение строительных материалов и гибель растительности.
Специалисты утверждают, что термин «кислотные дожди» недостаточно точен. Для такого типа загрязнителей лучше подходит выражение «кислотные осадки». Действительно, загрязняющие вещества могут выпадать не только в виде дождя, но и в виде снега, облаков, тумана («влажные осадки»), в виде газа и пыли («сухие осадки») в засушливый период.
Несмотря на то что сигнал тревоги прозвучал больше ста лет назад, индустриальные государства долго игнорировали опасность кислотных осадков. Но вот в 60-е гг. XX в. экологи сообщили об уменьшении косяков рыбы и даже полном ее исчезновении в некоторых озерах
Скандинавии. В 1972 г. проблема кислотных дождей была впервые поднята ученымиэкологами Швеции на Конференции ООН по окружающей среде. С этого времени опасность глобального закисления окружающей среды превратилась в одну из наиболее острых проблем, обрушившихся на человечество.
По состоянию на 1985 г. в Швеции из-за кислотных дождей серьезно пострадал рыбный промысел в 2500 озерах. В 1750 из 5000 озер Южной Норвегии полностью исчезла рыба. Исследование водоемов Баварии (Германия) показало, что в последние годы наблюдается резкое сокращение численности, а в отдельных случаях — и полное исчезновение рыбы. При изучении 17 озер в осенний период было установлено, что показатель рН воды колебался от 4,4 до 7,0. В озерах, где показатель рН составил 4,4; 5,1 и 5,8, не было поймано ни одной рыбы, а в остальных озерах обнаружены только отдельные экземпляры озерной и радужной форели и гольца.
Наряду с гибелью озер происходит деградация лесов. Хотя лесные почвы менее восприимчивы к подкислению, нежели водоемы, произрастающая на них растительность крайне негативно реагирует на увеличение кислотности. Кислые осадки в виде аэрозолей обволакивают хвою и листву деревьев, проникают в крону, стекают по стволу, накапливаются в почве. Прямой ущерб выражается в химическом ожоге растений, снижении прироста, изменении состава подпологовой растительности.
Кислотные осадки разрушают здания, трубопроводы, приводят в негодность автомобили, понижают плодородие почв и могут способствовать просачиванию токсичных металлов в водоносные слои почвы.
Разрушительному действию кислотных осадков подвергаются многие памятники мировой культуры. Так, за 25 веков мраморные статуи всемирно известного памятника архитектуры Древней Греции Акрополя постоянно подвергались воздействию ветровой эрозии и дождей. В последнее время действие кислотных осадков ускорило этот процесс. Кроме того, это сопровождается и осаждением на памятниках корки сажи в виде двуокиси серы, выделяемой промышленными предприятиями. Для соединения отдельных архитектурных элементов древние греки использовали небольшие стержни и скобы из железа, покрытые тонким слоем свинца. Тем самым они были защищены от ржавчины. Во время реставрационных работ (1896-1933) были использованы стальные детали без всяких мер предосторожности, и вследствие окисления железа под действием раствора кислот в мраморных структурах образуются обширные трещины. Ржавчина вызывает увеличение объема, и мрамор раскалывается.
Результаты исследований, проведенных по инициативе одной из комиссий ООН, свидетельствуют, что кислотные осадки оказывают губительное воздействие и на старинные витражные стекла в некоторых городах Западной Европы, что может окончательно их разрушить. Под угрозой находится более 100 000 образцов цветного стекла. Старинные витражи находились в хорошем состоянии до начала XX в. Однако за последние 30 лет процесс разрушения ускорился, и если не будут проведены необходимые реставрационные работы, через несколько десятков лет витражи могут погибнуть. Особой опасности подвергается цветное стекло, изготовленное в VIII-XVII вв. Это объясняется особенностями технологии производства.
Вещества, содержащие серу, оказывают губительное влияние также на кожаные и бумажные изделия. Старинные образцы кожи, обработанные органическими веществами, так же как и бумага, подвержены воздействию двуокиси серы: в результате они становятся ломкими. Особенно страдает бумага, изготовленная после 1750 г.
15. ПРОБЛЕМА ОЗОН РАЗРУШАЮЩИХ ВЕЩЕСТВ.
Озоноразрушающие вещества (ОРВ) – это химические соединения, в основе которых хлорированные, фторированные или бромированные углеводороды, способные вступать в реакцию с молекулами озона в стратосфере. Способность веществ разрушать озоновый слой называется озоноразрушающим потенциалом (ОРП). За единицу ОРП принята способность ХФУ-11 реагировать со стратосферным озоном.
В настоящее время оборот ОРВ строго регламентируется Монреальским протоколом по озоноразрушающим веществам.
Защитную функцию биосферы от губительных УФ-лучей Солнца выполняют верхние слои атмосферы – мезосфера и стратосфера. Эта защита основана на поглощении первичного УФ-облучения, поступающего в атмосферу с энергетическими потоками солнечных и космических лучей атомарными и молекулярными частицами этих зон. Поглощённая таким образом энергия трансформируется в неопасное видимое и ИК-излучение. Таким образом, присутствующие в мезосфере и стратосфере частицы выполняют функцию экрана, который блокирует губительное действие УФ-облучения на живые организмы.
Рассмотрим основные превращения, происходящие в верхних слоях атмосферы и обусловливающие её защитные по отношению к живым обитателям Земли свойства.
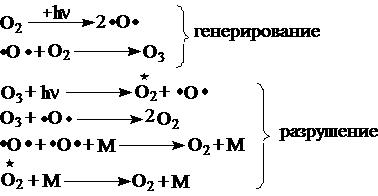
Ключевую роль в защите планеты от УФ-излучения играет озон. Сформировавшийся в стратосфере озоновый слой является результатом баланса между двумя процессами: генерированием озона и его разрушением.
В последней группе реакций первичный процесс поглощения
кванта |
света |
и |
представляет |
собой |
ключевой |
акт поглощения озоном |
коротковолновых |
фотонов, |
поглощая |
||
самые опасные из них 240-280 нм. Таким образом, в стратосфере существует цикл озона – сбалансированное образование и разложение О3.
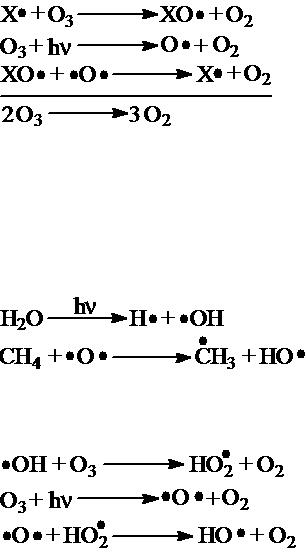
Расчётное значение толщины озонового слоя в стратосфере, сложившееся в результате баланса между естественными процессами его генерирования и гибели составляет 3 мм. Это подчёркивает хрупкость существующего баланса по отношению к факторам, которые, “вмешиваяясь” в этот баланс, могут существенно повлиять на толщину О3 и вызвать неблагоприятные экологические последствия. Отмеченные за последние годы процессы разрушения озонового слоя связывают с каталитическим действием на эти процессы оксидов водорода, азота, метана, а также фторхлоруглеводородов и других органических соединений, содержащих хлор и бром.
Действие различных озоноразрушителей интерпретируется общей схемой, предполагающей, что последние генерируют в атмосфере свободные радикалы Х, вовлекающиеся в каталитический цикл разрушения озона.
Согласно этому циклу, Х помимо прямого разрушающего действия на озон, генерирует радикалы ХО, которые являются ловушками для О, блокируя образование новых молекул озона.
Примером подобных каталитических циклов является действие метана и Н2О, генерирующих в качестве радикаларазрушителя ОН.
Образующиеся НО-радикалы вовлекаются в процесс разрушения озона в соответствии с вышеприведённой общей схемой:
