- •1.Электронное сторение атома с в основном, в возбужденным состоянии, карбоанионная, карбокатионная. Тетраэдическая можель атома с
- •2.Основные положения теории химического строения а.М. Бутлерова и ее значение для развития органической химии
- •3. Типы гибридизации орбиталей атомов углерода (sp3-, sp2-, sp- гибритизация).
- •Sp-гибридизация
- •Sp2-гибридизация
- •Sp2-гибридизация
- •9. Электронные смещения в насыщенных соединениях (индукционный эффект) и сопряженных системах(мезомерный эффект)
- •10. Классификация органических реакций по типу. Примеры.
- •11. Классификация органических реакций по механизму. Примеры.
- •12. Алканы. Изомерия, номенклатура, природные источники и методы получения. Химические свойства алканов. Механизм реакции галогенирования, сульфохлорирования, нитрования.
10. Классификация органических реакций по типу. Примеры.
По характеру химических превращений различают реакции:
Реакции замещения
CH3-CH3 + Cl2 –(hv)---- CH3-CH2Cl + HCl
C6H5CH3 + Cl2 ---500 C--- C6H5CH2Cl + HCl
Реакции присоединеия
Такие реакции характерны для органических соединений, содержащих кратные(двойные или тройные) связи. К реакциям этого типа относятся реакции присоединения галогенов, галогеноводородов и воды к алкенам и алкинам
CH3-CH=CH2 + HCl ---- CH3-CH(Cl)-CH3
Реакции отщепления (элиминирования)
Это реакции, приводящие к образованию кратных связей. При отщеплении галогеноводородов и воды наблюдается определенная селективность реакции, описываемая правилом Зайцева, согласно которому атом водорода отщепляется от того атома углерода, при котором находится меньше атомов водорода. Пример реакции
CH3-CH(Cl)-CH2-CH3 + KOH →CH3-CH=CH-CH3 + HCl
Полимеризации и поликонденсации
n(CH2=CHCl) (-CH2-CHCl)n
Окислительно-восстановительные
Наиболее интенсивная из окислительных реакций – это горение, реакция, характерная для всех классов органических соединений. При этом в зависимости от условий горения углерод окисляется до С (сажа), СО или СО2, а водород превращается в воду. Однако для химиков-органиков большой интерес представляют реакции окисления, проводимые в гораздо более мягких условиях, чем горение. Используемые окислители: растворы Br2 в воде или Cl2 в CCl4; KMnO4 в воде или разбавленной кислоте; оксид меди; свежеосажденные гидроксиды серебра (I) или меди(II).
3C2H2 + 8KMnO4 +4H2O→3HOOC-COOH + 8MnO2 + 8KOH
Этерификации (и обратной ей реакции гидролиза)
R1COOH + HOR2 H+ R1COOR2 + H2O
Циклоприсоединение
Y R Y—R
‖ + ‖ → ǀ ǀ
R Y R—Y
Y
‖ + →
R
11. Классификация органических реакций по механизму. Примеры.
Механизм реакции предполагает детальное постадийное описание химических реакций. При этом устанавливают, какие именно ковалентные связи разрываются, в каком порядке и каким путем. Столь же тщательно описывают образование новых связей в процессе реакции. Рассматривая механизм реакции, прежде всего обращают внимание на способ разрыва ковалентной связи в реагирующей молекуле. Таких способов два – гомолитический и гетеролитический.
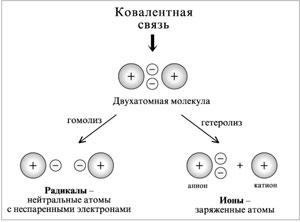
Радикальные реакции протекают путем гомолитического (радикального) разрыва ковалентной связи:
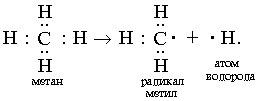
Радикальному разрыву подвергаются неполярные или малополярные ковалентные связи (С–С, N–N, С–Н) при высокой температуре или под действием света. Углерод в радикале СН3• имеет 7 внешних электронов (вместо устойчивой октетной оболочки в СН4). Радикалы неустойчивы, они стремятся захватить недостающий электрон (до пары или до октета). Один из способов образования устойчивых продуктов – димеризация (соединение двух радикалов):
СН3 •
+ • СН3 ![]() СН3 : СН3,
СН3 : СН3,
Н
• + • Н ![]() Н : Н.
Н : Н.
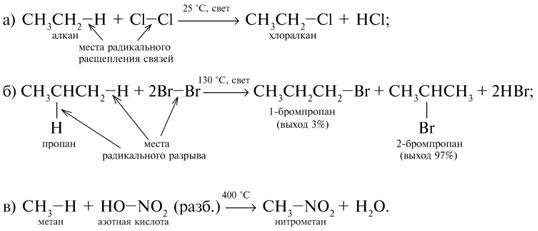
Радикальные реакции – это, например, реакции хлорирования, бромирования и нитрования алканов:
Ионные реакции протекают с гетеролитическим разрывом связи. При этом промежуточно образуются короткоживущие органические ионы – карбкатионы и карбанионы – с зарядом на атоме углерода. В ионных реакциях связывающая электронная пара не разъединяется, а целиком переходит к одному из атомов, превращая его в анион:
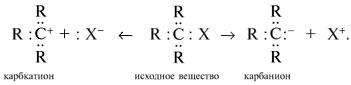
К гетеролитическому разрыву склонны сильно полярные (Н–O, С–О) и легко поляризуемые (С–Вr, С–I) связи.
Различают нуклеофильные реакции (нуклеофил – ищущий ядро, место с недостатком электронов) и электрофильные реакции (электрофил – ищущий электроны). Утверждение, что та или иная реакция является нуклеофильной или электрофильной, условно всегда относится к реагенту. Реагент – участвующее в реакции вещество с более простой структурой. Субстрат – исходное вещество с более сложной структурой. Уходящая группа – это замещаемый ион, который был связан с углеродом. Продукт реакции – новое углеродсодержащее вещество (записывается в правой части уравнения реакции).
К нуклеофильным
реагентам (нуклеофилам)
относят отрицательно заряженные ионы,
соединения с неподеленными парами
электронов, соединения с двойными
углерод-углеродными связями.
К электрофильным
реагентам (электрофилам)
относят положительно заряженные ионы,
соединения с незаполненными электронными
оболочками (АlCl3,
ВF3,
FeCl3),
cоединения с карбонильными группами,
галогены. Электрофилы – любые атом,
молекула или ион, способные присоединить
пару электронов в процессе образования
новой связи.
Движущая сила ионных
реакций – взаимодействие противоположно
заряженных ионов или фрагментов разных
молекул с частичным зарядом (![]() +
и
+
и ![]() –).
–).
Примеры ионных реакций разных типов.
Нуклеофильное замещение:
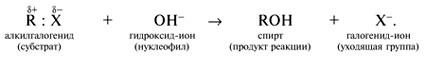
Электрофильное замещение:
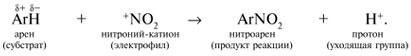
Нуклеофильное присоединение (сначала присоединяется CN–, потом Н+):
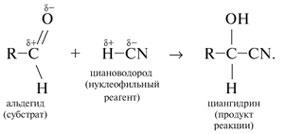
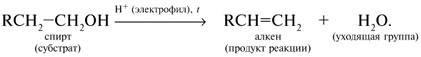
Электрофильное присоединение (сначала присоединяется Н+, потом Х–):

Элиминирование при действии нуклеофилов (оснований):

Элиминирование при действии электрофилов (кислот):