
07_Tema__SerdNedost_KoronarNedost__2014__layt
.pdfТЕМА: Недостаточность кровообращения. Сердечная недостаточность. Коронарная недостаточность _ лайт 2014
Недостаточность кровообращения, определение понятия, виды. Типовые формы патологии системы кровообращения
Введение. Сердечно-сосудистая система (ССС) является компонентом системы кровообращения в которую, помимо сердца и сосудов (т.е. ССС), входят также кровь и лимфа. Система кровообращения – одна из интегрирующих систем организма. В ней условно выделяют два звена: центральное и периферическое. Центральное кровообращение осуществляется на уровне сердца, а также крупных сосудов. Периферическое кровообращение (син.: органнотканевое) осуществляется в сосудах отдельных органов и тканей в соответствии с их функциональной активностью и уровнем пластических процессов. К периферическому кровообращению относится также кровообращение в сосудах микроциркуляторного русла.
Нарушения функции сердца, сосудистого тонуса или изменения в системе крови могут привести к недостаточности кровообращения.
Недостаточность кровообращения (НК) – патологическое состояние, при котором система кровообращения не обеспечивает потребности тканей и органов в оптимальном кровоснабжении.
Основные причины недостаточности кровообращения:
1.расстройства сердечной деятельности;
2.нарушения тонуса стенок кровеносных сосудов;
3.изменений массы циркулирующей крови и/или реологических свойств крови.
Виды недостаточности кровообращения классифицируют по критериям:
• компенсированности расстройств;
• остроте их развития и течения;
• выраженности признаков.
По компенсированности расстройства системы кровообращения подразделяют на
компенсированные (признаки расстройств кровообращения выявляются при нагрузке) и некомпенсированные (признаки нарушения кровообращения обнаруживаются в покое).
По остроте развития и течения выделяют острую (развивается в течение часов и суток) и хроническую (развивается на протяжении нескольких месяцев или лет) недостаточность кровообращения.
•Острая недостаточность кровообращения. Наиболее частые причины: инфаркт миокарда, некоторые аритмии (пароксизмальная тахикардия, мерцательная аритмия и др.), шок, острая кровопотеря.
•Хроническая недостаточность кровообращения. Причины: миокардиты, миокардиодистрофии, кардиосклероз, пороки сердца, гипер- и гипотензивные состояния, анемии, гиперволемии различного генеза.
По выраженности признаков недостаточности кровообращения выделяют:
•недостаточность кровообращения I степени (по классификации Н.Д. Стражеско и В.Х. Василенко – I стадия, начальная). Характеризуется одышкой; тахикардией; утомляемостью. Эти признаки выявляются при физической нагрузке и отсутствуют в покое.
•недостаточность кровообращения II степени (II стадия, умеренно или значительно выраженная). Те же признаки, что и в I стадии, обнаруживаются как в покое, так и особенно при физической нагрузке.
•недостаточность кровообращения III степени (III стадия, конечная). Характеризуется значительными нарушениями сердечной деятельности и гемодинамики в покое, а также развитием дистрофических и структурных изменений в органах и тканях.
Факторы риска. Показатели заболеваемости и смертности от сердечно-сосудистых заболеваний занимают первое место среди причин инвалидизации и гибели современного человека («убийца» № 1). Высокий уровень заболеваемости и летальности от болезней ССС в значительной мере определяется широкой распространённостью различных форм патологии сердца и прежде всего – ишемической болезни сердца (ИБС). В промышленно развитых странах 15–20% взрослого населения страдает ИБС.
1
Факторы риска сердечно-сосудистых заболеваний – это факторы, статистически достоверно определяющие высокий уровень заболеваемости и смертности от сердечнососудистых заболеваний. Всего известно не менее 50 факторов риска, существенно влияющих на возникновение сердечно-сосудистых заболеваний. Неуправляемые факторы риска: пол; возраст; наследственность. Управляемые факторы риска: артериальная гипертензия; гипергликемия; ожирение; эмоциональный стресс; низкая физическая активность; табакокурение; и др.
Типовые формы патологии. При анализе патологических процессов сердечно-сосудистой системы условно выделяют две группы типовых форм патологии:
•нарушения центрального кровообращения, которые обусловлены расстройством сердечной деятельности и патологией магистральных сосудов;
•расстройства периферического кровообращения, включающие и нарушения микроциркуляции.
Большая часть различных патологических процессов, поражающих сердце, относится к трём группам типовых форм патологии: коронарной недостаточности, аритмиям, сердечной недостаточности.
Сердечная недостаточность: характеристика понятия, виды и причины, её вызывающие
Сердечная недостаточность (СН) – это типовая форма патологии, при которой сердце не обеспечивает потребности органов и тканей в адекватном их кровоснабжении.
Сердечная недостаточность – это недостаточность насосной функции сердца. Сущность данной патологии заключается в том, что сердце (при данном сосудистом сопротивлении) не способно переместить в артериальное русло всю кровь, притекающую к нему по венам.
Сердечная недостаточность – это не заболевание, а синдром, развивающийся при многих болезнях (в том числе, поражающих органы и ткани, не относящиеся к сердечно-сосудистой системе).
Причины сердечной недостаточности. Две основных группы причин приводят к развитию сердечной недостаточности: оказывающие непосредственное повреждающее действие на сердце и обусловливающие функциональную перегрузку сердца.
Факторы, непосредственно повреждающие сердце:
•физические факторы: сдавление сердца (экссудатом, кровью, опухолью); действие электрического тока; механическая травма (ушибы грудной клетки, проникающие ранения).
•химические факторы: токсические соединения (например, соли тяжёлых металлов, разобщители окислительного фосфорилирования и др.); лекарственные средства в неадекватной дозировке (например, сердечные гликозиды, адреноблокаторы); дефицит кислорода и др.
•биологические факторы: высокие уровни биологически активных вещест (например,
катехоламинов, тироксина), дефицит витаминов (например, В1) и др.
Факторы, обусловливающие функциональную перегрузку сердца, подразделяются на увеличивающие преднагрузку и постнагрузку.
Увеличение преднагрузки – это перегрузка объёмом крови, притекающей к сердцу и увеличивающей давление наполнения его желудочков. Перегрузку объёмом сердце испытывает при:
•увеличении венозного возврата крови к сердцу, в частности при увеличении объёма циркулирующей крови (гиперволемия), увеличении тонуса венозных сосудов (уменьшение ёмкости венозной системы);
•пороках сердца – недостаточности его клапанов (при недостаточности аортального и митрального клапанов развивается перегрузка левого желудочка; при недостаточности клапана лёгочной артерии и трёхстворчатого клапана – перегрузка правого желудочка).
Увеличение постнагрузки – это перегрузка сопротивлением изгнанию крови из желудочков в аорту и/или лёгочную артерию. Основным фактором постнагрузки является увеличение общего периферического сосудистого сопротивления, которое наблюдается при:
•артериальных гипертензиях любого генеза (особенно при гипертонических кризах): при гипертензии большого круга кровообращения перегрузку сопротивлением испытывает левый желудочек, а при гипертензии малого круга – правый желудочек;
2
• пороках сердца – стенозах клапанных отверстий (при стенозе отверстия аорты развивается перегрузка левого желудочка, при стенозе отверстия митрального клапана – левого предсердия; при стенозе отверстия лёгочной артерии – правого желудочка, при стенозе отверстия трёхстворчатого клапана – правого предсердия).
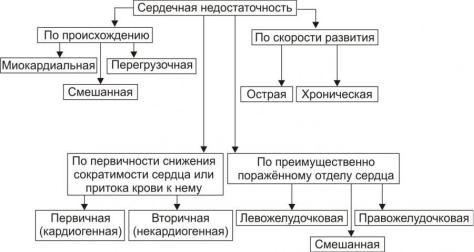
Виды сердечной недостаточности. Существует классификация видов СН в зависимости от различных признаков и факторов (рис. 1).
Рис. 1. Виды сердечной недостаточности
По происхождению СН подразделяют на следующие виды:
•миокардиальная форма, развивающаяся преимущественно в результате непосредственного повреждения миокарда.
•перегрузочная форма, возникающая преимущественно вследствие перегрузки сердца.
•смешанная форма, обусловленная сочетанием прямого повреждения миокарда и его перегрузки.
По первичности снижения сократительной функции миокарда или притока венозной крови к сердцу выделяют два вида СН:
•первичная (кардиогенная) СН развивается в результате преимущественного снижения сократительной функции сердца при близкой к нормальной величине притока венозной крови к нему (например, при ИБС, кардиосклерозе, миокардитах и др.).
•вторичная (некардиогенная) СН возникает в результате первичного преимущественного уменьшения венозного притока к сердцу при близкой к нормальной величине сократительной функции миокарда. Причины: острая массивная кровопотеря; коллапс; нарушение диастолического расслабления сердца и заполнения его камер кровью (например, при сдавлении сердца жидкостью, накапливающейся в полости перикарда – кровью, экссудатом).
По преимущественно поражённому отделу сердца:
•левожелудочковая СН – развивается в результате повреждения или перегрузки миокарда левого желудочка (например, при инфаркте миокарда). Левожелудочковая недостаточность характеризуется развитием застойных явлений в сосудах малого круга кровообращения, что может привести к развитию, например, – отёка лёгких (сердечной астмы).
•правожелудочковая СН – развивается в результате повреждения или перегрузки миокарда правого желудочка, например, при хронических заболеваниях лёгких (бронхиальной астме, эмфиземе лёгких и др.). При этом возрастает сопротивление сосудов малого круга кровообращения. Правожелудочковая недостаточность характеризуется развитием застойных явлений в большом круге кровообращения. При этом увеличивается кровенаполнение печени, появляются отёки на ногах, асцит.
•тотальная СН – при этой форме выражена и левожелудочковая и правожелудочковая сердечная недостаточность.
По скорости развития СН может быть:
3
•острой (минуты, часы), т.е. является результатом инфаркта миокарда, эмболии лёгочных сосудов, гипертонического криза, острого токсического миокардита и др.
•хронической (недели, месяцы, годы), возникающей вследствие хронической артериальной гипертензии, хронической дыхательной недостаточности, хронических пороков сердца и др.
По преимущественной недостаточности фазы сердечного цикла. В зависимости от вида нарушения функций миокарда левого желудочка (снижения силы и скорости его сокращения или нарушения скорости расслабления) левожелудочковую СН подразделяют на систолическую и диастолическую.
•Систолическая СН характеризуется снижением сократительной способности левого желудочка, что приводит к уменьшению сердечного выброса.
•Диастолическая СН характеризуется нарушением расслабления и наполнения левого желудочка. Обусловлена его гипертрофией, фиброзом или инфильтрацией (причины: ИБС, гипертрофическая кардиомиопатия, амилоидоз сердца, артериальная гипертензия, клапанные пороки сердца и др.). В результате снижения податливости и нарушения наполнения левого желудочка в нём повышается конечное диастолическое давление, что вызывает снижение сердечного выброса. Это приводит к увеличению давления в левом предсердии и малом круге кровообращения. В последующем может возникнуть правожелудочковая сердечная недостаточность.
Общие механизмы развития сердечной недостаточности
Миокардиальная форма СН характеризуется снижением развиваемого сердцем напряжения. Это проявляется снижением силы и скорости его сокращения и расслабления.
Перегрузочная форма СН формируется на фоне более или менее длительного периода его гиперфункции, которая в конечном итоге приводит к снижению силы и скорости сокращения и расслабления сердца.
В обоих случаях (при перегрузке и при повреждении миокарда) снижение сократительной функции сердца сопровождается включением механизмов компенсации этого сдвига.
Механизмы компенсации гемодинамических нарушений можно подразделить на интракардиальные (компенсаторная гиперфункция сердца, гипертрофия миокарда) и экстракардиальные (активация симпатико-адреналовой системы, активация выделительной функции почек, активация эритропоэза и др.). Такое деление в некоторой степени условно, поскольку реализация этих механизмов находится под контролем нейрогуморальных регуляторных систем организма.
Механизмы экстренной (срочной) компенсации СН.
•Повышение сократимости миокарда при его растяжении притекающей кровью
(механизм Франка-Старлинга) – увеличение напряжения, развиваемого сердцем, в ответ на возрастающее растяжение миокарда. В связи с этим его называют гетерометрическим (от греч. heteros – другой), т.е. обусловленным изменением длины сердечной мышцы.
•Увеличение сократимости миокарда при возрастании нагрузки на него – обеспечивает увеличение силы сокращений миокарда в ответ на повышенную нагрузку при неизменной длине кардиомиоцитов. Данный механизм называют гомеометрическим (от греч. homois – подобный, тот же самый), поскольку он реализуется без значительного изменения длины сердечной мышцы (феномен Анрепа).
•Компенсация острой сердечной недостаточности симпатическимим рефлекторными механизмами: увеличение частоты сердечных сокращений и увеличение силы сердечных сокращений (положительный хроноинотропный эффект катехоламинов – КА).
Симпатическая стимуляция увеличивает также и венозный возврат крови к сердцу, т.к. происходит увеличение тонуса кровеносных сосудов, особенно вен. При этом давление в правом предсердии увеличивается, благодаря чему сердце перекачивает больший, чем обычно объём крови (восстанавливается сердечный выброс левого желудочка). Увеличение давления в правом предсердии и устье полых вен «включает» рефлекс Бейнбриджа – увеличение частоты и силы сердечных сокращений.
4
Увеличение давления в правом предсердии может поддерживать нормальную величину сердечного выброса, несмотря на низкую сократительную способность миокарда. По этой причине у многих людей, особенно пожилых и старых, сердечный выброс имеет нормальную величину на фоне повышенного давления в правом предсердии, что указывает на состояние компенсированной сердечной недостаточности.
Механизмы долговременной компенсации СН. Уменьшение сердечного выброса способствует снижению почечного кровотока, что обусловливает стимуляцию ренин- ангиотензин-альдостероной системы (РААС). Увеличивается выработка ренина, что инициирует избыточную продукцию ангиотензина II, вызывающего вазоконстрикцию и задержку воды в организме. В результате этих процессов увеличивается венозный возврат к сердцу, что может полностью компенсировать снижение сократительной способности миокарда. Например, если сократительная способность сердца снижена на 40-50%, увеличение венозного возврата нередко возвращает величину сердечного выброса к нормальному уровню в условиях покоя.
Поскольку сердечный выброс стал нормальным, нормализовался и почечный диурез. Установился равновесный баланс жидкости в организме. Состояние гемодинамики стабилизировалось на фоне нормального сердечного выброса и повышенного давления крови в правом предсердии. Это будет продолжаться до тех пор, пока какой-нибудь дополнительный внешний фактор не изменит или величину сердечного выброса, или величину венозного возврата.
Отрицательное значение задержки жидкости в организме при тяжёлой сердечной недостаточности обусловлено тем, что избыток жидкости может привести к опасным последствиям: перегрузке сердца объёмом притекающей крови, что делает его сократительную функцию ещё слабее, развитие отёка органов и тканей.
Компенсаторная гиперфункция миокарда обусловливает активацию генетического аппарата кардиомиоцитов, что проявляется увеличением синтеза нуклеиновых кислот и белков, приводит к увеличению массы миокарда – гипертрофии миокарда (увеличение массы сердца за счёт увеличения размеров кардиомиоцитов). Биологическое значение: увеличенная функция миокарда выполняется его возросшей массой.
Стадии развития компенсаторной гипертрофии миокарда (Ф. Меерсон).
•Первая стадия (аварийная). Характеризуется увеличением интенсивности функционирования структур миокарда (ИФС миокарда – это механическая работа, приходящаяся на единицу массы миокарда), представляет собой компенсаторную гиперфункцию ещё не гипертрофированного сердца.
•Вторая стадия (стадия завершившейся гипертрофии). Характеризуется нормальной ИФС миокарда и соответственно нормальным уровнем энергообразования, синтеза нуклеиновых кислот
ибелков в ткани сердечной мышцы. Патологические изменения в метаболизме и структуре миокарда не выявляются (потребление кислорода, образование энергии, содержание макроэргических соединений не отличаются от нормы). Гипертрофированное сердце приспособилось к новым условиям нагрузки и в течение длительного времени компенсирует их (гемодинамические показатели в пределах нормы).
•Третья стадия (стадия декомпенсации и прогрессирующего кардиосклероза). Характеризуется метаболическими и структурными изменениями в миокарде с развитием дистрофических и склеротических процессов, что способствует появлению признаков декомпенсации и сердечной недостаточности.
Механизмы декомпенсации гипертрофированного миокарда. Гипертрофированный миокард отличается от нормального по ряду метаболических, функциональных и структурных признаков, которые, с одной стороны, позволяют ему длительное время преодолевать повышенную нагрузку, а с другой – создают предпосылки для возникновения патологических изменений. В основе декомпенсации длительно гипертрофированного миокарда лежит нарушение сбалансированности роста различных его структур, что обусловливает, в конечном счёте,
уменьшение силы и скорости сердечных сокращений, т.е. развитие сердечной недостаточности. Механизмами декомпенсации гипертрофированного миокарда являются:
•отставание роста микрососудов от увеличения массы миокарда (развитие относительной коронарной недостаточности);
5
•большее увеличение массы клеток по сравнению с их поверхностью (ухудшение обмена с внеклеточной жидкостью);
•относительная недостаточность количества митохондрий на единицу массы миокарда
(снижение энергообеспечения клеток миокарда);
•относительная недостаточность пластических процессов (дефицит энергии, недостаток субстратов);
•ионный дисбаланс (накопление в кардиомиоцитах Na+ и Ca2+, потеря К+).
•нарушение регуляторного обеспечения сердца (отставание роста нервных окончаний от роста массы миокарда).
Кардиомиоциты не способны к пролиферации, поэтому погибшие клетки замещаются соединительной тканью.
Ремоделирование миокарда – это структурные и метаболические изменения в миокарде, приводящие к изменению его размеров, формы и снижению сократительной функции сердца.
Варианты ремоделирования миокарда: гипертрофия (увеличение толщины стенки миокарда); дилатация (расширение полостей сердца); фиброз (разрастание соединительной ткани
–кардиосклероз).
Гемодинамические варианты ремоделирования миокарда
Патогенный фактор |
Исход |
Нарушение гемодинамики |
Клиническое проявление |
|
ремоделирования |
|
|
Перегрузка объёмом |
Дилатация |
Систолическая дисфункция |
Синдром малого выброса |
Перегрузка давлением |
Гипертрофия |
Диастолическая дисфункция |
Синдром застоя на путях |
|
|
|
притока в ослабленный |
|
|
|
отдел сердца |
Повреждение миокарда |
Кардиосклероз (с гипер- |
Сочетание систолической и |
Сочетание обоих синдромов |
|
трофией и/или дилата- |
диастолической дисфункции |
|
|
цией) |
|
|
Клинические формы сердечной недостаточности Острая сердечная недостаточность – внезапное нарушение насосной функции сердца,
приводящее к развитию недостаточности кровообращения, несмотря на включение компенсаторных механизмов.
Причины: заболевания, приводящие к быстрому и значительному снижению сердечного выброса (инфаркт миокарда, миокардиты, гипертензивный криз, тампонада сердца и др.).
Острая левожелудочковая СН может проявляться развитием сердечной астмы, отёка лёгких, кардиогенным шоком.
Сердечная астма (удушье, пароксизмальная ночная одышка) возникает в результате застоя крови в малом круге кровообращения при положении больного лёжа как проявление интерстициального отёка лёгких (отёк паренхимы лёгких без выхода транссудата в просвет альвеол). Клинически проявляется одышкой и кашлем без мокроты. Может развиться ортопноэ (от греч. orthos – вставший, поднявшийся и pnoe – дыхание) – одышка, при которой больной не может лежать и принимает вынужденное сидячее положение. В положении «сидя» уменьшается кровенаполнение малого круга (↓ венозный возврат к сердцу), облегчается работа сердца, улучшается самочувствие пациента.
Отёк лёгких, или альвеолярный отёк лёгких является следствием прогрессирования сердечной астмы. Характеризуется пропотеванием плазмы в просвет альвеол. У больных появляется кашель с отделением пенистой мокроты, удушье, в лёгких выслушиваются хрипы.
Кардиогенный шок развивается в результате острого снижения сердечного выброса и характеризуется значительным снижением перфузии в органах и тканях. Как правило, он возникает при обширном инфаркте миокарда на фоне множественного поражения венечных артерий. Сопровождается быстрым и выраженным снижением системного АД.
Хроническая сердечная недостаточность (ХСН): синдром, осложняющий течение ряда заболеваний. Характеризуется наличием одышки вначале при физической нагрузке, а затем и в
6
покое; быстрой утомляемостью; периферическими отёками и объективными признаками нарушения функций сердца в покое (например, аускультативными или эхокардиографическими).
Причины ХСН: ИБС, кардиомиопатии, миокардиты, токсические воздействия (например, алкоголь); инфильтративные заболевания (саркоидоз, амилоидоз), тиреотоксикоз, нарушения питания (дефицит витамина В1); перегрузка миокарда (артериальная гипертензия, пороки сердца); аритмии и др.
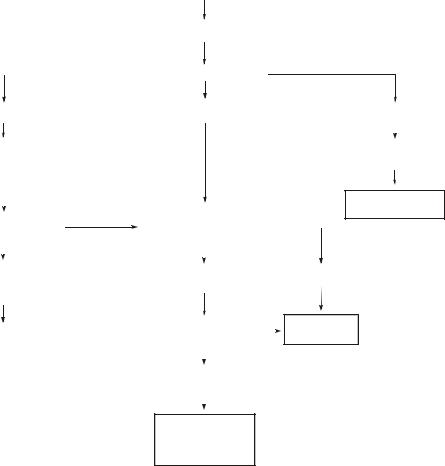
В результате действия патогенных факторов нарушается насосная функция сердца, что приводит к снижению сердечного выброса, развивается гипоперфузия органов и тканей. Наибольшее значение имеет снижение перфузии сердца, почек, периферических мышц (рис. 2).
Снижение сократительной функции миокарда
Падение сердечного выброса
Уменьшение перфузии
сердца |
|
почек |
|
мышц |
|
|
|
|
|
Стимуляция
симпатической
нервной
системы
|
|
Увеличение |
|
Периферическая |
|||
концентрации ренина, |
|||
вазоконстрикция |
|||
ангиотензина II |
|||
|
|
||
|
|
|
|
Увеличение |
Увеличение концентрации |
||
периферического |
альдостерона |
||
сопротивления |
|
||
Накопление лактата, атрофия
Утомляемость |
АДГ 
|
Задержка ионов |
Возрастание |
Na, воды |
постнагрузки |
|
на сердце |
Возрастание объёма |
|
|
|
плазмы |
Увеличение |
преднагрузки |
на сердце |
Отёки |
Рис. 2. Патогенез хронической систолической сердечной недостаточности
Уменьшение кровоснабжения сердца и развитие его недостаточности ведёт к активации симпатико-адреналовой системы и учащению ритма сердца (↑ ЧСС).
Уменьшение перфузии почек обусловливает стимуляцию ренин-ангиотензин- альдостероной системы (РААС). Увеличивается выработка ренина, что инициирует избыточную продукцию ангиотензина II.
Ангиотензин-II вызывает вазоконстрикцию, задержку воды (отёки, ↑ОЦК) и последующее увеличение преднагрузки на сердце.
Гиперволемия ведёт к раздражению механорецепторов, локализованных в устье полых вен, «включается» рефлекс Бейнбриджа, возникает рефлекторная тахикардия, что ещё больше увеличивает нагрузку на миокард и потребность сердечной мышцы в кислороде. Создается «порочный круг».
Повышение гидростатического давления в микроциркуляторном русле способствует выходу жидкой части крови в ткани и формированию отёков.
7
Снижение кровотока в периферических мышцах обусловливает накопление в них недоокисленных продуктов метаболизма и как результат – выраженную утомляемость.
Правожелудочковая систолическая сердечная недостаточность проявляется лёгочным сердцем.
Лёгочное сердце (лат. cor pulmonale) – это гипертрофия стенок и расширение просвета правого желудочка сердца в ответ на лёгочную гипертензию.
Острое лёгочное сердце – это острая правожелудочковая недостаточность, развивающаяся в результате тромбоэмболии крупных ветвей лёгочной артерии или пневмонии, возникающей на фоне хронического лёгочного сердца.
Хроническое лёгочное сердце – это хроническая правожелудочковая недостаточность, возникающая вследствие длительно существующей лёгочной гипертензии. Правый желудочек дилатирован (расширен), его стенки гипертрофированы (утолщены). Самая частая причина хронического лёгочного сердца – левожелудочковая недостаточность с застоем крови в малом круге кровообращения (например, при стенозе отверстия митрального клапана). Другие причины хронического легочного сердца, как правило, связаны с различными заболеваниями лёгких (например, хронический бронхит, хроническая обструктивная болезнь лёгких, бронхоэктатическая болезнь и др.).
Проявления правожелудочковой недостаточности. Сопровождается развитием застойных явлений в большом круге кровообращения: характерно увеличение печени (гепатомегалия, «мускатная печень»), спленомегалия, отёки нижних конечностей, асцит.
Общие принципы лечения сердечной недостаточности Этиотропная терапия направлена на уменьшение преднагрузки (↓ возврата венозной
крови к сердцу) и постнагрузки (↓ тонуса резистивных сосудов). С этой целью используют: вазодилататоры, диуретики, α-адреноблокаторы, ингибиторы ангиотензин-превращающего фермента (эналаприл и др.).
Патогенетическая терапия: повышение сократительной функции сердца; уменьшение нарушения энергообеспечения кардиомиоцитов; защита мембран и ферментов от факторов повреждения; снижение дисбаланса ионов и жидкости в миокарде; коррекция адрено- и холинергических влияний на сердце. С этой целью применяют: сердечные гликозиды (дигоксин), антигипоксанты (актовегин), антиоксиданты (витамин Е, С и др.), коронародилататоры (эуфиллин, папаверин), мембранопротекторы (эссенциальные фосфолипиды, метионин).
Коронарная недостаточность: характеристика понятия, виды, причины возникновения
Коронарная недостаточность (КН) – типовая форма патологии сердца, характеризующаяся превышением потребности миокарда в кислороде и субстратах метаболизма над их притоком по коронарным артериям.
Ведущий патогенетический фактор коронарной недостаточности – ишемия миокарда. Клинически коронарная недостаточность проявляется ишемической болезнью сердца (ИБС).
Виды коронарной недостаточности. Все разновидности коронарной недостаточности подразделяются на обратимые и необратимые (рис. 3).
Обратимые (транзиторные) нарушения коронарного кровотока клинически проявляются различными формами стенокардии и состояниями после реперфузии (реваскуляризации) миокарда.
Стенокардия (син. грудная жаба, лат. – angina pectoris; грудная боль) – это типовая форма коронарной недостаточности, характеризующаяся сильной сжимающей болью в области грудины слева вследствие ишемии миокарда. Боль часто иррадиирует в область левой лопатки и левого плеча.
Различают несколько разновидностей стенокардии.
• Стабильная стенокардия – самая частая форма стенокардии. Вызывается физической или эмоциональной нагрузкой. Обусловлена ишемией миокарда вследствие снижения коронарного кровотока до критического уровня.
8

•Нестабильная, или прогрессирующая, стенокардия также известна как предынфарктное состояние, поскольку может завершиться развитием инфаркта миокарда. Характеризуется нарастающими по частоте, длительности и тяжести эпизодами стенокардии, нередко даже в покое. Болевые приступы раз от раза становятся всё более тяжёлыми и возникают после менее интенсивной нагрузки. Эта форма стенокардии является результатом разрушения атеросклеротической бляшки и развития тромба на месте дефекта, эмболии коронарной артерии, спазма ветви венечной артерии сердца.
•Вариантная стенокардия (вазоспастическая стенокардия, или стенокардия Принцметала) возникает в покое и обусловлена спазмом венечных артерий. Приступы легко купируются приёмом вазодилататоров (например, нитроглицерина).
Повторные (даже кратковременные – до 3-8 мин) эпизоды стенокардии могут привести к формированию небольших участков некроза миокарда с последующим развитием мелкоочагового кардиосклероза.
•Состояния после реперфузии (реваскуляризации) миокарда возникает в результате возобновления коронарного кровотока (например, после аортокоронарного шунтирования или вследствие тромболизиса с помощью тромбо- и фибринолитиков).
Рис. 3. Классификация видов и форм коронарной недостаточности
Необратимые нарушения коронарного кровотока в каком-либо регионе сердца завершаются, как правило, инфарктом миокарда.
Инфаркт миокарда (от лат. infarctus – набитый, т.е. «набитый» клетками крови) – это ишемический некроз сердечной мышцы.
В механизме развития инфаркта миокарда различают стадии: ишемии, повреждения, некроза и рубцевания.
Стадия ишемия может длиться относительно долго (например, стенокардия напряжения). В основе процесса – нарушение гемодинамики миокарда. При исчерпывании компенсаторных механизмов развивается повреждение, нарушаются метаболизм и функция миокарда. Изменения могут носить обратимый характер. Некроз характеризуется необратимостью повреждения. Если инфаркт не приводит к смерти, погибший участок сердца замещается соединительной ткань (стадия рубцевания). Развивается крупноочаговый кардиосклероз.
Осложнения инфаркта миокарда: аритмии сердца; кардиогенный шок; разрыв сердца (стенки желудочка, межжелудочковой перегородки); острая аневризма сердца (выпячивание сердечной стенки, представленной некротическими тканями); образование пристеночных тромбов (в желудочках, предсердиях); перикардит; хроническая аневризма (появляется через несколько недель или даже месяцев после инфаркта, возникая обычно на месте крупных постинфарктных рубцов).
9
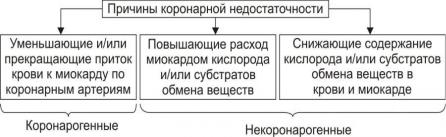
Причины коронарной недостаточности. Выделяют две основные группы причин коронарной недостаточности (рис. 4).
Коронарогенные причины – вызывающие уменьшение или полное прекращение притока крови к миокарду по коронарным артериям. Обусловливают развитие «абсолютной» коронарной недостаточности, т.е. вызванной «абсолютным» снижением доставки крови к миокарду.
Некоронарогенные причины:
•вызывающие существенное повышение расхода миокардом кислорода и субстратов метаболизма в сравнении с уровнем их притока;
•приводящие к снижению содержания кислорода и субстратов обмена веществ в крови и клетках миокарда (например, при общей гипоксии).
Коронарная недостаточность вызываемая «некоронарогенными» причинами называются «относительной». Она может развиваться как при измененных (чаще) так и неизмененных артериях сердца и при нормальном или даже повышенном (в сравнении с покоем) уровне притока крови к миокарду. Это состояние возникает при гипертоническом кризе, чрезмерной физической нагрузке, при двусторонней пневмонии и др.
Рис. 4. Этиология коронарной недостаточности
Причины абсолютной коронарной недостаточности (коронарогенные).
•Атеросклеротическое поражение коронарных артерий.
•Тромбоз коронарных артерий (чаще тромбы формируются на поверхности атеросклеротической бляшки, где нарушились структура и целостность эндотелиального слоя).
•Спазм коронарных артерий. Решающее значение в развитии коронароспазма имеют катехоламины.
•Уменьшение притока крови к сердцу и снижения в связи с этим перфузионного давления в коронарных артериях (значительная брадиили тахикардия; трепетание или фибрилляция предсердий и желудочков сердца; недостаточность аортальных клапанов; острая артериальная гипотензия; сдавление коронарных артерий сердца рубцом и др.).
Причины относительной коронарной недостаточности (некоронарогенные). 1. Увеличение потребления миокардом кислорода.
•Существенное повышение в сердце уровня кахехоламинов (например, при стрессе или
феохромоцитоме). Избыток КА в миокарде обусловливает развитие их кардиотоксического эффекта. Механизмы кардиотоксического эффекта катехоламинов:
чрезмерное повышение расхода кислорода и субстратов метаболизма миокардом за счёт положительного хроно- и инотропных эффектов;
снижение эффективности механизмов ресинтеза АТФ (КА стимулируют образование свободных радикалов, активируют процессы перекисного окисления липидов, активируют липолиз, образование ВЖК, что приводит к повреждению мембран, инактивации ферментов тканевого дыхания, гликолиза; разобщению окислительного фосфорилирования).
уменьшение (в сравнении с потребным) величины коронарного кровотока в результате укорочения диастолы (катехоламиновая тахикардия).
• Значительное увеличение работы сердца. Наиболее часто является следствием чрезмерной физической нагрузки, длительной тахикардии, острой артериальной гипертензии, выраженной гемоконцентрации, значительной гиперволемии.
10
