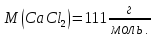- •Техніка безпеки в хімічній лабораторії
- •Заняття 1. Біогенні елементи; біологічна роль, застосування в медицині.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Характерні реакції іонів деяких макро – та мікроелементів
- •Заняття 2. Комплексоутворення в біологічних системах.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •КомплексНі сполуки
- •Заняття 3. Величини, що характеризують кількісний склад розчинів. Приготування розчинів.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Приготування розчину кобальт (іі) нітрату розбавленням більш концентрованого розчину
- •Заняття 4. Кислотно-основна рівновага в організмі. Водневий показник біологічних рідин.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Гідроліз солей
- •Заняття 5. Основи титриметричного аналізу.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Визначення молярної концентрації еквівалента натрій гідроксиду за титрованим розчином сульфатної кислоти
- •Заняття 6. Буферні системи, їх біологічна роль.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Приготування буферних розчинів і вивчення їх властивостей
- •Завдання:
- •Визначення буферної ємності ацетатного буферного розчину
- •Завдання:
- •Заняття 7. Колігативні властивості розчинів.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Визначення теплот нейтралізації
- •Заняття 9. Кінетика біохімічних реакцій.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Дослідження залежності швидкості розкладу тіосульфатної кислоти від її молярної концентрції
- •Заняття 10. Хімічна рівновага. Добуток розчинності.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Визначення нормального окисно-відновного потенціалу
- •Заняття 12. Сорбція біологічно-активних речовин. Іонний обмін. Хроматаграфія.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Адсорбція ацетатної кислоти на активованому вугіллі
- •Кількісне визначення іонів кальцію у розчині методом іонообмінної адсорбції
- •Розділення суміші барвників за допомогою методу тонкошарової хроматографії
- •Розділення суміші катіонів заліза(ііі) і купруму(іі) за допомогою адсорбційної колонкової хроматографії
- •Заняття 13. Одержання ,очистка та властивості колоїдних розчинів.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Одержання, очищення та властивості колоїдних розчинів
- •Заняття 14. Коагуляція колоїдних розчинів. Властивості розчинів біополімерів.
- •Теоретичні питання:
- •Тести та вправи до самостійної роботи:
- •Визначення порогу коагуляції
- •Визначення ізоелектричної точки (іет) альбуміну сироватки крові
- •Довідкова інформація
- •Приклад письмової роботи (Модуль 1)
- •Письмова робота
- •Приклад письмової роботи (Модуль 2)
- •Письмов робота
Тести та вправи до самостійної роботи:
1. Справжній розчин може бути системою:
а) гомогенною; б) гетерогенною; в) мікрогетерогенною.
2. Розчин, що знаходиться в динамічній рівновазі з надлишком розчиненої речовини, називається:
а) насиченим; б) ненасиченим; в) перенасиченим?
3. Молярну масу еквівалента речовини вимірюють в:
а) г; б) г/моль; в) моль/л; г) моль/кг; д) г/л.
4. Якщо
фактор еквівалентності
 ,
то для знаходження молярної маси
еквівалента речовини необхідно її
молярну масу поділити на:
,
то для знаходження молярної маси
еквівалента речовини необхідно її
молярну масу поділити на:
а) 2; б) 3; в) 4; г) 5; д) 6?
5. Рівняння, що виражає зв’язок між молярною концентрацією еквівалента і густиною розчину визначається формулою:
а) ; б)
; б) ;
;
в) ; г)
; г) .
.
6. Розчинення супроводжується:
а) збільшенням вільної енергії;
б) спочатку збільшенням, а потім зменшенням вільної енергії;
в) зменшенням вільної енергії;
г) спочатку зменшенням, а потім збільшенням вільної енергії.
7. Як буде змінюватися взаємна розчинність рідин з підвищенням температури:
а) зменшуватися; б) не змінюється; в) збільшуватися?
8. Розчинність кисню за однакової температури і парціального тиску найбільша у:
а) дистильованій воді; б) річковій воді; в) озерній воді;
г) морській воді; д) плазмі крові.
9. Якщо налити в склянку холодної води і поставити її на стіл, то через деякий час на її стінках з’являються бульбашки газу. Це пояснюється тим, що при підвищенні температури розчинність газів у воді:
а) збільшується;
б) зменшується;
в) не змінюється;
г) спочатку збільшується, а потім зменшується.
10. Як потрібно подіяти на насичений розчин кисню у воді, щоб зробити його ненасиченим:
а) підвищити температуру;
б) зменшати тиск;
в) додати сіль;
г) додати воду?
11. В якому водному розчині натрій хлориду концентрація кисню буде найменшою:
а) 0,0001моль/л; б) 0,01моль/л; в) 0,1моль/л; г) 1 моль/л?
12. Максимальна маса речовини, що здатна розчинитися за даної температури в 100г води, називається:
а) масовою концентрацією;
б)масовою часткою речовини в розчині;
в) коефіцієнтом розчинності;
г)молярною концентрацією.
13. Процес виділення твердої речовини з розчину при зниженні температури, називається:
а) кристалізацією; б) випаровуванням; в) розчиненням.
14. Відносний об’єм внутрішньоклітинної рідини з віком:
а) зменшується; б) збільшується; в) не змінюється.
15. Яким математичним рівнянням пов’язані молярна та масова концентрації речовини?
|
16. Харчова сода (натрій гідрокарбонат) входить до складу багатьох кулінарних рецептів, а також використовується для полоскання горла у вигляді 2%-го розчину. Розрахувати масу харчової соди та об’єм води, необхідні для приготування 250г такого розчину. | |
|
17. Розчин
з масовою часткою глюкози 5% в медицині
застосовують для поповнення об’єму
рідини в організмі та як джерело
легкозасвоюваного цінного поживного
матеріалу. Розрахувати масу глюкози,
введеної в організм при вливанні
250мл даного розчину. Густина розчину
| |
|
18. Водний
розчин натрій гіпохлориту
| |
|
19. Водний
розчин фурациліну з масовою часткою
0,02% застосовують зовнішньо як
антибактеріальний препарат. Який
об’єм такого розчину можна приготувати
з однієї таблетки, що містить 0,1г
фурациліну? Густина розчину
| |
|
20. В
медичній практиці часто користуються
0,9%-вим розчином натрій хлориду.
Розрахувати масу води, яку потрібно
додати до 200г розчину з масовою часткою
| |
|
21. Обчислити
масу кальцій хлориду, яку потрібно
додати до 250г розчину з масовою часткою
| |
|
22.При
опіках лугами уражену ділянку шкіри
протягом 5-10хв промивають водою, а
потім нейтралізують розчином оцтової
кислоти с масовою часткою
| |
|
23. В
медичній практиці використовуються
3%-вий та 30%-вий розчини пероксиду
водню. Який об’єм води потрібно додати
до 5мл розчину з масовою часткою
| |
|
24. Яка
маса калій дихромату необхідна для
приготування 500мл розчину з молярною
концентрацією еквівалента
| |
|
25. Яка
маса калій гідроксиду необхідна для
приготування 500мл розчину з молярною
концентрацією
| |
|
26.
Яка маса фосфатної кислоти міститься
в 300мл розчину з молярною концентрацією
еквівалента
| |
|
27.Розрахувати
масову частку хлорної кислоти в
розчині, якщо молярна концентрація
| |
|
28. Розрахувати
молярну концентрацію розчину нітратної
кислоти з масовою часткою
| |
|
29. Розрахувати
молярну концентрацію еквівалента
фосфатної кислоти
| |
|
30.Для
отримання нашатирного спирту в 500г
води розчинили 54,75г амоніаку. Обчислити
масову частку, масову концентрацію
та молярну концентрацію
| |
|
31. Розчин
кальцій хлориду з масовою часткою
| |
|
|
|
ЛАБОРАТОРНА РОБОТА №3

 .
. відзначається потужною бактерицидною
активністю та окислювальною дією і
використовується в стоматології для
медикаментозної обробки кореневих
каналів і дезінфекції порожнини зуба.
Обчислити масу натрій гіпохлориту,
що міститься в 30мл розчину з масовою
часткою
відзначається потужною бактерицидною
активністю та окислювальною дією і
використовується в стоматології для
медикаментозної обробки кореневих
каналів і дезінфекції порожнини зуба.
Обчислити масу натрій гіпохлориту,
що міститься в 30мл розчину з масовою
часткою
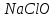 10%.Густина
розчину
10%.Густина
розчину
 .
.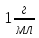 .
.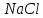 5%,
щоб отримати розчин з масовою часткою
0,9%.
5%,
щоб отримати розчин з масовою часткою
0,9%.  3%,
щоб отримати розчин з масовою часткою
3%,
щоб отримати розчин з масовою часткою
 10%.
10%.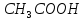 1%. Який об’єм оцтової есенції з масовою
часткою
1%. Який об’єм оцтової есенції з масовою
часткою 80% (густина есенції
80% (густина есенції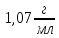 )
потрібно взяти для приготування 1л
1%-го розчину оцтової кислоти (густина
розчину
)
потрібно взяти для приготування 1л
1%-го розчину оцтової кислоти (густина
розчину
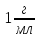 )?
)?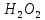 30%, щоб приготувати розчин з масовою
часткою
30%, щоб приготувати розчин з масовою
часткою 3%? Густина розчинів
3%? Густина розчинів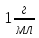 .
. ?
?

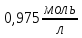 ?
?
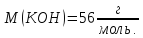
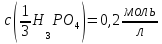 ?
?
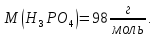
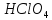
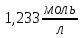 .
Густина розчину
.
Густина розчину
 ;
;
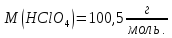
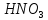 30%. Густина розчину
30%. Густина розчину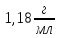 ;
;

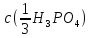 в розчині з масовою часткою
в розчині з масовою часткою
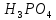 10,32%.Густина
розчину
10,32%.Густина
розчину
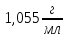 ;
;
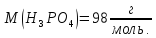
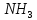 в отриманому розчині. Густина розчину
в отриманому розчині. Густина розчину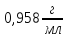 .
.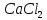 10% застосовується в медицині як
протиалергійний та протизапальний
засіб. Розрахувати масову та молярну
концентрації цього розчину. Густина
розчину
10% застосовується в медицині як
протиалергійний та протизапальний
засіб. Розрахувати масову та молярну
концентрації цього розчину. Густина
розчину ,
,