
- •Тексти лекцій з фармацевтичної хімії Лікарські речовини неорганічної природи
- •Випробування на чистоту
- •Випробування на граничний вміст домішок
- •Випробування на хлориди
- •Випробування на сульфати
- •Випробування на солі амонію
- •Випробування на солі кальцію
- •Випробування на солі цинку
- •Випробування на солі важких металів
- •Випробування на миш'як
- •Випробування на солі заліза
- •Випробування на фториди
- •Випробування на солі магнію
- •Випробування на солі магнію і лужноземельні метали
- •Випробування на фосфати
- •Випробування на солі калію
- •Випробування на солі алюмінію
- •Визначення втрати в масі при висушуванні і води
- •Лікарські речовини, що містять елементи VII-VI груп періодичної системи д. І. Менделєєва План
- •Лікарські речовини - сполуки галогенів з воднем. Кислота хлористоводнева концентрована ( дфу ) (Acidum hydrochloridum concentrata) нс1
- •( Відносна щільність становить близько 1.18 )
- •Лікарські речовини, що містять солі хлорнуватистої і соляної кислот. Вапно хлорне ( біле вапно)
- •Лікарські речовини - галогеніди лужних металів Натрію хлорид (Natrii chloridum) NaCi ( дфу ) Калію хлорид (Kalii chloridum ) кci ( дфу )
- •Натрію бромід (Natrii bromidum ) № Вг ( дфу ) Калію бромід ( Kalii bromidum ) кВг ( дфу )
- •Натрію йодид ( Natrii iodidum ) Nal ( дфу ) Калію йолід ( Kalii iodidum ) ki ( дфу )
- •Препарати йоду Йод ( Iodum ) i2 ( дфу )
- •Розчин йоду спиртовий 5 % ( Solution Iodi spirituosa 5 % ) (проект монографії)
- •Розчин йоду спиртовий 10%
- •Лікарські речовини, що містять водню пероксид.
- •Гідроперит ( Нуdroperitum)
- •Магнію пероксид ( Маgnesii регохуdum )
- •Препарати, що містять сірку Натрію тіосульфат ( Natrii thiosulfas ) ( дфу )
- •Натрію сульфат декагідрат ( Natrii sulfas decahydricus ) ( дфу )
- •Сірка для зовнішнього застосування ( Sulfur ad usum externum ) ( дфу )
- •Лікарські речовини, що містять елементи III , IV і V груп періодичної системи д.І. Менделєєва
- •Натрію нітрит (Natrii nitris )
- •Аміаку розчин концентрований ( дфу )
- •Ammoniae solutio concentrate
- •Ammonia solution , concentrated *
- •Лікарські засоби, що містять миш'як і вісмут
- •Вісмуту нітрат основний Bismuthi subnitras
- •Лікарські речовини, що містять вуглець Вугілля активоване ( Carbo activatus )
- •Натрію гідрокарбонат ( дфу ) ( Natrii hydrohenocarbonas )
- •Лікарські речовини, що містять бор і алюміній Кислота борна ( дфу ) Acidum boricum
- •Натрію тетраборат ( дфу ) Вогах
- •Лікарські речовини, що містять алюміній Алюмінію гідроксид Aluminii hydroxydum
- •Лікарські речовини, що містять елементи
- •Магнію сульфат гептагідрат ( Magnesii sulfas heptahydricus ) ( дфу )
- •Магнію карбонат легкий ( Мagnesii subcarbonas levis ) ( дфу ) Магнію карбонат важкий ( Мagnesii subcarbonas ponderosus ) ( дфу )
- •Лікарські речовини, що містять кальцій
- •Кальцію хлорид дигідрат ( Calcii chloridum dihydricum ) ( дфу )
- •Кальцію хлорид гексагідрат ( СаІсі chloridum hexahydricum ) ( дфу )
- •Лікарські речовини, що містять барій
- •Барію сульфат ( Barii sulfas ) ( дфу )
- •Лікарські речовини, що містять цинк
- •Цинк оксид (Zinci oхуdum ) ( дфу ) ZnO
- •Лікарські речовини, що містять ртуть Ртуть хлорид ( сулема ) ( Нуdrargyri dichloridum) ( дфу ) HgCl2
- •Ртуті оксид жовтий ( Hydrargyri oxydum flavum ) HgO
- •Ртуті оксиціанід ( Нуdrargyri oxycyanidum)
- •Лікарські речовини, що містять елементи
- •Срібла нітрат (Argenti nitras) ( дфу )
- •Колоїдні препарати срібла ( коларгол , протаргол )
- •Коларгол ( Соllargolum)
- •Протаргол ( Protargolum )
- •Заліза сульфат гептагідрат ( Ferri sulfas heptahydricus ) ( дфу )
- •Лікарські речовини з радіоактивними ізотопами ( радіо фармацевтичні препарати) План
- •Розчин натрію фосфату , міченого фосфором -32 , для ін'єкцій ( Solutio Natrii phosphatis phosphoro -32 notati pro injectionibus )
- •Розчин натрію о - йодгіппурату , міченого йодом -131 , для ін'єкцій
Магнію сульфат гептагідрат ( Magnesii sulfas heptahydricus ) ( дфу )
Отримання . Розчиненням магнезиту в надлишку розведеної кислоти сірчаної :
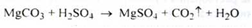
Розчин фільтрують і концентрують при паруванні до кристалізації . Сірчана кислота береться у надлишку , тому що внаслідок можливого гідролізу магнію сульфату будуть виходити основні солі типу :

Властивості. Кристалічний порошок білого кольору або блискучі безбарвні кристали. Легко розчинний у воді , дуже легко в киплячій воді , практично не розчинний у 96 % спирті.
Ідентифікація .
Реакції на Mg2 + ( rФУ ) .
Реакція на SO4- ( ДФУ ) .
Кількісне визначення . Комплексонометричний метод , індикатор - уїдливий чорний (перерахунок на суху речовину , титр розраховують на б / в магнія сульфат ) , ( s = 1 ) (ДФУ)
Застосування . При парентеральному введенні надає гіпотензивну , заспокійливу і проти судомну дію. При введенні всередину - жовчогінний і послаблюючу дію.
Зберігання . У добре закупореній тарі.
Магнію карбонат легкий ( Мagnesii subcarbonas levis ) ( дфу ) Магнію карбонат важкий ( Мagnesii subcarbonas ponderosus ) ( дфу )
![]()
Отримання .
Взаємодія розчинів магнію сульфату і натрію карбонату при 70-80 ° С:
![]()
З магнію гідрокарбонату нагріванням до 40-50 ° С:
![]()
Властивості. Порошки білого кольору. Практично не розчинні у воді. Розчиняються у розведених мінеральних кислотах з бурхливим виділенням бульбашок газу.
Ідентифікація.
Для магнію карбонату легкого насипний об'єм 15 г субстанції повинен бути близько 180 мл, для важкого - близько 30 мл (ДФУ).
Реакції на карбонати (а, Ь, с) (ДФУ).
3 . Реакція на Mg 2+ , після розчинення в кислоті азотної і нейтралізації надлишку кислоти натріэи гідроксидом ( ДФУ ) .
Кількісне визначення . Комплексонометрія ( індикатор - уїдливий чорний) після розчинення субстанції в кислоті хлористоводневої . Розрахунок ведуть на магнію оксид
( 40-45 %) , ( s = 1) . ( ДФУ ) .
Застосування . В’яжучий і антацидний засіб .
Зберігання . У добре закупореній тарі.
Лікарські речовини, що містять кальцій
З'єднання кальцію зустрічаються в природі у вигляді вапняку і крейди , мармуру , мінералів - гіпсу ( CaS04 • 2Н20 ) і флюорита ( CaF2 ) .
Кальцію хлорид дигідрат ( Calcii chloridum dihydricum ) ( дфу )
![]()
Кальцію хлорид гексагідрат ( СаІсі chloridum hexahydricum ) ( дфу )
![]()
Отримання . Обробкою крейди або мармуру кислотою хлористоводневою з подальшим очищенням і концентруванням :
![]()
У природних мінералах містяться домішки іонів магнію і заліза , які при обробці кислотою хлористоводневою переходять у MgCl2 і FeCl2 . Отриманий розчин насичують газоподібним хлором ( FeCl2 окислюють до FeCl3 ) і потім додають надлишок кальцію гідроксиду :

Розчин збагачується кальцієм хлоридом , а домішки випадають в осад , який фільтрують . Надлишок кальцію гідроксиду переводять у кальцій хлорид , діючи кислотою хлористоводневою :
![]()
Властивості. Кристалічна маса білого кольору або білі кристали.
CaCl2•6H2O гігроскопічний. СаСI2 * 2Н20 - легко розчинний у воді , розчинний в 96 % спирті ; СаСl2 • 6Н20 - дуже легко розчинний у воді , легко розчинний в 96 % спирті , замерзає при t ° = 29С °.
Індентифікація .
Реакція ( а ) на СІ- ( ДФУ ) .
Реакції на Са2+ ( a , b , c , d ) ( ДФУ ) .
Субстанція повинна витримувати вимоги розділу « Кількісне визначення » (ДФУ ) .
Кількісне визначення . Комплексонометрія в присутності індикатора калькокарбонової кислоти і розчину натрія гідроксиду концентрованого ; ( s = 1 ) :


В точці еквівалентності:

Застосування . При посиленому виведенні кальцію з організму , при алергічних захворюваннях спільно з протигістамінними препаратами , як засіб, що зменшує проникність судин , як кровоспинний засіб , як протиотрута при отруєнні солями магнію.
Зберігання . У повітронепроникному контейнері.
