
Контр_Спецпитання_термодинаміки
.docМіністерство освіти і науки України
ХАРКІВСЬКИЙ ДЕРЖАВНИЙ ТЕХНІЧНИЙ УНІВЕРСИТЕТ
БУДІВНИЦТВА ТА АРХІТЕКТУРИ
Спеціальність 6.092108
До друку дозволяю
Перший проректор університету Д.Л. Череднік
МЕТОДИЧНІ ВКАЗІВКИ
до виконання контрольних робіт з курсу
«СПЕЦПИТАННЯ ТЕРМОДИНАМІКИ»
|
Усі цитати, цифровий, фактичний матеріал та бібліографічні відомості перевірено, написання одиниць відповідає стандартам. |
Затверджено на засіданні кафедри ТГВ та ТВЕР Протокол № 10 від 05.05.2010 р. |
Укладачі: В.Б. Поволочко
Н.Г. Ланцберг
Відповідальний за випуск О.Ф. Редько
Декан санітарно-технічного факультету В.В. Шилін
Бібліотека

ХАРКІВСЬКИЙ ДЕРЖАВНИЙ ТЕХНІЧНИЙ
УНІВЕРСИТЕТ БУДІВНИЦТВА ТА АРХІТЕКТУРИ
Спеціальність 6.092108
МЕТОДИЧНІ ВКАЗІВКИ
до виконання контрольних робіт з курсу
«СПЕЦПИТАННЯ ТЕРМОДИНАМІКИ»
Харків 2010
Міністерство освіти і науки України
ХАРКІВСЬКИЙ ДЕРЖАВНИЙ ТЕХНІЧНИЙ УНІВЕРСИТЕТ
БУДІВНИЦТВА ТА АРХІТЕКТУРИ
Спеціальність 6.092108
МЕТОДИЧНІ ВКАЗІВКИ
до виконання контрольних робіт з курсу
«СПЕЦПИТАННЯ ТЕРМОДИНАМІКИ»
|
Затверджено на засіданні кафедри ТГВ та ТВЕР Протокол № 10 від 05.05.2010 р. |
Харків 2010
Методичні вказівки до виконання контрольних робіт з курсу «Спецпитання термодинаміки» для студентів спеціальності 6.092108 «Теплопостачання і вентиляція» / Укладачі: В.Б. Поволочко, Н.Г. Ланцберг – Харків: ХДТУБА, 2010. – 16 с.
Рецензент Н.М. Басова
Кафедра «Теплогазопостачання, вентиляції та використання теплових вторинних енергоресурсів»
ВСТУП
Дисципліна «Спецпитання термодинаміки» відноситься до циклу професійно-орієнтованих дисциплін в системі підготовки випускника з вищою освітою з освітньо-кваліфікаційним рівнем «Бакалавр» за спеціальністю «Теплогазопостачання та вентиляція».
Призначення дисципліни «Спецпитання термодинаміки» надати знань студентам щодо методів розрахунку термодинамічних процесів у проточних системах: витікання газів, компресорних,теплових та холодильних машинах.
Дисципліна «Спецпитання термодинаміки» передбачає вивчення:
- принципів розрахунку проточних систем;
- методів розрахунку витікання та дроселювання газів та пари;
- методів розрахунку циклів двигунів внутрішнього згорання, паросилових установок та компресорних машин;
- методів розрахунку циклів холодильних машин та теплових насосів.
Надання студентам теоретичних знань та прищеплення їм практичних навичок відбувається під час лекційних та лабораторних занять, а також шляхом самостійної роботи, спрямованої на закріплення теоретичних знань і практичних навичок.
Для засвоєння дисципліни «Спецпитання термодинаміки» необхідні знання з курсів вища математика, фізика та термодинаміка.
У результаті вивчення курсу студент повинен бути ознайомленим:
- із поняттям ексергії потоку та її використанням для оптимізації енерготехнологічного обладнання;
- із сучасними методами енергозбереження та використанням альтернативних джерел енергії.
Задача №1
Визначити швидкість витікання повітря з резервуара з постійним тиском Р1 МПа і температурою t1 і його секундні витрати.
Повітря витікає в атмосферу через трубку з внутрішнім діаметром d.
Зовнішній тиск Р2 (рис. 1).
Вихідні дані подані в таблиці 1.
Таблиця 1 – Вихідні дані
|
Кінцева цифра шифру |
Р1, МПа |
t1, 0С |
Передостання цифра шифру |
d, мм |
Р2, МПа |
|
0 |
1,0 |
10 |
0 |
10 |
0,55 |
|
1 |
1,2 |
11 |
1 |
11 |
0,6 |
|
2 |
1,5 |
12 |
2 |
12 |
0,15 |
|
3 |
1,3 |
13 |
3 |
10 |
0,18 |
|
4 |
1,4 |
14 |
4 |
11 |
0,14 |
|
5 |
1,6 |
15 |
5 |
12 |
0,16 |
|
6 |
2,0 |
16 |
6 |
10 |
0,12 |
|
7 |
2,1 |
17 |
7 |
11 |
0,17 |
|
8 |
2,2 |
18 |
8 |
12 |
0,20 |
|
9 |
2,5 |
20 |
9 |
10 |
0,25 |
Приклад розв’язання
Дано: Р1 = 10 МПа; t1 = 150С; d = 10 мм.
Розв’язання:
![]()
![]() (для
повітря);
(для
повітря);
0,01<0,528 (для повітря).
Пояснення: Отримане числове значення Р2/Р1 порівнюють з так званим критичним відношенням тисків для даного газу, який визначається з рівності
![]() (1.1)
(1.1)
|
|
і рівним: для одноатомних газів при k = 1,67 (Р2/Р1)кр = 0,487; для двоатомних газів при k = 1,4 (Р2/Р1)кр = 0,528; для трьох-багатоатомних газів при k= 1,29 (Р2/Р1) кр = 0,546. |
|
Рис. 1 |
|
Якщо адіабатне витікання газу відбувається при (Р2/Р1)> (Р2/Р1) кр, то теоретична швидкість газу у гирлі звуженого сопла визначається за формулою
 ,
(1.2)
,
(1.2)
де k - показник адіабати;
υ1 - питомий обсяг газу на вході в сопло.
Замінюючи для ідеального газу у формулі р1υ1 на RT, отримуємо
 .
(1.3)
.
(1.3)
У формулах (1.2) і (1.3) значення р, v і R дані відповідно в таких одиницях: Па, кг/м3 і Дж/(кг К).
Теоретична швидкість газу може бути також знайдена за формулою
![]() ,
(1.4)
,
(1.4)
де h1 і h2 - відповідно ентальпії газу в початковому і кінцевому станах в Дж/кг.
Якщо значення h виражені в кДж/кг, то формула (1.4) набуває вигляду:
![]()
У всіх наведених випадках швидкість w вимірюється в м/с.
Витрати газу визначаються за формулою
 ,
(1.5)
,
(1.5)
де f - вихідний перетин сопла в м2.
Якщо ж адіабатне витікання газу відбувається при (Р2/Р1)≤ (Р2/Р1) кр, то теоретична швидкість газу в гирлі звуженого сопла буде дорівнювати критичній швидкості і визначиться з рівняння
![]() .
(1.6)
.
(1.6)
Критична швидкість визначена за формулою (1.6) залежить тільки від початкового стану газу та показника адіабати k. Тому, підставляючи значення k для різних робочих тіл, отримаємо більш зручні формули для визначення критичної швидкості. Зокрема, для двоатомних газів:
![]() (1.7)
(1.7)
або
![]() (1.8)
(1.8)
Критична швидкість може бути також визначена за однією з наступних формул:
-
 ;
;(1.9)
 ,
,
де h - ентальпія газу при критичному тиску ркр.
У першій формулі ентальпія виражена в Дж /кг, у другій - в кДж /кг.
Витрати газу в цьому випадку будуть максимальними і можуть бути обчислені за рівнянням
![]() . (1.10)
. (1.10)
Підставляючи до цієї формули значення k, отримаємо:
-
для двоатомних газів:
![]() ;
(1.11)
;
(1.11)
-
для трьохатомних газів:
![]()
![]() .
(1.12)
.
(1.12)
Розв’язання:
Швидкість витікання дорівнює критичній і визначається за формулою
![]() м/с.
м/с.
Секундні витрати знаходимо за формулою
![]() ,
,
![]() ,
,
d=10 мм = 0,01 м; R=287 Дж/кг°К; Т1=273+150=2880К,
![]() м3/кг,
м3/кг,
отже,
![]() кг/с.
кг/с.
Задача №2
Визначити часові витрати аміаку, розсолу і охолоджуючої води, та теоретичну потужність двигуна холодильної машини, якщо
-
холодопродуктивність установки - Q0, кВт (табл. 2);
-
теплоємність розсолу - Ср, кДж/кг0С (табл. 2).
Параметри аміаку:
-
вхід – на всмоктування в компресор: t10C; х1(ступінь сухості);
-
вихід – після адіабатного стиснення: t20C; х2=1;
-
тиск аміаку після дроселювання, Р, МПа;
-
ступінь сухості пари на виході з випарника, х1.
Температура розсолу:
-
на вході:
 ,0С
(табл. 2);
,0С
(табл. 2); -
на виході:
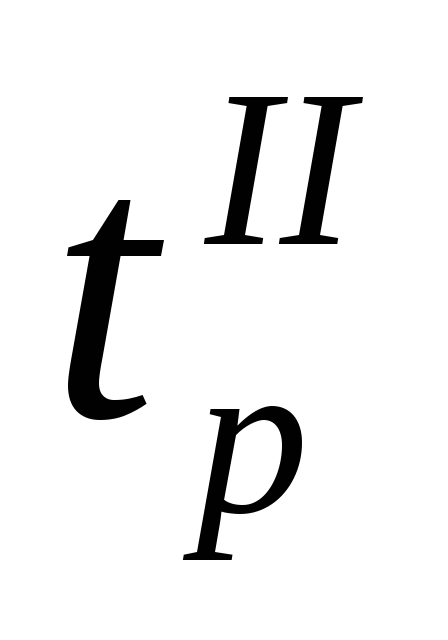 ,0С
(табл. 2).
,0С
(табл. 2).
Таблиця 2
|
Кінцева цифра шифру |
QО, кВт |
Параметри розсолу |
Перед-остання цифра шифру |
Параметри аміаку |
Параметри води |
|||||||
|
ср, кДж/кг °С |
tрI, оС |
tрII, оС |
t1, оС |
Х1 |
t2, оС |
Х2 |
Р1, МПа |
tвI, оС |
tвI, оС |
|||
|
0 |
60,0 |
4,20 |
-2,0 |
-5,0 |
0 |
-10 |
0,92 |
20 |
1 |
0,29 |
12 |
20 |
|
1 |
65,0 |
4,18 |
-3,1 |
-6,1 |
1 |
-5 |
0,91 |
18 |
1 |
0,35 |
13 |
21 |
|
2 |
70,0 |
4,19 |
-2,1 |
-5,1 |
2 |
-15 |
0,93 |
15 |
1 |
0,24 |
14 |
22 |
|
3 |
58,0 |
4,21 |
-2,2 |
-5,2 |
3 |
-20 |
0,94 |
25 |
1 |
0,19 |
11 |
20 |
|
4 |
67,0 |
4,22 |
-2,3 |
-5,3 |
4 |
-15 |
0,95 |
22 |
1 |
0,24 |
12 |
21 |
|
5 |
72,0 |
4,23 |
-3,2 |
-6,2 |
5 |
-10 |
0,89 |
20 |
1 |
0,29 |
15 |
25 |
|
6 |
62,0 |
4,24 |
-3,3 |
-6,3 |
6 |
-5 |
0,90 |
15 |
1 |
0,35 |
14 |
23 |
|
7 |
75,0 |
4,17 |
-2,4 |
-6,4 |
7 |
-20 |
0,88 |
21 |
1 |
0,19 |
12 |
22 |
|
8 |
77,0 |
4,25 |
-2,5 |
-5,5 |
8 |
-25 |
0,87 |
19 |
1 |
0,15 |
13 |
26 |
|
9 |
80,0 |
4,26 |
-2,5 |
-5,7 |
9 |
-30 |
0,86 |
24 |
1 |
0,12 |
12 |
22 |
|
Рідина Вода Пар |
Цикл парової компресорної холодильної установки. Схема парової компресорної холодильної установки зображена на рис. 2. Насичена пара аміаку (або іншого робочого тіла) при температурі, близькій до температури охолоджуваного приміщення 1, всмоктується компресором 2 і адіабатно стискається. З компресора пар аміаку надходить в конденсатор 3, де в результаті постійного тиску він конденсується внаслідок поглинання його теплоти охолоджуючою водою. |
|
Рис. 2 |
Отриманий рідкий аміак надходить до редукційного вентиля 4, в якому відбувається його дроселювання, що супроводжується падінням тиску і температури. При цьому аміак частково випаровується.
Отримана дуже волога насичена пара (ступінь сухості х зазвичай знаходиться в межах 0,01 - 0,15) з низькою температурою і є холодоносієм. Його направляють до труби охолоджуваного приміщення, де за рахунок теплоти, що відбирається від охолоджуваних тіл, ступінь сухості його збільшується, і він знову прямує до компресора. Далі цей цикл повторюється.
На рис. 3 в діаметрі Тs дано цикл зміни стану 1 кг аміаку в паровій компресорній установці з проміжним теплоносієм. Точка 1 характеризує стан пари аміаку на час входу її в компресор, лінія 1 - 2 - процес адіабатного стискання в компресорі, точка 3 - стан рідкого аміаку перед входом його в редукційний вентиль, в якому він піддається дроселюванню. Так як цей процес характеризується рівністю значень ентальпій в початковому і кінцевому станах, то в точці 4, яка відповідає стану аміаку після дроселювання, останній має таку саму ентальпію, що і в точці 3. Лінія 4-1 відповідає процесу пароутворення у випарнику.
|
|
Залежно від того, яка пара всмоктується компресором (суха чи волога), процес у холодильних машинах називають сухим або вологим. У випадку сухого процесу в випарнику виходить сухий насичений пар. Щоб забезпечити надходження до компресора сухої пари, холодильну установку забезпечують віддільником рідини, або сепаратором, через який рідина повертається у випарник. Витрату роботи в компресорі під час адіабатного стискання визначають за формулою |
|
Рис. 3 |
lк=h2-h1.
Холодопродуктивність 1 кг холодильного агента є наступною:
q0=h1-h4= r(x1-x4),
де r - теплота пароутворення, a x1-x4 — відповідно ступінь сухості пари після випарника і після редукційного вентиля.
Теплове навантаження конденсатора визначається за формулою
q=q0 +l0=h2- h3.
Приклад роз’вязання
Дано: Q0=58,15[кВт=кДж/с];
Ср=4,19 кДж/кг0К;
t1= -100С;
х1=0,92;
t2= 200С;
х2=1;
![]() =120С;
=120С;
![]() =
200С;
=
200С;
Р = 0,3 МПа;
х1 = 0,92;
![]() = -20С;
= -20С;
![]() = -50С.
= -50С.
Розв’язання
На рис. 4. Зображено цикл аміачної холодильної машини.

Рис. 4 – цикл аміачної холодильної машини
1-2 – адіабатний стиск в компресорі; т. 3 – стан рідкого аміаку перед дроселюванням; т. 4 – стан рідкого аміаку після дроселювання; 4-1 – випаровування аміаку в випарнику
Работа в компресорі:
lк=h2-h1,
де h2 – ентальпія сухої насиченої пари на виході з компресора (див. додаток А) при температурі t2= 200C;
h2=hII=1699,4 кДж/кг;
![]() =
512,5 кДж/кг;
=
512,5 кДж/кг;
r2 = 1186,9 кДж/кг (теплота пароутворення).
Ентальпія вологої пари NH3, що всмоктується компресором:
![]() .
.
При t1=-100C (див. додаток А) при всмоктуванні в компресор:
![]() 372,6
кДж/кг,
372,6
кДж/кг,
![]() 1296,6
кДж/кг.
1296,6
кДж/кг.
Тоді:
![]() 372,6+1296,6∙0,92
= 1565,6 кДж/кг;
372,6+1296,6∙0,92
= 1565,6 кДж/кг;
Робота, що витрачається на привід компресора, буде складати:
![]() 1699,4
- 1565,6 = 133,8 кДж/кг.
1699,4
- 1565,6 = 133,8 кДж/кг.
Кількість NH3 (аміаку), що всмоктується компресором:
![]()
 ,
,
де Q0 - холодопродуктивність;
q0 - питома холодопродуктивність:
![]() 1565,6
- 512,5 = 1053,1 кДж/кг
1565,6
- 512,5 = 1053,1 кДж/кг
![]() (
(![]() = 512,5 кВт).
= 512,5 кВт).
Кількість аміаку знаходиться наступним чином:
![]() 0,0552 кг/с = 198,72 кг/год.
0,0552 кг/с = 198,72 кг/год.
Теоретична потужність двигуна буде складати:
![]() 0,0552 х 133,8 = 7,39 кВт.
0,0552 х 133,8 = 7,39 кВт.
Витрати розсолу визначимо з
рівняння
![]() :
:
 4,626 кг/с = 16653,6 кг/год;
4,626 кг/с = 16653,6 кг/год;
![]() .
.
Витрати охолоджуючої води в компресорі складають

Задача №3
Виконати розрахунок процесу теоретичного стискання в поршневому компресорі.
Дано:
Барометричний (атмосферний) тиск: Рб = 102 кПа.
Надмірний тиск стисненого повітря: Ризб = 2 кг/см2.
Обсяг повітря на початку процесу стиснення: V1 = 113,6*10-6 .
Температура всмоктуваного повітря t1 (див. табл. 3).
Температура стисненого повітря в повітрозбірнику t2 (див. табл. 3).
Число оборотів валу компресора f (див. табл. 3).
Таблиця 3
|
Кінцева цифра шифру |
t1, 0С |
t2, 0С |
Передостання цифра шрифту |
f, об/хв. |
|
0 |
18 |
35 |
0 |
770 |
|
1 |
19 |
36 |
1 |
780 |
|
2 |
20 |
37 |
2 |
790 |
|
3 |
21 |
38 |
3 |
800 |
|
4 |
22 |
39 |
4 |
810 |
|
5 |
17 |
36 |
5 |
800 |
|
6 |
16 |
35 |
6 |
780 |
|
7 |
23 |
40 |
7 |
820 |
|
8 |
24 |
41 |
8 |
830 |
|
9 |
25 |
42 |
9 |
800 |
Вказівки до розв’язання задачі:
1 Визначити початкові і кінцеві параметри повітря, що стискається в політропному процесі (див. рис. 1)
Дійсний абсолютний тиск повітря в кінці процесу всмоктування (Па): Р1 = Рб.
Абсолютний тиск в кінці процесу стиснення (Па) обчислюється за формулою
Р2 = Рб + Ризб.
Маса М повітря, що стискається, визначається з рівняння стану ідеального газу, так як повітря за властивостями є близьким до ідеального газу, (кг):
![]() ,
,
де R1= 287 Дж/(кг°К) – питома газова стала повітря.
Об'єм повітря в кінці процесу стискання V2 обчислюється з рівняння стану (м3):
![]() .
.
2 Визначення термодинамічних характеристик політропного процесу стиснення 1-2
Показник політропи n визначення співвідношення початкових і кінцевих значень параметрів процесу стиснення: Р1V1n = Р2V2n, звідки
 .
.
Теплоємність процесу (Дж/кг°К):
![]() ,
,
де Сv – ізохорна масова теплоємність повітря;
Сv = 720 Дж/кг°К;
к – показник адіабати, для повітря к = 1,4.
Знак теплоємності буде
негативниv,
так як процес політропного стиснення
відбувається з відведенням теплоти (
dq<0 ), але температура газу при цьому
все ж таки підвищується (dТ>0), тому
![]() <0.
<0.



