
- •Технологія спирту лабораторний практикум
- •6.051701 «Харчові технології та інженерія»
- •Технологія спирту
- •Дослідження органолептичних і фізичних властивостей зерна
- •Основні теоретичні положення
- •Визначання органолептичних показників (гост 10967-90)
- •Проведення визначання
- •Визначання фізичних показників
- •Визначання явно вираженої смітної та зернової домішок
- •Визначання вмісту зіпсованих і ушкоджених зерен
- •Визначання вмісту шкідливої домішки
- •Визначання вмісту особливо враховуваних домішок Визначання вмісту сажкових зерен
- •Визначання вмісту гальки
- •Визначання вмісту металомагнітної домішки
- •Кінцеве обробляння результатів визначання загального вмісту смітної й зернової домішок
- •Визначання вмісту дрібних зерен і крупності
- •Визначання натури зерна (гост 10840-64)
- •Визначання маси 1000 зерен (гост 10842-89)
- •Проведення визначання
- •Визначання зараженості зерна шкідниками (гост 13586.4-83)
- •Проведення визначання
- •Органолептичні та фізичні показники досліджуваного зерна
- •Контрольні питання
- •Основні теоретичні положення
- •Визначання вологи зерна
- •Основний стандартний метод визначання вологи зерна
- •Хід визначання
- •Визначання умовної крохмалистості
- •Підготовка до визначання
- •Виділення наважок для аналізу
- •Проведення аналізу із застосуванням 1,124% - ного розчину соляної кислоти
- •Проведення аналізу із застосуванням розчину хлористого кальцію.
- •Обробляння результатів
- •Визначання загальної лужності або кислотності в мелясі
- •Хід визначання
- •Визначання активної кислотності.
- •Підготовка до визначання Приготування реактиву Герлеса
- •Проведення визначання
- •Обробляння результатів
- •Визначання масової частки суми цукрів, що зброджуються
- •Визначання інверсійної поляризації
- •Підготовка до визначання Приготування розчину соляної кислоти
- •Проведення визначання
- •Обробляння результатів
- •Визначання масової частки редукувальних речовин класичним методом Мюллера
- •Проведення визначання
- •Обробляння результатів
- •Визначання масової частки редукувальних речовин методом Оффнера (метод, який використовується в разі виникнення розбіжностей в оцінці якості)
- •Підготовка до визначання Приготування початкового розчину
- •Проведення визначання
- •Обробляння результатів
- •Визначання доброякісності меляси
- •Хімічні показники зерна
- •Контрольні питання
- •Тема: Визначання вмісту засвоюваного азоту та азоту амінокислот у мелясі. Визначання калію, натрію і кальцію в мелясі.
- •Теоретична основи
- •Визначання вмісту загального азоту в мелясі.
- •Визначання амінного азоту «мідним методом».
- •Визначання калію кобальтонітритним методом у мелясі.
- •Комплексометричний метод визначання кальцію.
- •Визначання кольору меляси.
- •Оцінка якості меляси.
- •Контрольні питання.
- •Тема: Оцінка якості ферментних препаратів, що застосовуються у спиртовому виробництві
- •Теоретична частина
- •Визначання амілолітичної активності (ас)
- •Підготовка до визначання Приготування розчину крохмалю з масовою часткою 1 % (субстрата)
- •Приготування фосфатного буферного розчину з рН 5,6 і рН 6,0
- •Приготування основного розчину йоду
- •Приготування робочого розчину йоду
- •Приготування основного розчину очищених ферментних препаратів
- •Приготування робочого розчину очищених ферментних препаратів
- •Приготування основного розчину із повітряно-сухої культури гриба
- •Приготування робочого розчину із повітряно-сухої культури гриба
- •Приготування основного розчину із культурної рідини бактеріального походження
- •Приготування робочого розчину із культуральної рідини
- •Проведення визначання
- •Обробляння результатів
- •Визначання глюкоамілазної активності
- •Підготовка до визначання
- •Приготування основного і робочого розчинів очищених ферментних препаратів готують за п.1
- •Приготування основного і робочого розчинів із повітряно-сухої культури гриба
- •Приготування робочого розчину із культуральної рідини
- •Побудова градуювального графіка
- •Проведення визначання
- •Обробляння результатів
- •Визначання глюкоамілазної активності (ГлС) глюкооксидазним методом (арбітражний метод)
- •Приготування до визначання
- •Обробляння результатів
- •Визначання оцукрюючої активності (ос)
- •Підготовка до визначання
- •Визначання оцукрюючої активності в очищених препаратах і в культурі гриба, отриманого із Asp. Awamori
- •Визначання оцукрюючої активності в очищених препаратах і в культурі із Bac. Subtilis
- •Обробляння результатів
- •Контрольні питання:
- •Теоретична частина.
- •Визначання якісних показників затору. Відбір середньої проби
- •Визначання концентрації сухих речовин
- •Визначання повноти оцукрювання затору
- •Визначання загальної й активної кислотності
- •Приготування розчину індикатора метилового червоного.
- •Проведення визначання
- •Оцінка якості затору
- •Визначання вмісту незброджених цукрі. Теоретична частина
- •Метод Бертрана
- •Приготування реактивів
- •Хід визначання
- •Приклади розрахунків:
- •Визначання вмісту незброджених розчинних цукрів в зерновій зрілій бражці. Теоретична основа
- •Хід визначання
- •Визначання загального вмісту незброджених розчинних вуглеводів і нерозчинного крохмалю
- •Хід визначання
- •Оцінка якості
- •Контрольні питання
- •Теоретична частина.
- •Порядок виконання роботи. Визначання кольоровості, загального вигляду смаку та запаху.
- •Визначання вологості
- •Визначання кислотності.
- •Визначання підйомної сили.
- •Оцінка якості
- •Приклад
- •Визначання об'ємної частки спирту етилового
- •Підготовка до визначання
- •Проведення визначання
- •Обробляння результатів
- •Контроль якості вимірювань
- •Визначання проби на чистоту
- •Проведення визначання
- •Визначання проби на фурфурол
- •Підготовка проби спирту до визначання
- •Проведення визначання
- •Обробляння результатів
- •Визначання окислюваності спирту
- •Проведення визначання
- •Контроль якості вимірювань
- •Визначання масової концентрації альдегідів
- •Визначання масової концентрації альдегідів з фуксиносірчистим реактивом 1 у спирті етиловому ректифікованому
- •Підготовка проби спирту до визначання
- •Проведення визначання
- •Обробляння результатів
- •Визначання масової концентрацїї альдегідів з фуксиносірчистим реактивом і у спирті етиловому — сирці
- •Контроль якості вимірювань
- •Визначання масової концентрації сивушного масла
- •Визначання масової концентрації сивушного масла з саліциловим альдегідом
- •Кількісне визначання масової концентрації сивушного масла в спирті
- •Проведення визначання
- •Обробляння результатів
- •Контроль якості вимірювань
- •Визначання масової концентрації сивушного масла (ізоамілового, ізобутилового і пропілового спиртів) з парадиметиламінобензальдегідом (п-дмаба)
- •Готування дослідних водно-спиртових розчинів
- •Готування розчину парадиметиламінобензальдегіду (п-дмаба) в сірчаній кислоті
- •Кількісне визначання масової концентрації сивушного масла в спирті етиловому ректифікованому
- •Обробляння результатів
- •Контроль якості вимірювань
- •Випробовування етилового спирту-сирцю на вміст сивушного масла
- •Визначання масової концентрації кислот
- •Проведення визначання
- •Обробляння результатів
- •Контроль якості вимірювань
- •Визначання масової концентрації органічних речовин, що омилюються Визначання масової концентрації органічних речовин методом омилювання
- •Проведення визначання
- •Обробляння результатів
- •Визначанні масової концентрації естерів у спирті етиловому-сирці проводять методом омилювання ,аналогічно попередньому досліду. Контроль якості вимірювань
- •Визначання масової концентрації естерів
- •Готування розчину солянокислого гідроксиламіну концентрацією 2 моль/дм3
- •Моль/дм3
- •Готування розчинів реакційної суміші
- •Проведення визначання
- •Обробляння результатів
- •Контроль якості вимірювань
- •Випробовування спирту етилового — сирцю
- •Обробляння результатів
- •Контроль якості вимірювань — за таблицею 12. Визначання об'ємної частки метилового спирту
- •Підготовка до визначання Готування водного розчину динатрієвої солі хромотропової кислоти з масовою часткою 2 %
- •Готування водного розчину перманганату калію
- •Обробляння результатів
- •Аналіз етилового спирту - сирцю на вміст метилового спирту проводять аналогічно попередньому досліду Контроль якості вимірювань
- •Визначання масової концентрації сухого залишку
- •Проведення визначання
- •Обробляння результатів
- •Контрольні питання
- •Тема: Органолептичний аналіз спирту етилового ректифікованого Мета роботи: в процесі дегустації визначити головні показники якості: смак, запах, прозорість. Основні теоретичні положення.
- •Колір, прозорість.
- •Сприйняття смаку
- •Сприйняття запаху
- •Умови і порядок проведення дегустації. Види і характер дегустації.
- •Приміщення для дегустації
- •Порядок і методи проведення дегустації
- •Система дегустаційних оцінок
- •Контрольні питання.
- •Література: Основна література:
- •Додаткова література:
- •З лабораторних робіт
Обробляння результатів
Масову частку суми цукрів, що зброджуються, Сзбр. у відсотках обчислюють за формулою:
Сзбр. = 0,68П + 0,96И + 0,80Ис,
де П – масова частка сахарози, %;
И – величина інверсійної поляризації, %;
Ис – масова частка редукувальних речовин, %.
За кінцевим результатом випробування приймають середнє арифметичне результатів двох паралельних визначень, допущена розбіжність між якими не повинна перевищувати 0,7 %.
Визначання доброякісності меляси
Доброякісність меляси розраховують за рівнянням:
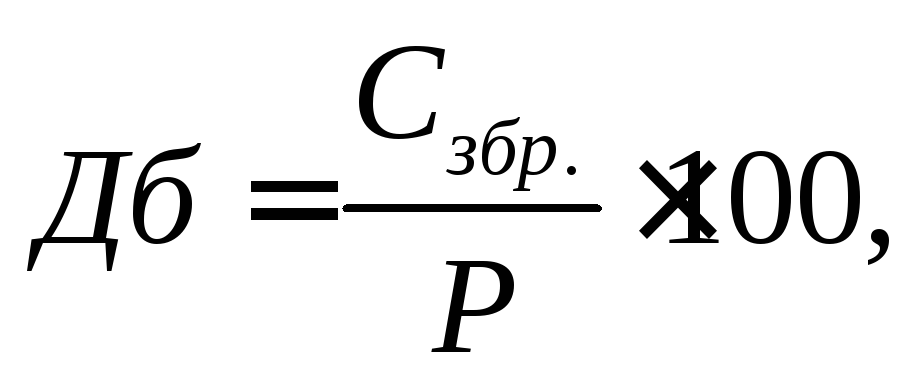
де Сзбр. – масова частка суми цукрів, що зброджуються, %;
Р – масова частка сухих речовин у мелясі, %.
Хімічні показники зерна
|
№ п/п |
Назва показників |
Вимоги ГОСТу на зерно |
Фактичні дані | ||
|
Зразок 1 |
Зразок 2 |
Зразок 3 | |||
|
1. |
Вологість, % |
|
|
|
|
|
2. |
Вміст крохмалю, % |
|
|
|
|
Контрольні питання
1.Сировина, яка використовується для виробництва спирту етилового
ректифікованого. Характеристика сировини згідно з ДСТУ.
2.Підготовка сировини до виробництва, як зерна так і меляси.
3.Визначання вологи у зерні.
4.Розшифруйте термін «умовна крохмалистість».
5.Сутність методу Визначання крохмалистості за Еверсом.
6.Визначання лужності або кислотності меляси. В яких одиницях виражають
ці показники?
7.Визначання вмісту сухих речовин меляси. Сутність методу.
8.Сутність методу Визначання сахарози у мелясі.
9.Розшифруйте поняття «зброджувальні цукри». Як вони визначаються?
10.Сутність методу інверсійної поляризації.
11.Як визначають редукувальні речовини за методом Оффнера і Мюллера.
Провести порівняльну характеристику цих методів.
12. Основні показники доброякісної меляси. Як розраховують доброякісність
меляси?
ЛАБОРАТОРНА РОБОТА № 3
Тема: Визначання вмісту засвоюваного азоту та азоту амінокислот у мелясі. Визначання калію, натрію і кальцію в мелясі.
Мета роботи: Вивчити метод Визначання загального азоту методом Кьєльдаля і амінного азоту мідним методом. Вивчити комплексометричний метод Визначання кальцію,кобальтонітритний метод швидкого Визначання калію.
Теоретична основи
Азотні речовини меляси в процесі росту дріжджів змінюються, утворюють нові сполуки в значній мірі визначають вихід і якість готового продукту.
Загальний вміст азоту визначають по методу Кьєльдаля. Принцип методу складається в окисленні органічних азотовмісних сполук концентрованою сірчаною кислотою при нагріванні. При цьому вуглець та водень окислюється киснем, який виділився при розкладенні сірчаної кислоти, азот відщеплюється в вигляді аміаку, який з сірчаною кислотою утворює сульфат амонію. При цьому пробігають такі реакції:
H2SO4 → H2O + SO2 + O;
C + O2 → CO2
H2 + O →H2O
RNH2 + HOH → ROH + NH3;
( де R – радикал органічної сполуки )
2NH3 + H2SO4 → (NH4)2SO4.
Після згорання додають NaOH, в результаті чого виділяється аміак, який відганяють розчином сірчаної кислоти, концентрації с(1/2Н2SO4)=0.1моль/дм3
(NH4)2SO4 + 2NaOH → Na2SO4 + 2H2O + 2NH3.
2NH3 + H2SO4 → (NH4)2SO4.
Надлишок кислоти відтитровують розчином (NaOH)=0,1моль/дм3 та по кількості кислоти, яка вступила в реакцію з аміаком визначають кількість аміаку в перерахунку на азот.
Мідний метод полягає в здатності амінокислот утворювати розчинні комплексні сполуки з надлишком суспензії ортофосфату міді Си3(РО4)2∙3Н2О в боратному буферному розчині. Надлишок ортофосфату міді відфільтровують, в фільтрат додають оцтову кислоту і йодиту калію та титрують тіосульфатом натрію, концентрацією с=0,01 моль/дм3.
2Си(RCHNH2СОО)2 + 4КI = 2CuI + I2 + 4RCHNH2COOK.
1см3 0,01моль/дм3 розчину тіосульфату натрію відповідає 0,28мг азоту амінокислот.
Методи визначання калію, натрію і кальцію розділяються на хімічні і фізико-хімічні. Серед перших для Визначання кальцію і магнію застосовують комплексометрію. Для Визначання калію застосовують кобальтонітритний метод.
В основі кобальтонітритного методу лежить реакція взаємодії калію із кобальтонітритом натрію в нейтральному або слабко кислому середовищі з утворенням мілко кристалічного осаду жовтого кольору у вигляді комплексної солі: Na3[Co(NO2)6]+2K=2Na+K2Na[Co(NO2)6]
Реакція специфічна і дуже чутлива, особливо у присутності натрію. Осад, що утворився, промивають, висушують і зважують.
Комплексометричний метод визначання кальцію заснований на здатності комплексона 111 (трилон Б або етилендиамінтетраацетат натрію Na2H2 [ЕДТА])утворювати в лужному середовищі з катіонами Са2+ і Mg2+ розчинні у воді, але міцні внутрішньо комплексні сполуки за схемою:
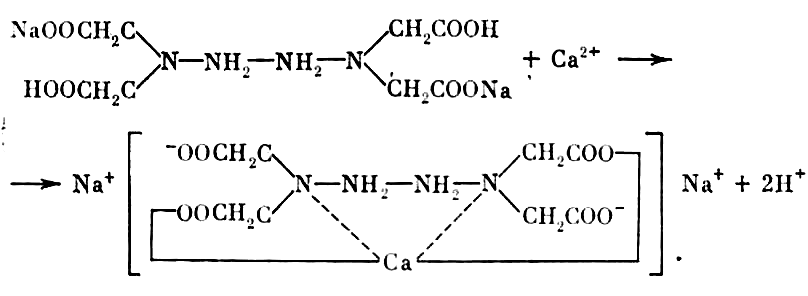
Міцність утвореного комплексу Na2Ca[ЕДТА] залежить від величини рН. Для здвигу реакції зліва направо водень, що утворився, необхідно нейтралізувати надлишком лугу. При титруванні трилоном Б дослідженого розчину, який містить Са2+ і Мg2+, кінець комплексоутворення встановлюють спеціальними органічними індикаторами, що відносяться до азобарвників.
Калій міститься в мелясі в кількості від 1 до 5,5% в перерахунку на К2О. Встановлено, що для нормального виходу хлібопекарських дріжджів в буряковій мелясі має бути не менше 3,5% К2О.
Відомо також, що в нормальній мелясі міститься Са2+ в перерахунку на СаО від 0,1 до 1,5%. Проте на спиртові і дріжджові заводи іноді надходить меляса із вмістом СаО більше 10%, що різко погіршує умови біосинтезу і розділення біомаси.
Комплексометричне визначання катіону кальцію в мелясі проводять в присутності магнію не більше 25 мг в титрованому об'ємі.
