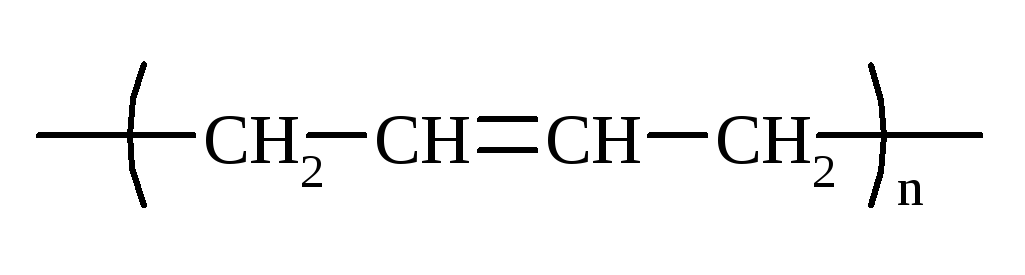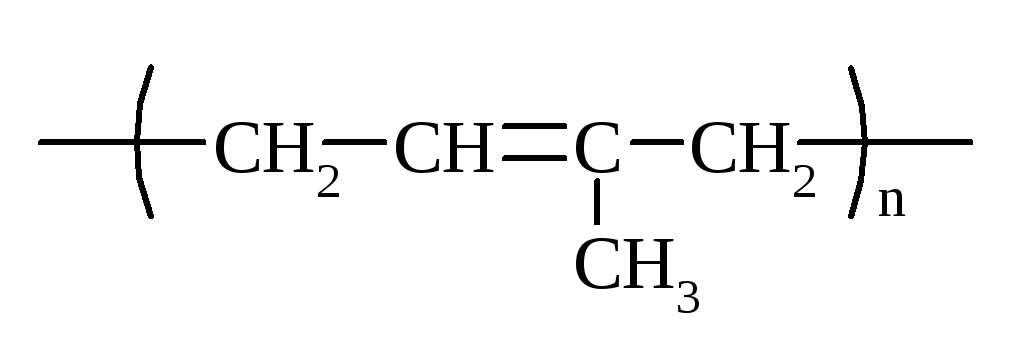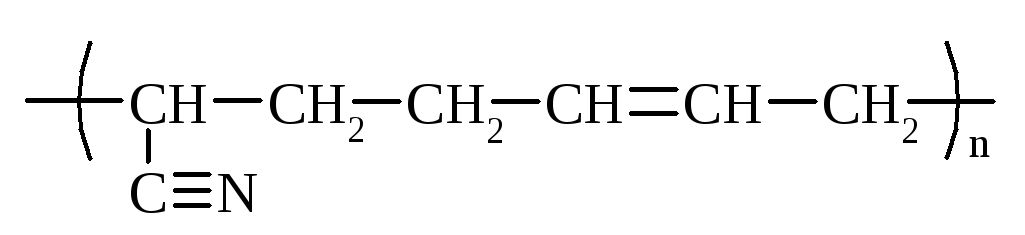3. Фізичні властивості.
У гомологічному ряду алкадієнів перші представники С3-С4 – гази; С5-С15 – рідини, а С16 – тверді речовини. Із збільшенням молекулярної маси зростають температури плавлення та кипіння, які підпорядковані таким же закономірностям, що і в рядах алканів та алкенів, (табл. 8.1.).
4. Будова алкадієнів.
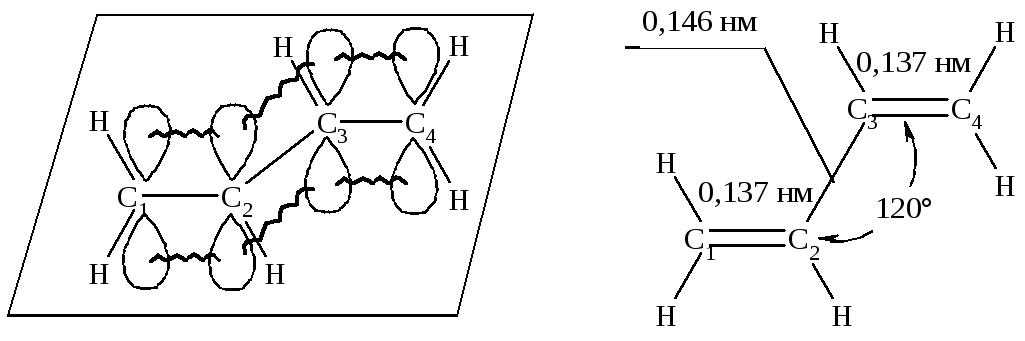
В алкадієнах атоми карбону подвійного зв’язку знаходяться у sp2-гібридному стані. Орбітальна модель молекули бутадієну-1,3 наведена на рис. 8.1.
|
Рис. 8.1. Орбітальна модель ,-супряження в молекулі бутадієну-1,3. |
Молекула дивінілу копланарна, тобто всі гібридизовані sp2-АО знаходяться у одній площині, а негібридизовані pz-орбіталі атомів карбону розташовуються у перпендикулярній до неї площині. -Зв’язок в бутадієні-1,3 |
утворюється при перекриванні s-орбіталей атомів гідрогену і гібридизованих sp2-орбіталей атома карбону або при перекриванні атомів карбону між собою; природа утворення -зв’язку дещо інша, ніж у алкенах. У цьому випадку маємо ,-супряження, при якому перекривання pz-орбіталей атому карбону С1-С2 та С3-С4, має місце часткове додаткове перекривання pz-орбіталей атомів карбону С2-С3. При цьому відбувається перерозподіл (делокалізація) -електронної густини з утворенням єдиної -електронної системи:
|
|
Підтвердженням цьому є скорочення зв’язку С2-С3 (від 0,154 нм в алканах до 0,137 в дієнах). За рахунок ,-супряження алкадієни стають термодинамічно більш стабільними. Енергію ,-супряження можна визначити, порівнюючи експериментальні та розрахункові значення енергії гідрування, наприклад, бутадієну-1,3: Нексп.=-238,6 кДж/моль, Нрозрах.=-251,2 кДж/моль. |
Різниця Нексп. - Нрозрах.=-238,6-(-251,2)=12,6 кДж/моль в енергіях називається енергією супряження.
За рахунок часткового перекривання pz-орбіталей атомів карбону С2-С3 в молекулі бутадієну-1,3 вільне обертання навколо цього зв’язку утруднюється, що приводить до утворення S-цис- та S-транс-ізомерів:

5. Хімічні властивості.
Відмінність у будові алкадієнів, у порівнянні з алкенами, приводить до того, що вони приєднують різні сполуки не лише по одному подвійному зв’язку (1,2-приєднання), а й до крайніх атомів супряженої системи з переміщенням подвійного зв’язку (1,4-приєднання). Співвідношення продуктів реакції залежить від умов її перебігу та від природи електрофільного реагенту.
5.1. Реакції1,2- та 1,4-приєднання.
5.1.1. Реакцією гідрування, в залежності від умов її перебігу, утворюються різні продукти:
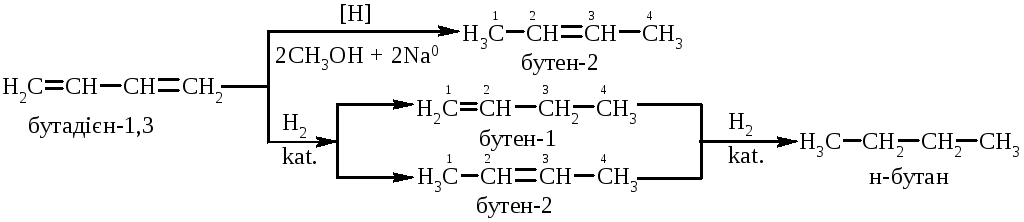
Атомарний гідроген (Н) в момент виділення відновлює бутадієн-1,3 до бутену-2, а гідрування в присутності каталізаторів (Pt0, Ni0) приводить до кінцевого н-бутану.
5.1.2. Приєднання галогеноводнів (HCl, HBr) відбувається з утворенням продуктів 1,2- та 1,4-приєднання:
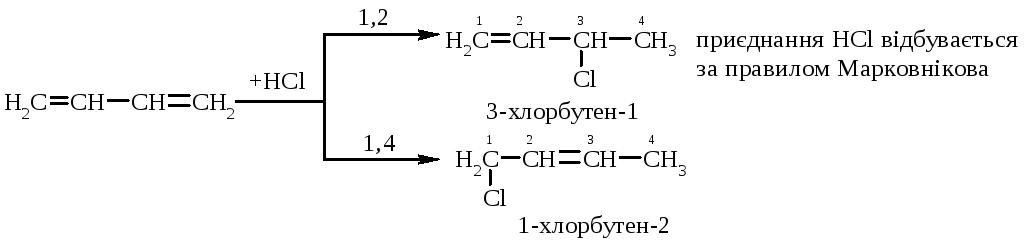
Співвідношення продуктів реакції залежить від умов її перебігу (t°, ), а сама реакція відбувається за механізмами АЕ або AR.
Механізм реакції АЕ:
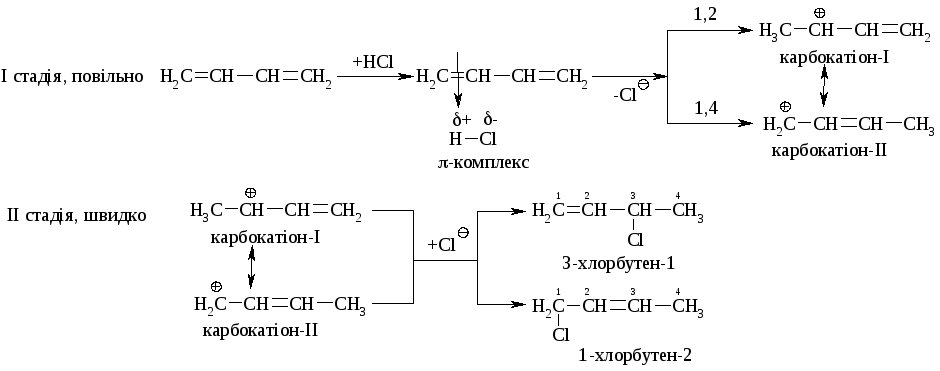
На першій стадії йде утворення карбокатіонів І та ІІ, за рахунок ,р-супряження. Подальше утворення та співвідношення продуктів 1,2- та 1,4-приєднання (стадія ІІ) підлягає кінетичному та термодинамічному контролю.
Як правило, вихід продуктів 1,4-приєднання з підвищенням температури зростає:
|
Температура, °С |
Продукти, % | |
|
1,2-приєднання |
1,4-приєднання | |
|
-80 |
80 |
20 |
|
+20 |
34 |
66 |
|
+40 |
20 |
80 |
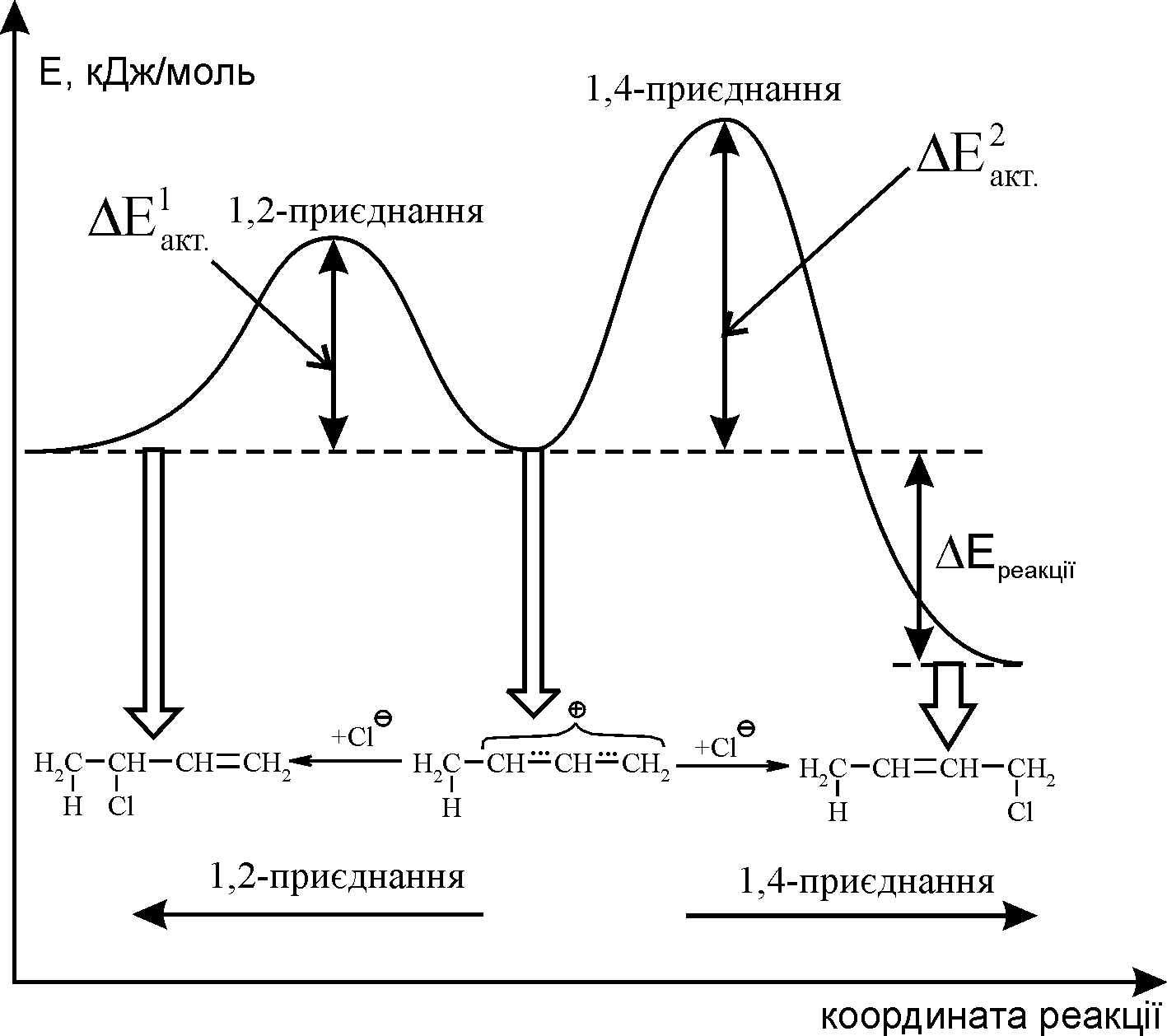
Цей факт можна пояснити за допомогою енергетичної діаграми гідрохлорування бутадієна-1,3, рис. 8.2.
|
Рис. 8.2. Енергетична діаграма гідрохлорування бутадієну-1,3. |
При
низьких температурах швидкість
реакції визначається енергією
активації
5.1.3. Приєднання галогенів (Cl2, Br2) відбувається, як і у випадку з галогеноводнями, з утворенням продуктів 1,2- та 1,4-приєднання за АЕ та AR-механізмами: |
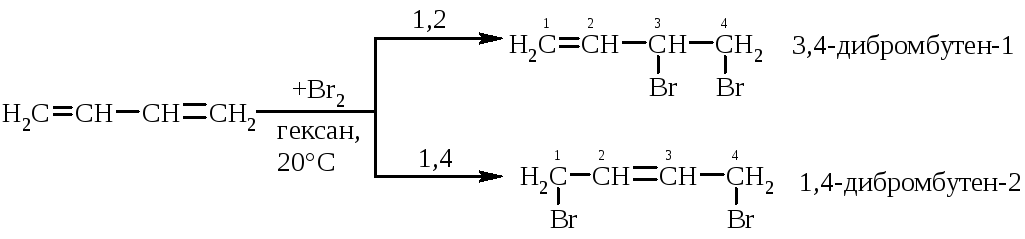
У випадку ініціювання молекулярного брома (h) реакція відбувається за AR-механізмом:
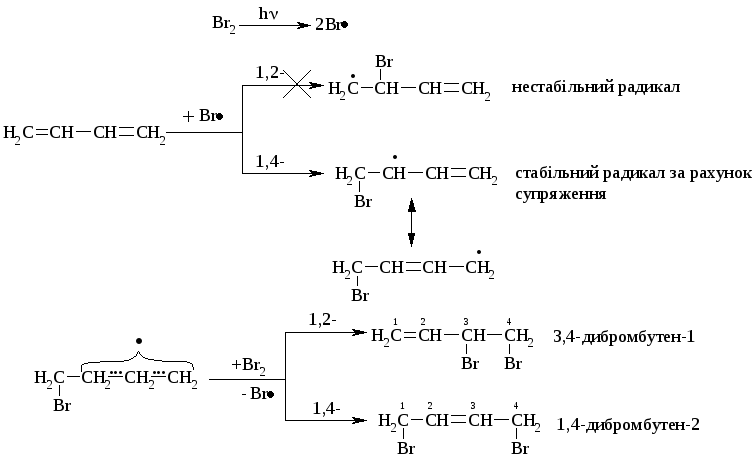
5.2. Реакція дієнового синтезу (реакція 1,4-приєднання Дільса-Альдера, 1923 р.; Нобелівська премія 1950 р.). Взаємодіють супряжені цис-алкадієни та дієнофіли (алкени або алкіни із електроноакцепторними групами: –NO2, –CN, –COOH):
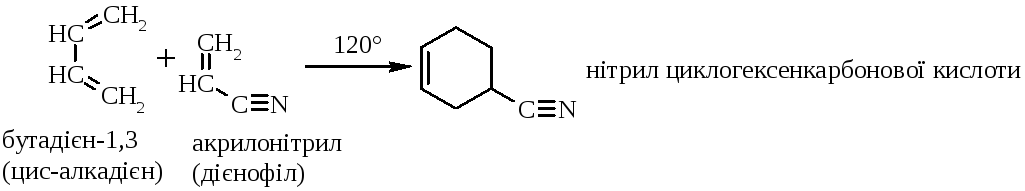
5.3. Реакція полімеризації.
Здатність вступати в реакцію полімеризації є важливою властивістю дієнових вуглеводнів. Полімеризація 1,3-дієнів відбувається за рахунок розкриття подвійних зв’язків переважно в положеннях 1,4, як за радикальним, так і за іонним механізмами:
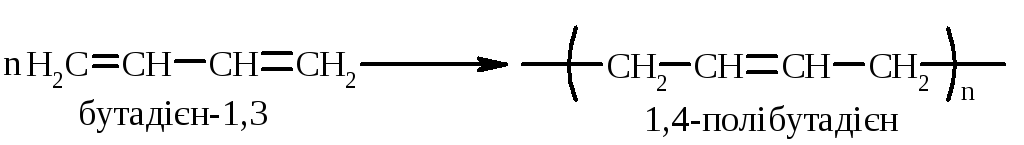
Необхідно відзначити, що в залежності від типу реакції полімеризації та умов її перебігу дієни реагують в 1,2- та 1,4-положення:
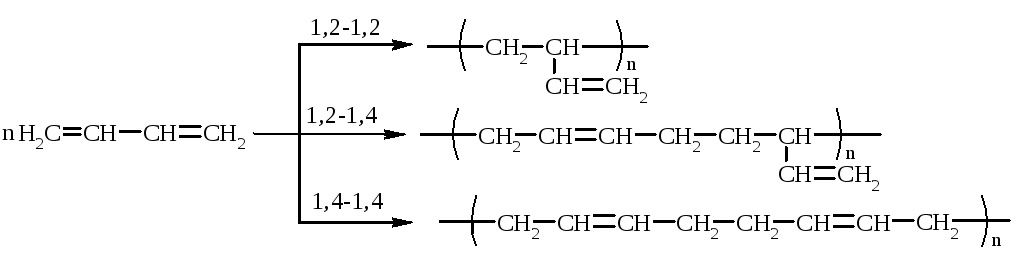
При цьому ланки головного ланцюга полібутадієну можуть мати цис- або транс-конфігурацію:
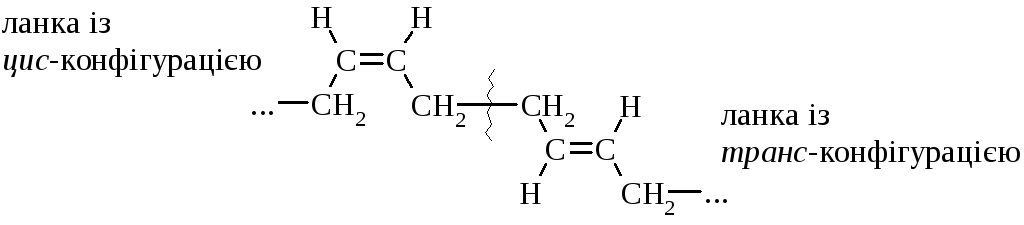
В табл. 8.2. наведені найважливіші синтетичні каучуки (СК) полімеризації супряжених дієнових вуглеводнів та їх функціональних похідних.
Таблиця 8.2.
Основні синтетичні каучуки.
|
Формула |
Назва каучука |
Промислове позначення |
|
|
бутадієновий |
СКБ |
|
|
ізопреновий |
СКІ |
|
|
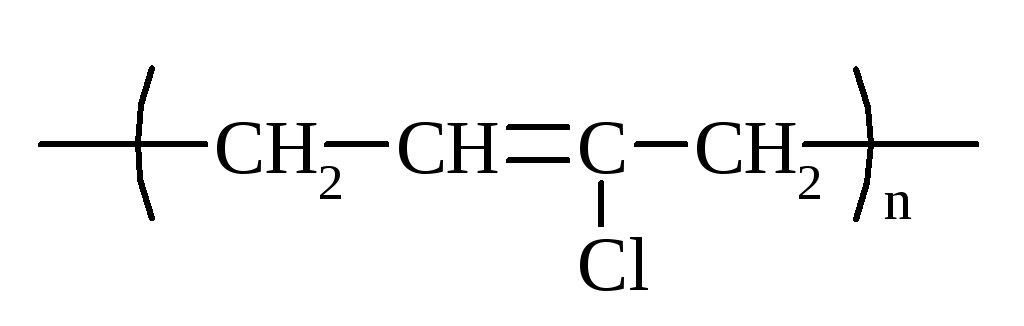
хлоропреновий |
наірит, неопрен (СКХ) |
|
|
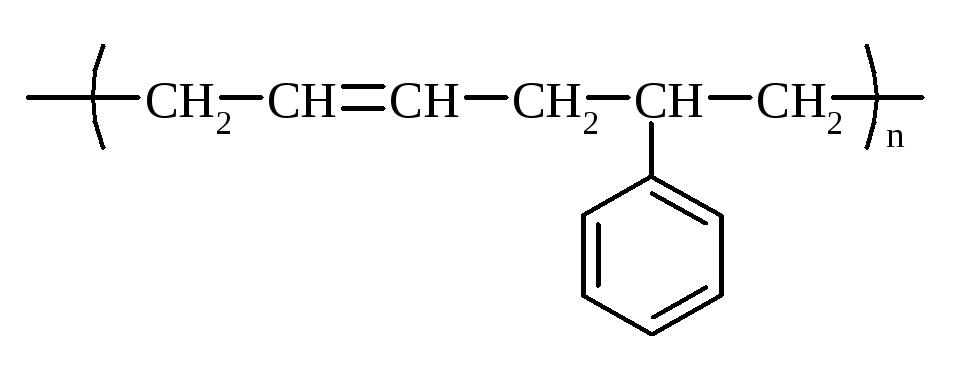
бутадієнстирольний |
СКС |
|
|
бутадієннітрильний |
СКН |
Для добування гуми, із якої виготовляють числені вироби, проводять вулканізацію (поперечне зшивання полімерних ланцюгів) синтетичних каучуків елементною сіркою під дією прискорювачів цього процесу:
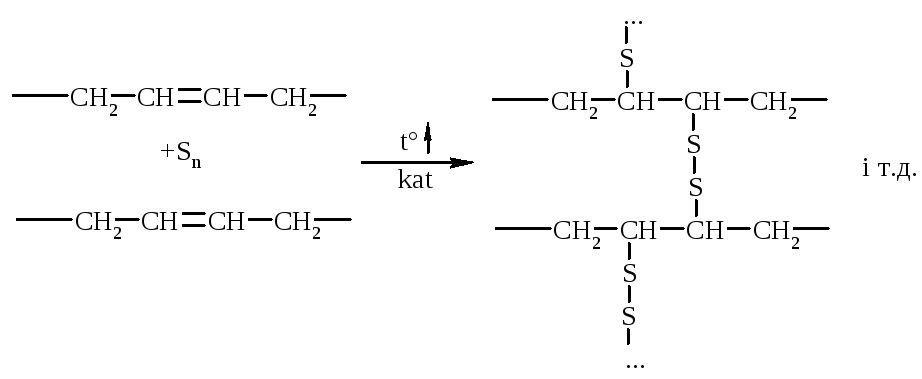
Гуми, в залежності від наявності в їх складі різних інгредієнтів, можуть мати високі механічні та фізико-хімічні властивості.