
Slyshenkov_Rabochaja_tetrad
.pdf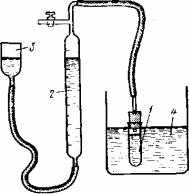
Лабораторная работа № 5
Химическая кинетика
«______»____________200____г.
Тема: изучение скорости разложения пероксида водорода газометрическим методом.
Цель: ознакомиться с кинетическими методами исследования, экспериментально определить энергию активации реакции, константу скорости и ее зависимость от температуры.
Оборудование и реактивы: схема установки для изучения скорости разложения Н2О2 газометрическим методом, термостат, секундомер, 3 %-й раствор перекиси водорода, 0,1 н. раствор дихромата калия, пипетка, колба, химический стакан, пробирки.
Схема установки для изучения скорости разложения Н2О2 газометрическим методом
Выполнение работы
Пероксид водорода в водных растворах самопроизвольно медленно разлагается по уравнению: H2O2 →H2O + 0,5 O2 . Катализаторами этой реакции могут быть ионы Fe2+, Fe3+, Cr2O72-, CrO42-, WO42-, МоО42-, смешанные катализаторы: CuSO4 + МоО42-, CuSO4 + NiSO4 и
многие другие. При соответствующем подборе условий реакция может протекать по первому или близкому к первому порядку. За ходом реакции наблюдают по измерениям объема выделившегося кислорода через различные промежутки времени от начала реакции.
1. В штативе закрепите бюретку (2) на 25 мл и уравнительный сосуд (3), соединенные каучуковой трубкой и содержащие подкрашенную воду. Верхний конец бюретки соедините с пробиркой (1). С помощью уравнительного сосуда установите уровень воды в бюретке на нулевое деление. На дно пробирки капельной пипеткой внесите 15 капель 3 %-ного раствора пероксида водорода и 4 капли 0,1 н. раствора дихромата калия. Затем быстро пробирку плотно соедините с бюреткой, так, чтобы прибор был герметичен, и одновременно включите секундомер. Каждую минуту производите отсчет по бюретке, отмечая время. Во время отсчета жидкость в бюретке и уравнительном сосуде должна быть на одном уровне. Опыт продолжайте до тех пор, пока возможен отсчет выделившегося за 1 мин кислорода. Когда за это время уровень жидкости начнет опускаться менее чем на одно деление, секундомер остановите. Всего в среднем за 12 мин выделяется около 13 мл кислорода. Опыт проведите при двух температурах: 22 и 40 ºС. Результаты запишите в таблицу по образцу.
2. Определите V∞ – объем кислорода, выделившийся после разложения всего пероксида водорода. Для этого пробирку со смесью растворов пероксида водорода и дихромата калия, соединенную с бюреткой, поместите в воду с температурой 90 ºС и произведите отсчет по бюретке при максимальном выделении кислорода.
Температура опыта, °С____________; катализатор _______________;
20
PDF created with pdfFactory Pro trial version www.pdffactory.com
количество пероксида водорода________.
|
|
|
|
|
|
|
|
|
|
|
Таблица 1 |
|
№ |
Время |
Уро- |
Объем |
V∞-Vτ |
lg(V∞-Vτ ) |
Скорость |
lgWτ |
|
k |
|
||
изме- |
от |
вень |
выделив |
|
|
реакции |
|
|
|
|
||
рения |
начала |
жид- |
шегося |
|
|
|
Wτ |
|
|
|
|
|
|
реак- |
кости в |
газа Vτ, |
|
|
1. по расчетам |
|
|
|
|
||
|
ции, |
бюрет- |
см3 (мл) |
|
|
2. по графику |
|
|
|
|
||
|
τ,мин |
ке, мл |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
t=22 ºС |
|
|
|
|
1 |
|
2 |
1 |
|
|
|
1 |
1 |
|
|
|
|
|
|
|
|
|
|
|
2 |
2 |
|
|
|
|
|
|
|
|
|
|
|
3 |
3 |
|
|
|
|
|
|
|
|
|
|
|
4 |
4 |
|
|
|
|
|
|
|
|
|
|
|
5 |
5 |
|
|
|
|
|
|
|
|
|
|
|
6 |
6 |
|
|
|
|
|
|
|
|
|
|
|
7 |
7 |
|
|
|
|
|
|
|
|
|
|
|
8 |
8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
K1ср= |
|
|
|
t=40 ºС |
|
|
|
|
|
|
|
|
|
|
|
1 |
1 |
|
|
|
|
|
|
|
|
|
|
|
2 |
2 |
|
|
|
|
|
|
|
|
|
|
|
3 |
3 |
|
|
|
|
|
|
|
|
|
|
|
4 |
4 |
|
|
|
|
|
|
|
|
|
|
|
5 |
5 |
|
|
|
|
|
|
|
|
|
|
|
6 |
6 |
|
|
|
|
|
|
|
|
|
|
|
7 |
7 |
|
|
|
|
|
|
|
|
|
|
|
8 |
8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
K2ср= |
|
|
3. Рассчитайте (V∞ – Vτ ), lg(V∞ – Vτ ) скорость реакции Wτ |
и логарифм скорости lgWτ по |
|||||||||||
формуле W= (V∞ – (V∞ – Vτ))/τ для каждого измерения при двух температурах, |
результаты |
|||||||||||
запишите в таблицу: |
|
|
|
|
|
|
|
|
|
|
||
_______________________________________________________________________________________
_______________________________________________________________________________________
_______________________________________________________________________________________
_______________________________________________________________________________________
_______________________________________________________________________________________
_______________________________________________________________________________________
_______________________________________________________________________________________
_______________________________________________________________________________________
_______________________________________________________________________________________
_______________________________________________________________________________________
4. Рассчитайте константу скорости реакции по формуле: k = |
2,303 |
lg |
|
V∞ |
для каждого |
|
τ |
V |
∞ |
−V |
|||
|
|
|
|
τ |
|
|
измерения и среднее ее значение при двух температурах. Результаты запишите в таблицу. (V∞ – объем кислорода, выделившийся после разложения всего пероксида водорода, определяется как разность уровней в бюретке в момент, принятый за начало реакции, и после кипячения Н2О2 до полного разложения):
_______________________________________________________________________________________
_______________________________________________________________________________________
21
PDF created with pdfFactory Pro trial version www.pdffactory.com

_______________________________________________________________________________________
_______________________________________________________________________________________
_______________________________________________________________________________________
_______________________________________________________________________________________
_______________________________________________________________________________________
5. По опытным данным постройте графики зависимости разности объемов кислорода от времени V∞ – Vτ = f(τ) для двух температур (на оси абсцисс откладывайте время в минутах). Из графиков определите скорость реакции по тангенсу угла наклона касательной к кривой, сравните с расчетным значением. Все полученные результаты запишите в таблицу 1:
22 °С 
 40 °С
40 °С
6. По опытным данным постройте графики зависимости логарифма разности объемов кислорода от времени lg(V∞—Vτ )=f( τ ) для двух температур (на оси абсцисс откладывайте время в минутах). По графикам определите порядок и константу скорости реакции, сравните с расчетным значением. Все полученные результаты запишите в таблицу 1:
|
|
|
|
|
|
22 °С |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
40 °С |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(22 °С) n = |
К |
1с |
= |
(40 °С) n = |
К |
2с |
= |
. |
22
PDF created with pdfFactory Pro trial version www.pdffactory.com

|
k2ср |
æ |
1 |
|
1 |
ö |
|||
7. Рассчитайте энергию активации реакции по формуле: ln |
= |
Еакт |
*ç |
- |
|
÷ |
|||
|
|
|
|
|
|||||
|
k1ср |
|
R èçT1 |
T |
÷ |
||||
|
|
2 ø |
|||||||
_________________________________________________________________________________
_________________________________________________________________________________
_________________________________________________________________________________
_________________________________________________________________________________
_________________________________________________________________________________
8. По опытным данным постройте графики зависимости логарифма скорости реакции lg W τ (ордината) через различные промежутки времени от логарифма разности объемов выделенного кислорода lg(V¥—Vτ) (абсцисса) (lgWτ =f[lg(V¥—Vτ)]) по графикам определите порядок реакции:
Выводы.
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
Вопросы.
1.Чем измеряется скорость реакции? Какие факторы влияют на ее величину?
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
23
PDF created with pdfFactory Pro trial version www.pdffactory.com
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
2.Сформулируйте основные положения теории активации молекул. Что называется энергией активации?
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
3.Что называется катализом, катализатором? Какие виды катализа вы знаете?
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
4.Какие вы знаете методы определения порядка реакции?
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
24
PDF created with pdfFactory Pro trial version www.pdffactory.com
Лабораторная работа № 6
Поверхностные явления
«______»____________200____г.
Тема: измерение адсорбции уксусной кислоты на поверхности угля.
Цель работы: исследовать адсорбцию на границе жидкой и твердой фаз, построить изотерму адсорбции и найти константы в уравнении Фрейндлиха.
Оборудование и реактивы: три колбы на 100 (150) мл с корковыми пробками, шесть конических колб на 150 мл, мерные пипетки, цилиндры, бюретка на 50 мл с делениями в 0,1 мл, три вороноки для фильтрования, фильтровальная бумага, активированный уголь, растворы 1М СН3СООН, 0,1 М NaOH, фенолфталеин (индикатор).
Выполнение работы
1. Разбавлением 1 М раствора уксусной кислоты приготовьте в трех колбах растворы примерно следующих концентраций и в количествах, указанных в таблице 1:
Таблица 1
Номер колбы |
1 |
2 |
3 |
|
Объем |
раствора, мл |
100 |
100 |
100 |
Концентрация, моль/л |
0,0125 |
0,05 |
0,2 |
|
Объем |
раствора |
40 |
20 |
5 |
кислоты, взятый на |
|
|
|
|
титрование, мл |
|
|
|
|
2. Определите точную концентрацию уксусной кислоты в полученных пробах титрованием их 0,1М раствором NaOH (индикатор — фенолфталеин), причем из колб пипеткой отберите указанный в таблице 1 объем растворов. Результаты титрования V1 и рассчитанную точную концентрацию растворов кислоты до адсорбции запишите в таблицу 2:
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
3.В следующие три колбы с пробками отберите по 50 мл приготовленных растворов уксусной кислоты. В каждую колбу внесите по 1,5 г угля и тщательно взболтайте все колбы в течение 10 мин. После этого отфильтруйте отдельно содержимое каждой колбы через бумажные фильтры.
4.Отберите из полученных фильтратов пробы пипеткой в тех же объемах, какие были взяты
для первоначального титрования. Результаты титрования V2 и рассчитанную точную концентрацию растворов кислоты после адсорбции запишите в таблицу 2:
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
5. Рассчитайте количество уксусной кислоты n (моль), поглощенное m=1,5 г угля из 50 мл раствора по формулам n=(С1—С2)*0,05(моль),Г=n/mизанесите втаблицу 2:
25
PDF created with pdfFactory Pro trial version www.pdffactory.com

____________________________________________________________________________________________
____________________________________________________________________________________________
____________________________________________________________________________________________
____________________________________________________________________________________________
____________________________________________________________________________________________
____________________________________________________________________________________________
____________________________________________________________________________________________
____________________________________________________________________________________________
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Таблица 2 |
|
№ |
|
|
|
|
|
|
|
|
Объем |
Точная |
|
|
Объем |
Точная |
|
n=(С1—С2) |
n/m |
lg C1 |
|
lg n/m |
||||||||||||||||||||||
Колбы |
Приблизи- |
титран- |
концен. |
титран-та, |
концен. |
|
моль/г |
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
та, |
до |
|
|
V2, мл |
после |
|
*0,05 |
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
тельная |
V1, мл |
адсорб- |
|
|
|
|
|
|
|
|
|
адсорб- |
|
(моль) |
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
концентра- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
ции С1 |
, |
|
|
|
|
|
|
|
ции C2 |
, |
|
|
|
|
||||||||||||||||||
|
|
|
|
|
ция, моль/л |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
моль/л |
|
|
|
|
|
|
|
|
|
моль/л |
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
0.0125 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
0,05 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
0,2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
6. Постройте по полученным данным график изотермы адсорбции n/m=a*C1/b |
(а и 1/b — |
|||||||||||||||||||||||||||||||||||||||||
константы) в координатах n/m от С1. |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
7. Вычислите аналитическим методом константы a и b изотермы адсорбции, используя ее уравнение в логарифмической форме lg n/m=lg a+1/b*lg C:
______________________________________________________________________________
______________________________________________________________________________
______________________________________________________________________________
______________________________________________________________________________
______________________________________________________________________________
______________________________________________________________________________
______________________________________________________________________________
______________________________________________________________________________
26
PDF created with pdfFactory Pro trial version www.pdffactory.com

______________________________________________________________________________
______________________________________________________________________________
a = b = .
8. Постройте график в координатах lg n/m от lg C1, для логарифмического выражения изотермы адсорбции lg n/m=lg a+1/b*lg C. Графически определите константы a и b, принимая во внимание, что тангенс угла наклона прямой к оси абсцисс дает величину 1/b, а расстояние точки пересечения прямой с осью ординат от начала координат соответствует значению величины lg a. Сравните полученные значения с аналогичными значениями пункта 7.
________________________________________________________________________________
a = b = .
Выводы.
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
Вопросы.
1. Какие явления называются сорбцией?
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
27
PDF created with pdfFactory Pro trial version www.pdffactory.com
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
2.Какая разница между адсорбцией и абсорбцией? От каких факторов они зависят?
_______________________________________________________________________________________
_______________________________________________________________________________________
_______________________________________________________________________________________
_______________________________________________________________________________________
_______________________________________________________________________________________
_______________________________________________________________________________________
_______________________________________________________________________________________
_______________________________________________________________________________________
_______________________________________________________________________________________
_______________________________________________________________________________________
3.Где находят практическое применение адсорбция?
______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
4. В чем суть теории адсорбции Ленгмюра?
______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
5. В чем суть теории полимолеулярной адсорбции (теории БЭТ)?
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
28
PDF created with pdfFactory Pro trial version www.pdffactory.com
Лабораторная работа № 7
Коллоидные растворы.
«______»____________200____г.
Тема: способы получения коллоидных растворов.
Цель: ознакомиться с методами получения коллоидных растворов, с явлением коагуляции, научиться писать схемы мицелл.
Оборудование и реактивы. Химические стаканы на 100 мл, бюретки на 50 мл, ступка с пестиком, фарфоровая чашка, технические весы, мерные колбы на 100 и 50 мл, дистиллированная вода, растительное масло, куриное яйцо или альбумин в порошке, крахмал; растворы: 0,005 М и 0,1 М и насыщенный FeCI3, 0,005 М, 0,1М и насыщенный желтой кровяной соли K4[Fe(CN)6], 2 %-й хлорида железа (III), серы в абсолютном спирте, 0,002 М иодида калия, 0,01 М нитрата серебра, 1 %-й мыла, насыщенный сульфата аммония, 20 % солей NaCl, Na2SO4 и NaH2PO4, 5 % Na2SO4 и BaCl2.
Выполнение работы Опыт 1. Значение концентраций реагирующих веществ для получения коллоидных растворов.
Размеры дисперсных частиц при реакциях двойного обмена, в результате которого получаются нерастворимые продукты, зависят от концентрации реагирующих веществ. При очень высоких и очень низких концентрациях получают высокодисперсные (коллоидные) системы. В первом случае это объясняется возникновением одновременно очень большого количества центров кристаллизации (зародышевых центров), что связано с расходом всего реагирующего вещества. Возможность дальнейшего роста частиц этим ограничивается.
В случае низких концентраций весь возможный избыток веществ расходуется на возникновение сравнительно немногочисленных центров кристаллизации, и дальнейший рост частиц тем самым исчерпывается. При средних концентрациях реагирующих веществ получаются грубодисперсные частицы, выпадающие в осадок.
А) В стакан на 100 мл налейте 5 мл 0,005 М раствора хлорида железа (III) и добавьте 5 мл 0,005 М раствора желтой кровяной соли K4[Fe(CN)6]. Разбавьте полученный раствор 50 мл дистиллированной воды. Получается прозрачный коллоидный раствор берлинской лазури Fe4[Fe(CN)6]3. Опишите наблюдения и составьте уравнение реакции, схему мицеллы:
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
В) Выполните то же, что и в опыте 1, беря растворы хлорида железа (III) и желтой кровяной соли 0,1М концентрации. Из мутного раствора выпадает осадок берлинской лазури. Опишите наблюдения, составьте уравнение реакции:
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
С) В стакан емкостью на 100 мл налейте 5 мл насыщенного раствора хлорида железа (III), и 10 мл насыщенного раствора желтой кровяной соли. Образуется студнеобразный осадок. Часть полученного осадка перенесите в стакан со 100 мл дистиллированной воды и размешайте. Получается устойчивый золь берлинской лазури. Раствор сохраните для следующих опытов. Опишите наблюдения, составьте уравнение реакции, схему мицеллы:
29
PDF created with pdfFactory Pro trial version www.pdffactory.com
