
- •Лабораторний практикум
- •Фізична хімія
- •Передмова
- •Оформлення результатів вимірювань
- •Складання таблиць
- •Молярна електрична провідність водних розчинів
- •Побудова графіків
- •Розділ і термохімія
- •Лабораторна робота №1 визначення теплової сталої калориметра
- •Запис вимірювання температури під час досліду
- •Лабораторна робота №2 визначення теплоти гідратоутворення купрум (II) сульфату
- •Визначення теплоти нейтралізації сильної кислоти сильною основою у воді
- •Контрольні питання
- •Будова атома і молекули, електричні та оптичні властивості Рефрактометрія
- •Визначення рефракції речовини і встановлення його структури
- •Контрольні питання
- •Хімічна рівновага
- •Визначення залежності константи рівноваги від температури в гомогенній системі
- •Послідовність виконання роботи
- •Розрахунок рівноважних концентрацій речовин
- •Експерементальні данні
- •Контрольні питання
- •Розділ іv фазові рівноваги
- •Побудова та аналіз діаграм плавкості і3 простою евтектикою
- •Типи термопар
- •Визначення кристалізації речовини 3 розчину при низьких температурах
- •Послідовність виконання роботи
- •Лабораторна робота №7 кристалізація бінарних сумішей (система NaNо3 – kno3)
- •Контрольні питання
- •Розділ V розчини
- •Лабораторна робота №8 розподіл речовини між двома рідкими фазами
- •Послідовність виконання роботи
- •Визначення ступеня асоціації оцтової кислоти в бензолі (чи хлороформі)
- •Вивчення процесу екстрагування
- •Контрольні питання
- •Кріоскопія, ебуліоскопія
- •Установка термометра Бекмана для кріоскопії.
- •Лабораторна робота №11 визначення молекулярної маси речовини кріоскопічним методом
- •Послідовність виконання роботи.
- •Визначення молекулярної маси речовини ебуліоскопічним методом (метод визначення молекулярної маси по Сиволобову)
- •Послідовність виконання роботи.
- •Завдання до лабораторної роботи
- •Контрольні питання
- •Електрохімія
- •Водневий показник як кількісна характеристика кислотності-основності розчинів
- •Потенціометрія
- •Визначення рН буферних розчинів
- •Послідовність виконання роботи
- •Контрольні питання
- •Хімічна кінетика
- •Вивчення швидкості йодування ацетону
- •Послідовність виконання роботи
- •Контрольні питання
- •Вивчення швидкості інверсії цукру
- •Теоретичні відомості
- •Послідовність виконання роботи
- •Підготовка до роботи поляриметра
- •Контрольні питання
- •Вивчення кінетики розчинення твердої кислоти у воді
- •Дифузія
- •Послідовність виконання роботи
- •Котрольні питання
- •Додатки
- •Значення деяких фундаментальних сталих
- •Знаки деяких математичних дій
- •Множники і префікси для утворення десяткових кратних і дольних одиниць
- •Густина води при різних температурах
- •Питома електрична провідність 0,01м розчину kСl при різних температурах
- •Інтегральна теплота розчинення солей, які утворюють кристалогідрати, при температурі 18°с.
- •Йонні електричні провідності при нескінченному розведені λ∞
- •Йонні електричні провідності при нескінченному розведені при температурі 25°c
- •Література
- •Періодична система елементів д. І. Менделєєва
Типи термопар
|
Термопара |
Позначення по ОСТу
|
Верхня межа температури, °С |
Сплави |
Склад,% |
|
Хромель–алюмель Хромель - копель Залізо - копель |
ТХ ТХК ТЖК |
950 600 600 |
Хромель Алюмель Копель |
89Ni, 10Cr, 1Fe 95Ni, 2AI, 2Мn, 1Fe 44Ni, 56Cu |
Дроти ізолюють один від одного фарфоровою чи скляною трубкою. Термопару вміщують у скляний чохол у вигляді пробірки. Спай при цьому не повинен торкатися дна і бічних стінок чохла. Вільні кінці дротів (холодний кінець термопари) повинні знаходитися при постійній температурі, для цього їх поміщають у посудину Дьюара, або в лід, що тане.
Термо ЕРС, що виникає між гарячим і холодним спаями, для термопар ТХ і ТХК у першому наближенні пропорційна різниці температур між ними і вимірюються електронним автоматичним потенціометром (ЕПП) і записується на стрічковій діаграмі друкуючою кареткою. Шкала приладу довжиною 275 мм градуйована в абсолютних мілівольтах і відповідає 11,8 мВ. Показання приладу розраховують за допомогою покажчика.
Термопара повинна бути проградуйована в умовах, близьких до умов досліду по точках плавлення (чи кипіння) чистих речовин. У цьому випадку потрібно скористатися кривими охолодження нафталіну і бензойної кислоти, температури плавлення яких відомі: Тпл.нафталіну = 80,1°С; Тпл.бензойної кислоти= 122,5°С. Як третю точку беруть температуру киплячої води.
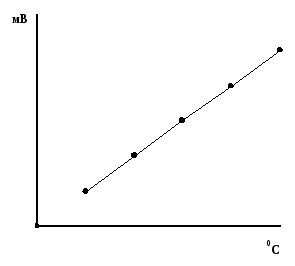
Рис. 4.3. Графік градуюровки термопари
Для побудови графіка градуюровки термопари на вісь абсцис відкладають дійсні температури, а на вісь ординат - показання потенціометра при їхній кристалізації (кипінні) у мілівольтах. Отримані точки з'єднують прямою, що служить для приведення показань потенціометра до дійсних значень температури (рис 4.3).
Лабораторна робота № 6
Визначення кристалізації речовини 3 розчину при низьких температурах
Мета роботи: визначення температури початку кристалізації сумішей нафталіну і бензойної кислоти різного складу методом термічного аналізу і побудова на підставі експериментальних даних діаграми плавкості.
Послідовність виконання роботи
Видається сім тиглів, що містять бензойну кислоту, нафталін та їх суміші:
№1 - бензойна кислота;
№ 2 -15% нафталіну і 85% бензойної кислоти;
№ 3 - 30% нафталіну і 70% бензойної кислоти;
№ 4 - 50% нафталіну і 50% бензойної кислоти;
№ 5 - 70% нафталіну і 30% бензойної кислоти;
№ 6 - 85% нафталіну і 15% бензойної кислоти;
№ 7 - нафталін.
Тигель № І ставлять на нагріту піщану баню. Коли його вміст розплавиться, у чохол для термопари, що є в кожному тиглі, вставляють термопару, включають потенціометр, переносять тигель разом з термопарою у вогнетривкий тигель, наповнений піском, і роблять діаграмний запис. Після зміни на діаграмній стрічці нахилу кривої, що відповідає початку кристалізації, запис припиняють, термопару виймають. Подібним чином роблять вимірювання з іншими тиглями, що послідовно нагрівають один за одним. Тиглі потрібно нагрівати вище температури плавлення вмісту для одержання достатньої ділянки кривої на діаграмній стрічці, що відповідає гомогенному розчину. При більшому перегріванні зростає час вимірювання, змінюється склад суміші, тому що нафталін більш леткий у порівнянні з бензойною кислотою. Через точку на початку і наприкінці кривої охолодження, де швидкість охолодження рівномірна, проводять прямі. Точка перетину прямих відповідає початку кристалізації досліджуваного розчину. За графіком градуюровки термопари необхідно перевести отримані значення в температуру в градусах С, дані звести в табл. 4.2.
На підставі дослідних даних будують діаграму температура-склад. На осі абсцис відкладають склад в масових частках, на осі ординат - температуру в градусах °С. За діаграмою визначають склад і температуру кристалізації евтектичної суміші.
Таблиця 4.2
|
Номер тигля |
Склад суміші, % |
Початок кристалізації |
|
Температура, 0С | ||
|
№1 №2 №3 №4 №5 №6 №7 |
бензойна кислота 15% нафталіну і 85% бензойної кислоти 30% нафталіну і 70% бензойної кислоти 50% нафталіну і 50% бензойної кислоти 70% нафталіну і 30% бензойної кислоти 85% нафталіну і 15% бензойної кислоти нафталін |
|
