
- •Вопрос1
- •Вопрос2
- •Вопрос3
- •Вопрос4
- •Вопрос5
- •Вопрос6
- •Вопрос7
- •Вопрос8
- •Вопрос9
- •Вопрос10
- •Вопрос11
- •Вопрос12
- •Вопрос13
- •Вопрос14
- •Вопрос15
- •Вопрос16
- •Вопрос17
- •Вопрос19
- •Вопрос20
- •Вопрос21
- •Вопрос22 оогенез
- •Вопрос23
- •Вопрос24
- •Вопрос25
- •Вопрос26
- •Вопрос27
- •Вопрос28
- •Вопрос29
- •Вопрос30
- •Вопрос31
- •Вопрос32
- •Вопрос33
- •Вопрос34
- •Вопрос35
- •Вопрос36
- •Вопрос37
- •Вопрос38
- •Вопрос 39
- •Вопрос40
- •Вопрос41
- •Вопрос42
- •Вопрос43
- •Вопрос44
- •Вопрос45
- •Вопрос46
- •Вопрос47
- •. Опорно-двигательный аппарат
- •2.1. Скелет
- •2.1.1. Осевой скелет
- •2.1.2. Скелет головы
- •2.1.3. Скелет конечностей
- •2.2. Мышечная система
- •2.2.1. Висцеральная мускулатура
- •2.2.2. Соматическая мускулатура
- •Вопрос48
- •Пищеварительная и дыхательная системы
- •14.3.1. Ротовая полость
- •3.2. Глотка
- •14.3.3. Средняя и задняя кишка
- •3.4. Органы дыхания
- •Вопрос49
- •Вопрос50
- •Вопрос51
- •Вопрос52
- •Гуморальная регуляция
- •Нервная регуляция
- •Иммунная система
- •Иммунитет отвечает за два важнейших процесса в организме:
- •Уровни регуляции физиологических функций
- •Вопрос 53
- •Вопрос54
- •Вопрос55
- •Вопрос56
- •Вопрос57
- •Вопрос58
Вопрос2
МАКРОЭЛЕМЕНТЫ - содержаться в больших
количествах, в сумме составляют более
99% массы живого организма. Это кислород,
водород, углерод, азот, сера, фосфор,
натрий, калий, хлор, кальций, магний.
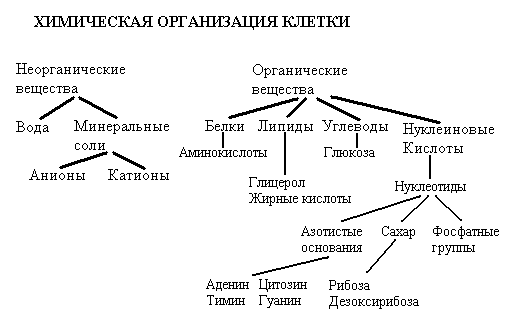
Углеводы — органические соединения, состоящие из углерода, водорода и кислорода. Их делят на простые — моносахариды (от греч. «монос» — один) и сложные — полисахариды (от греч. «поли» — много).
Липиды — это нерастворимые в воде жироподобные вещества и жиры, состоящие из глицерина и высокомолекулярных жирных кислот. Животные жиры содержатся в молоке, мясе, подкожной клетчатке. При комнатной температуре это твердые вещества. У растений жиры находятся в семенах, плодах и других органах. При комнатной температуре это жидкости. С жирами по химической структуре сходны жироподобные вещества. Их много в желтке яиц, клетках мозга и других тканях.
Белки — наиболее специфичны и важны для организма. Они относятся к непериодическим полимерам. В отличие от других полимеров их молекулы состоят из сходных, но нетождественных мономеров — 20 различных аминокислот.
Нуклеиновые кислоты (от лат. «нуклеус» — ядро) впервые обнаружены в ядре. Они бывают двух типов — дезоксирибонуклеиновые кислоты (ДНК) и рибонуклеиновые кислоты (РНК). Биологическая роль их велика, они определяют синтез белков и передачу наследственной информации от одного поколения к другому.
Молекула ДНК имеет сложное строение. Она состоит из двух спирально закрученных цепей. Ширина двойной спирали 2 нм1, длина несколько десятков и даже сотен микромикрон (в сотни или тысячи раз больше самой крупной белковой молекулы). ДНК — полимер, мономерами которой являются нуклеотиды — соединения, состоящие из молекулы фосфорной кислоты, углевода — дезоксирибозы и азотистого основания.
Вопрос3
(ДНК) — макромолекула, обеспечивающая хранение, передачу из поколения в поколение и реализацию генетической программы развития и функционирования живых организмов. Основная роль ДНК в клетках — долговременное хранение информации о структуре РНК и белков.
В клетках эукариот (например, животных или растений) ДНК находится в ядре клетки в составе хромосом, а также в некоторых клеточных органоидах (митохондриях и пластидах). В клетках прокариотических организмов (бактерий и архей) кольцевая или линейная молекула ДНК, так называемый нуклеоид, прикреплена изнутри к клеточной мембране. У них и у низших эукариот (например, дрожжей) встречаются также небольшие автономные, преимущественно кольцевые молекулы ДНК, называемые плазмидами. Кроме того, одно- или двухцепочечные молекулы ДНК могут образовывать геном ДНК-содержащих вирусов.
С химической точки зрения ДНК — это длинная полимерная молекула, состоящая из повторяющихся блоков — нуклеотидов. Каждый нуклеотид состоит из азотистого основания, сахара (дезоксирибозы) и фосфатной группы. Связи между нуклеотидами в цепи образуются за счёт дезоксирибозы и фосфатной группы. В подавляющем большинстве случаев (кроме некоторых вирусов, содержащих одноцепочечную ДНК) макромолекула ДНК состоит из двух цепей, ориентированных азотистыми основаниями друг к другу. Эта двухцепочечная молекула спирализована. В целом структура молекулы ДНК получила название «двойной спирали».
В ДНК встречается четыре вида азотистых оснований (аденин, гуанин, тимин и цитозин). Азотистые основания одной из цепей соединены с азотистыми основаниями другой цепи водородными связями согласно принципу комплементарности: аденин соединяется только с тимином, гуанин — только с цитозином. Последовательность нуклеотидов позволяет «кодировать» информацию о различных типах РНК, наиболее важными из которых являются информационные, или матричные (мРНК), рибосомальные (рРНК) и транспортные (тРНК). Все эти типы РНК синтезируются на матрице ДНК за счёт копирования последовательности ДНК в последовательность РНК, синтезируемой в процессе транскрипции, и принимают участие в биосинтезе белков (процессе трансляции). Помимо кодирующих последовательностей, ДНК клеток содержит последовательности, выполняющие регуляторные и структурные функции.
Рибонуклеи́новая кисло́та (РНК) — одна из трёх основных макромолекул (две другие — ДНК и белки), которые содержатся в клетках всех живых организмов.
Так же, как ДНК (дезоксирибонуклеиновая кислота), РНК состоит из длинной цепи, в которой каждое звено называется нуклеотидом. Каждый нуклеотид состоит из азотистого основания, сахара рибозы и фосфатной группы. Последовательность нуклеотидов позволяет РНК кодировать генетическую информацию. Все клеточные организмы используют РНК (мРНК) для программирования синтеза белков.
Азотистые основания в составе РНК могут образовывать водородные связи между цитозином и гуанином, аденином и урацилом, а также между гуанином и урацилом[15]. Однако возможны и другие взаимодействия, например, несколько аденинов могут образовывать петлю, или петля, состоящая из четырёх нуклеотидов, в которой есть пара оснований аденин — гуанин[16].
Важная структурная особенность РНК, отличающая её от ДНК — наличие гидроксильной группы в 2' положении рибозы, которая позволяет молекуле РНК существовать в А, а не В-конформации, наиболее часто наблюдаемой у ДНК[17]. У А-формы глубокая и узкая большая бороздка и неглубокая и широкая малая бороздка[18]. Второе последствие наличия 2' гидроксильной группы состоит в том, что конформационно пластичные, то есть не принимающие участие в образовании двойной спирали, участки молекулы РНК могут химически атаковать другие фосфатные связи и их расщеплять[19].
Белки́ (протеи́ны, полипепти́ды[1]) — высокомолекулярные органические вещества, состоящие из соединённых в цепочку пептидной связью альфа-аминокислот. В живых организмах аминокислотный состав белков определяется генетическим кодом, при синтезе в большинстве случаев используется 20 стандартных аминокислот. Множество их комбинаций создают молекулы белков с большим разнообразием свойств.
Белки длиной от 2 до нескольких десятков аминокислотных остатков часто называют пептидами, при большей степени полимеризации — белками, хотя это деление весьма условно.
Молекулы белков имеют большие размеры, поэтому их называют макромолекулами. Кроме углерода, кислорода, водорода и азота, в состав белков могут входить сера, фосфор и железо. Белки отличаются друг от друга числом (от ста до нескольких тысяч), составом и последовательностью мономеров. Мономерами белков являются аминокислоты (рис. 1)
Бесконечное разнообразие белков создается за счет различного сочетания всего 20 аминокислот. Каждая аминокислота имеет свое название, особое строение и свойства. Их общую формулу можно представить в следующем виде:
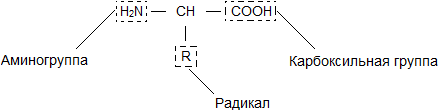
Молекула аминокислоты состоит из двух одинаковых для всех аминокислот частей, одна из которых является аминогруппой (—NH2) с основными свойствами, другая — карбоксильной группой (—COOH) с кислотными свойствами. Часть молекулы, называемая радикалом (R), у разных аминокислот имеет различное строение. Наличие в одной молекуле аминокислоты основной и кислотной групп обусловливает их высокую реакционную способность. через эти группы происходит соединение аминокислот при образовании белка. При этом возникает молекула воды, а освободившиеся электроны образуют пептидную связь. Поэтому белки называют полипептидами
Последовательность аминокислот в составе полипептидной цепи представляет первичную структуру белка. Она уникальна для любого белка и определяет его форму, свойства и функции.
Большинство белков имеют вид спирали в результате образования водородных связей между —CO- и —NH- группами разных аминокислотных остатков полипептидной цепи. Водородные связи малопрочные, но в комплексе они обеспечивают довольно прочную структуру. Эта спираль — вторичная структура белка.
Третичная структура — трехмерная пространственная «упаковка» полипептидной цепи. В результате возникает причудливая, но для каждого белка специфическая конфигурация — глобула. Прочность третичной структуры обеспечивается разнообразными связями, возникающими между радикалами аминокислот.
Четвертичная структура характерна не для всех белков. Она возникает в результате соединения нескольких макромолекул с третичной структурой в сложный комплекс. Например, гемоглобин крови человека представляет комплекс из четырех макромолекул белка.
Такая сложность структуры белковых молекул связана с разнообразием функций, свойственных этим биополимерам.
Классификация по типу строения
По общему типу строения белки можно разбить на три группы:
Фибриллярные белки — образуют полимеры, их структура обычно высокорегулярна и поддерживается, в основном, взаимодействиями между разными цепями. Они образуют микрофиламенты, микротрубочки, фибриллы, поддерживают структуру клеток и тканей. К фибриллярным белкам относятся кератин и коллаген.
Глобулярные белки — водорастворимы, общая форма молекулы более или менее сферическая.
Мембранные белки — имеют пересекающие клеточную мембрану домены, но части их выступают из мембраны в межклеточное окружение и цитоплазму клетки. Мембранные белки выполняют функцию рецепторов, то есть осуществляют передачу сигналов, а также обеспечивают трансмембранный транспорт различных веществ. Белки-транспортёры специфичны, каждый из них пропускает через мембрану только определённые молекулы или определённый тип сигнала.
Простые и сложные белки
Помимо пептидных цепей, в состав многих белков входят и неаминокислотные группы, и по этому критерию белки делят на две большие группы — простые и сложные белки (протеиды). Простые белки состоят только из полипептидных цепей, сложные белки содержат также неаминокислотные, или простетические, группы. В зависимости от химической природы простетических групп среди сложных белков выделяют следующие классы[16]:
Гликопротеины, содержащие в качестве простетической группы ковалентно связанные углеводные остатки; гликопротеины, содержащие остатки мукополисахаридов относятся к подклассу протеогликанов. В образовании связи с углеводными остатками обычно участвуют гидроксильные группы серина или треонина. Большая часть внеклеточных белков, в частности, иммуноглобулины относится к гликопротеинам. В протеогликанах углеводная часть составляет ~95 % от общей массы молекулы белка, они являются основным компонентом межклеточного матрикса;
Липопротеины, содержащие в качестве простетической части нековалентно связанные липиды. Липопротеины, образованные белками-аполипопротеинами и связывающимися с ними липидами, используются для транспорта липидов в крови;
Металлопротеиды, содержащие негемовые координационно связанные ионы металлов. Среди металлопротеидов есть белки, выполняющие депонирующие и транспортные функции (например, железосодержащие ферритин и трансферрин) и ферменты (например, цинксодержащая карбоангидраза и различные супероксиддисмутазы, содержащие в активных центрах ионы меди, марганца, железа и других металлов);
Нуклеопротеиды, содержащие нековалентно связанные ДНК или РНК. К нуклеопротеидам относится хроматин, из которого состоят хромосомы;
Фосфопротеины, содержащие в качестве простетической группы ковалентно связанные остатки фосфорной кислоты. В образовании сложноэфирной связи с фосфатом участвуют гидроксильные группы серина, треонина и тирозина. Фосфопротеином, в частности, является казеин молока[23];
Хромопротеиды, содержащие окрашенные простетические группы различной химической природы. К ним относится множество белков с металлсодержащей порфириновой простетической группой, выполняющие разнообразные функции: гемопротеины (белки, содержащие в качестве простетической группы гем, например, гемоглобин и цитохромы), хлорофиллы, флавопротеиды с флавиновой группой и др.
Аденозинтрифосфа́т (сокр. АТФ, англ. АТР) — нуклеотид, играет исключительно важную роль в обмене энергии и веществ в организмах; в первую очередь соединение известно как универсальный источник энергии для всех биохимических процессов, протекающих в живых системах. АТФ был открыт в 1929 году Карлом Ломанном[1], а в 1941 году Фриц Липман показал, что АТФ является основным переносчиком энергии в клетке[2].
Главная роль АТФ в организме связана с обеспечением энергией многочисленных биохимических реакций. Являясь носителем двух высокоэнергетических связей, АТФ служит непосредственным источником энергии для множества энергозатратных биохимических и физиологических процессов.
азотистое основание – аденин, углевод – рибоза и три остатка фосфорной кислоты.
Аденин – рибоза – Ф.К. – Ф.К. – Ф.К.
При использовании АТФ в качестве источника энергии обычно происходит отщепление путем гидролиза последнего остатка фосфорной кислоты.
АТФ + Н2О → АДФ + Н3РО4 + энергия
В физиологических условиях, то есть при условиях, которые имеются в живой клетке, расщепление моля АТФ сопровождается выделением 10 – 12 ккал энергии (43 -50 кДж).
Главными потребителями энергии АТФ в организме являются
реакции синтеза;
мышечная деятельность;
транспорт молекул и ионов через мембраны.
