
29. гетероциклы IV
.doc|
Лекция 29 |
ГЕТЕРОЦИКЛЫ IV
ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С НЕСКОЛЬКИМИ
ГЕТЕРОАТОМАМИ
ДИАЗИНЫ
ПИРИМИДИН

Наиболее важный из диазинов.
Пиримидин – низкоплавкое кристаллическое вещество, хорошо растворимое в воде.
По химическим свойствам – это ароматическое соединение, аналогичное пиридину, обладающее основными свойствами и более π-дефицитное:

Нуклеофилы атакуют пиримидиновое кольцо в места с наименьшей электронной плотностью – 2, 4, 6; электрофилы – в положение 5, имеющее относительно более высокую электронную плотность. Электрофильные реакции затруднены из-за в целом пониженной π-электронной плотности, а нуклефильные – наоборот облегчены:

У всех 2-, 4- и 6-оксипиримидинов водороды ОН-групп подвижны и способны к таутомерным переходам:

Различные способы получения пиримидиновых соединений можно объединить следующей схемой:

Получение барбитуровой кислоты и её производных

5,5-дизамещенные производные барбитуровой кислоты тормозят дыхательную ОВ- цепь в митохондриях и применяются как лекарственные препараты противосудорожного и снотворного действия (барбитураты).
Барбитуровая кислота и барбитураты – кислоты, образующие устойчивые соли с 1 эквивалентом щелочи:

В отличие от самих барбитуратов их натриевые соли хорошо растворимы в воде, что важно для лекарственного применения. Смесь барбитала и его натриевой соли применяется как рН-буферная смесь (вероналовый буфер).
НУКЛЕИНОВЫЕ ОСНОВАНИЯ – ПРОИЗВОДНЫЕ ПИРИМИДИНА
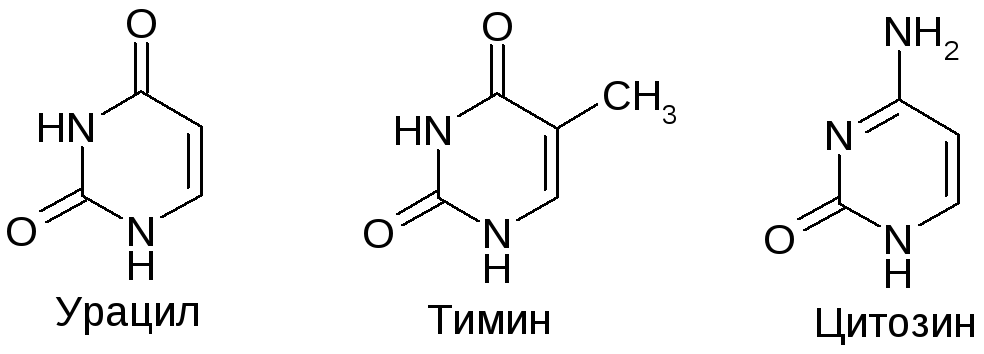
Получение производных урацила
Конденсация циануксусного эфира с мочевиной дает 6-аминоурацил (синтез Траубе):

Конденсация ацетоуксусного эфира с мочевиной дает 6-метилурацил, последний при окислении азотной кислотой превращается в оротовую кислоту:

Оротовая кислота – природный метаболит, участвующий в биосинтезе пиримидиновых нуклеиновых оснований. Калиевая соль её (оротат калия) используется как лекарственный препарат.
Многие производные урацила используются как лекарственные препараты. Они являются химическими аналогами урацила и тимина и их биологическими антагонистами: вмешиваясь в метаболические реакции, они замещают урацил и тимин, прерывая цепь биосинтеза нуклеиновых кислот и подавляют, таким образом, рост и развитие опухолевых клеток:

Другие природные и лекарственные вещества,
содержащие пиримидиновый цикл

БЕНЗОПИРИМИДИН (ХИНАЗОЛИН)
При конденсации о-аминобензальдегида с формамидом образуется бициклическая структура бензопиримидина:

Многие производные хиназолина обладают биологической активностью и используются как лекарственные препараты, например, адреноблокатор празозин:

ПИРИДАЗИН, ПИРАЗИН

Пиридазины
Образуются при конденсации малеинового ангидрида и его производных с гидразином:

Пример реакций пиридазина:

Пиперазины
При нагревании α-аминокислот происходит их димеризация (самоацилирование) с образование производных пиперазина:

Пиперазины также могут быть получены по методу Гофмана:

По химическим свойствами пиперазин – это типичный вторичный амин с высокой основностью.
Фрагменты пиперазина часто встречаются в лекарственных веществах, например, антибиотики фторхинолоны, препарат, действующий на мозговое кровообращение, циннаризин и др.:

ОКСАЗИН, ФЕНОКСАЗИН

Феноксазин легко окисляется в феноксазинон-3, последний может быть получен конденсацией о-аминофенола и бензохиноном:

Цикл феноксазина составляет основу структуры антибиотиков-цитостатиков актиномицинов:

ТИАЗИН, ФЕНОТИАЗИН

При взаимодействии дифениламина с серой при нагревании замыкается цикл тиазина:

Структура фенотиазина лежит в основе многочисленного ряда психотропных лекарственных препаратов (нейролептики):

Антибиотики цефалоспорины – аналоги пенициллинов – содержат гидрированный цикл 1,5-тиазина:

ЛИТЕРАТУРА:
Основная
1. Тюкавкина Н.А., Зурабян С.Э., Белобородов В.Л. и др. – Органическая химия (специальный курс), кн.2 – Дрофа, М., 2008 г., с. 68-77.
2. Н.А.Тюкавкина, Ю.И.Бауков – Биоорганическая химия – ДРОФА, М., 2007 г., с. 304-309.
Дополнительная
2. В.Г.Беликов – Фармацевтическая химия – МЕДпресс-информ, М., 2007 г., с. 511-534.
02.10.09
