
- •Электротехническое материаловедение
- •Домены в ферро и ферримагнетиках
- •Магнитнотвердые магнетики
- •Металлы с высокой проводимостью используются при конструировонии различных электротехнических приборов и устройств Материалы, используемые как нагревательные элементы
- •Сверхпроводящие материалы (металлы, керамика)
- •Металлы
Домены в ферро и ферримагнетиках
Внутренняя энергия ферромагнетика:
EВН= EКР – ЕОБ+ ЕМАГ
ЕОБ= -2АSiSj не зависит от Na
ЕМАГ= (Pa)2Na/ra3
Na – число атомов
Pa – магнитный момент атомa
Тогда при большом Na ЕМАГ> ЕОБ
и ферромагнитное состояние данного объема
становится не выгодным.
Происходит
разбиение объема на домены.
ЕМАГ=1 ЕМАГ=1/2 ЕМАГ 0
Существуют направления легкого намагничивания
Fe – ребра куба ОЦК-решетка
Со – ось гексагональной решетки
Ni – диагонали куба ГЦК
Намагниченность и петля гистерезис

μ=B/H
Динамическая μ - начальная (μа) при Н ≈ 0,001э,
максимальная (μмах) – при насыщении
Область упруго смещения границ доменов
Область неупругого роста доменов с магнитными моментами,
близкими к направлению Н
3. Область неупругового поворота моментов доменов


B
BS
H

HC
Магнитномягкие магнетики

HC= 0,004 Э ≤ 0.1 А/м,
Техническое железо (μа=250, μмах=7000, Нс=0,8э ), железо-никелевые сплавы – пермаллои (высоколегированные - 79НМ - μа=22000, μмах=120000, Нс=0,02э); пермаллои низколегированные ( 42НС: μа=2500, μмах=25000, Нс=0,1э); альсифер (μа=20000, μмах=117000, Нс=0,02э); магнито-стрикционные материалы – пермендюр (железо-кобальтовый сплав)
Используют для статоров и роторов электромашин, магнитопроводов электромагнитных устройств (трансформаторы, дроссели, реле и т.д.).
Магнитнотвердые магнетики
HC ≈ (103-104) Э
Альни АН1, АН2…(Вr ≈ 5000гс, Нс≈500э); альниси (Вr ≈ 4000гс, Нс≈750э;
альнико (Вr ≈ 7000-12000гс, Нс≈600э)
Магнитодиэлектрики – высокочастотные магнито-мягкие материалы – прессованные порошки ферромагнетика (карбонильное железо, альсифер) со связкой (полимер, стекло); μэфф≈50
Ферриты
Кристаллы окислов металлов
Магнитные свойства определяются
магнит моментами металлов
Кристаллы ферритов состоят из Fe2O3 и МеО
Хим. формула: МеFe2O4
Две разновидности кристаллов-ферритов:
кристаллы типа шпинели
кристаллы типа граната
Кристаллы шпинели состоят из 8формульных единиц
– 56 ионов-32 иона кислорода, Ме+2-8, Fe+3-16
Особенности ферритов:
- малые: обменное взаимод-вие между Fe+3, BS, Br, TC, μ
- высокое электрическое сопротивление
- высокочастотный материал
Характеристики ферро и ферри-магнетиков
|
магнетик |
Тс 0С |
Br Tл |
Hc Э |
μотн |
применение |
|
Fe Пермаллой (Ni-Fe) Мар.цинк феррит Со-Pt ЮНДК Fe,Ni, Al Феррит бария Магнитомягкие ферриты Ф, окифер
|
770 500 300 1000 800 450
μа=20-2000 |
0,8 1,4 0,5 0,8 1,4 0,4
0,1-1,0 |
<1 <1 <1 5000 3000 2000
|
5000 10000 2500 5000 10000 2500 |
Эл.машины,трансф.
Пост магниты, запомин устройства |
Раздел 3
Проводниковые материалы
Зонная теория твердого тела
Основные положения
ЗТТТ описывает поведение
валентных электронов в кристаллах
Эта теория позволяет понять
электрические, тепловые, магнитные
свойства твердых тел
Для теоретического исследования
Системы микрочастиц необходимо
решить уравнение Шредингера
Это дифференциальное уравнение
второго порядка
Уравнение содержит столько переменных,
сколько степеней свободы имеет система
Для двухчастичной задачи - 6 переменных,
Для трехчастичной задачи - 9 переменных,
Объектом физики твердого тела
Является система из всех электронов и атомов,
составляющих кристалл
В одном см3 содержится ~1022атомов,
поэтому число переменных
в уравнении Шредингера для кристалла
составляет величину порядка 1023
Такое число уравнений не в силах
решить ни одна ЭВМ
Прямое решение невозможно,
поэтому квантовая теория твердого тела
основывается на следующих допущения:
1. Атомные ядра неподвижны
по сравнению с электронами
2. Расположение атомов строго периодично
3. Электрон движется в силовом поле,
учитывающем все взаимодействия
4. Рассматриваются только валентные электроны.
Электроны внутренних оболочек и ядра
составляют атомные остовы
Волновая функция
валентных электронов в кристалле
(блоховская функция)
Взаимодействие валентных электронов
с атомными остовами описывается
периодическим потенциалом U (r)

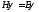
Уравнение Шредингера
для электрона в поле U (r):
101\* MERGEFORMAT (.)


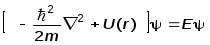 (1)
(1)

Решение (1) есть волновая функция,
заданная теоремой Блоха:
Волновая функция электрона,
движущегося в периодическом поле
есть плоская модулированная волна:
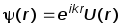 (2)
(2)
Функция Блоха
Энергетические зоны электронов
в кристаллах
Электроны в атоме занимают дискретные уровни
(1S,2S,2P,3S,….)
Для двухатомных молекул (O2,N2)
Каждый атомный уровень расщепляется на два подуровня,
образуя две молекулярные орбитали.
В кристалле N-атомов, каждый атомный уровень расщепляется
в зону разрешенных состояний, число которых N
Таким образом, энергетический атомный уровень Еа
в кристалле расщепляется в зону разрешенных состояний

}
Дисперсионные кривые для
валентных электронов в кристалле
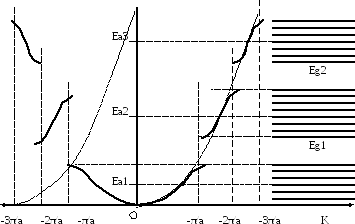
Причина возникновения
запрещенных зон в кристаллах
Для свободного электрона
дисперсионная кривая-
непрерывная парабола
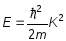 ;
;
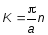
Для электрона в кристалле
возникают запрещенные зоны
Эффективная масса электрона
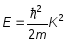
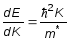
 -
эффективная масса электрона-
-
эффективная масса электрона-
определяет скорость движения волны,
описывающей микрочастицу
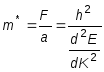

Валентные электроны мигрируют
между атомными остовами
под действием обобщенного потенциала.
Электроны движутся со скоростью,
пропорциональной эффективной массе
Учитывая корпускулярно-волновой дуализм,
движение электрона рассматривается
как распространение волны.
В этом случае имеет место
дифракция электронов на атомных рядах
и отражение волн от атомных рядов.
Условие отражения волны
от атомного ряда:
Условие Вульфа-Брегга



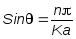
Полное отражение наблюдается при
 и
и
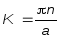
при этом V=0,
то есть электрон не движется
и обладает бесконечной массой
Следовательно вблизи границ
разрешенных зон имеем полное отражение электронных волн – в этой области эффективная масса электрона становится бесконечной, т.е. электрон здесь находиться не может.
Так возникают запрещенные зоны.
Зонная структура металлов,
полупроводников, диэлектриков
Рассмотрим атом,
валентные электроны которого
могут находиться в двух состояниях:
основном ЕА и возбужденном ЕА*

Зона проводимости
Валентная зона
Диэлектрик

Полупроводник

Металл
Понятие дырки
Е
ЗП










ВЗ










Под действием внешнего возбуждения
электрон из валентной зоны
переходит в зону проводимости
Отсутствие электрона в валентной зоне
называется дыркой
Дырка-антипод электрона
Проводники
Общие представления
об электропроводности вещества
Закон Ома в дифференциальной форме:
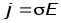
Удельная объемная проводимость (σ)
является характеристикой материала
и представляет собой
коэффициент пропорциональности
между плотностью тока
и напряженностью электрического поля
Удельное электрическое
сопротивление есть величина,
обратная удельной объемной проводимости:
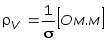
Получим общее выражение
для удельной проводимости
любого вещества.
Введем обозначения:
n – число носителей заряда
в единице объема материала,
q – заряд носителей заряда
Vg- скорость дрейфа
носителя заряда в электрическом поле
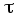 ,
,
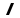 -
соответственно
-
соответственно
время и длина свободного пробега
носителя заряда
V – скорость движения носителя заряда,
определяемая его кинетической энергией
Поэтому:
 (3)
(3)
Cравнивая (1) и (3) имеем:

Здесь
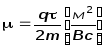 -
-
подвижность носителей заряда
m – масса носителя.
подвижность носителей заряда-
одна из важнейших
характеристик электропереноса-
равняется скорости движения
носителя заряда в единичном
электрическом поле
Удельная объемная проводимость
Вещества равна произведению
Концентрации, подвижности
и заряда носителей заряда

Понятие проводников
Проводники первого рода –носитель электроны и дырки
Проводники второго рода – носители ионы
Электропроводность металлов
Основы зонной теории металлов
В соответствии с законами
квантовой механики энергия электронов
в твердых телах может иметь
значения внутри зон
разрешенных состояний,
разделенных запрещенной зоной
Валентные электроны формируют
валентную зону,
которая отделена от зоны проводимости
запрещенной зоной.
Число уровней в зоне равно
числу атомов в крисалле
и составляет ~1022см3
В соответствии с принципом Паули
На каждом уровне может находиться
не более двух электронов
с разными спинами
В диэлектриках и полупроводниках
валентные зоны заполнены полностью
и для создания
свободных электронов (носителей заряда)
необходимо затратить энергию,
равною ширине запрещенной зоны
Для металлов – другая картина:
Валентная зона либо заполнена не полностью,
либо перекрывается с валентной зоной
Это обуславливает
высокую проводимость металлов
Энергетика валентных
электронов в металлах
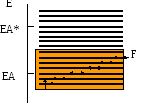
Для уровня Ферми имеем:
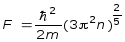
- вероятность заполнения
уровня электроном
Состояния, выше F свободны,
а состояния ниже F заняты
Классическая теория
электропроводности металлов
(теория Друде)
Свободные электроны
представляют собой классические частицы-
электронный газ
Носители заряда подчиняются
статистике Больцмана:
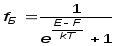
Это значит, что все электроны имеют
одинаковую энергию и скорость (VСР)
Вернемся к формуле для ϭ:
 (6)
(6)
Все свободные электроны
Принимают участие в электропереносе
Теория не согласуется с
экспериментом
Квантовая теория
электропроводности металлов
(теория Зоммерфельда)
Положения теории;
Свободные электроны в металлах-
квантовые частицы подчиняются
статистике Ферми-Дирака
В электропроводности принимает
участие только небольшая часть
свободных электронов, у которых E~F
В соответствии с теорией Зоммерфельда,
электропроводность металлов равна:

Так как
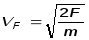 ,
,
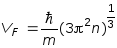
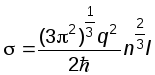

Температурная зависимость
Электропроводности металлов
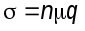
С ростом Т, σ уменьшается за счет уменьшения μ,
так как концентрация носителей тока в металлах
от температуры не зависит
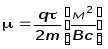 =
gl/2mvF
=
gl/2mvF
μ уменьшается при нагревании
в результате столкновений носителей заряда
с атомами и дефектами структуры
Проводники первого рода делятся на
Проводники 1-го рода с высокой и низкой проводимостью
Значения удельного сопротивления металлов
|
|


