
- •Глава 9. Физико-химические
- •9.1. Анализ состава газовой фазы в зоне столба дуги
- •9.1.2. Образование соединений между компонентами газовой смеси
- •9.1.3. Насыщение расплавленного металла газами в капле и сварной ванне
- •9.2. Влияние атмосферных газов на свойства стали и сплавов при сварке
- •9.2.1. Влияние кислорода на свойства стали
- •9.2.3. Влияние водорода на свойства стали
- •9.2.4 Влияние со2, со и паров н2о на свойства стали
- •9.2.5. Влияние атмосферных газов на свойства цветных металлов
- •9.3. Взаимодействие металла с защитными флюсами при сварке
- •9.3.1. Строение и свойства сварочных флюсов
- •9.3.2. Характеристика важнейших простых оксидов, входящих в состав шлаковой фазы
- •9.3.3. Основные системы сварочных шлаков
- •9.4. Массообмен между расплавленным металлом, газовой средой и шлаком
- •9.5. Расплавление электрода и перенос капель в ванну
- •9.6. Источники водорода при сварке под флюсом
- •9.7. Окисление металла шва флюсом
- •9.8. Переход вредных примесей из флюса в металл шва
- •9.9. Раскисление металла при сварке
- •9.9.1. Виды раскисли тельных процессов
- •9.9.2. Легирование наплавленного металла
- •9.10. Рафинирование сварочной ванны и модифицирование металла шва
- •9.10.1. Влияние серы на структуру и свойства шва
- •9.10.2. Десульфурация сварочной ванны
- •9.10.3. Снижение содержания фосфора в металле шва
- •9.11. Дефекты металлургического происхождения в сварных швах
- •9.11.2. Шлаковые включения в металле шва
- •9.11.3. Ликвационная неоднородность в металле шва
9.7. Окисление металла шва флюсом
Присутствие кислорода в газовой фазе флюсовой полости обусловлено в основном тем, что:
-на поверхности металла свариваемых кромок имеются оксиды (окалина Fe3О4 и ржавчина Fe2О3·2H2О), диссоциирующие при дуговом нагреве (с выделением свободного кислорода) или вступающие с жидким железом в реакции:
(9.43а)
 (9.436)
(9.436)
-во флюсе есть воздух и влага, диссоциирующая при сварке и взаимодействующая с жидким железом по реакции
![]() (9.44а)
(9.44а)
-при дуговой сварке происходит выделение на аноде кислорода по реакции
![]() (9.446)
(9.446)
а на катоде - водорода по реакции
![]() (9.45)
(9.45)
Кроме того, кислород попадает в жидкий металл ванны при прямом взаимодействии Feж с химически активными оксидами жидких шлаков в результате обменных реакций, например
![]() (9.46)
(9.46)
Таким образом, в шлаке возникает закись железа FeO, которая растворима в жидком железе. Если оксид, растворимый в металле, образуется во флюсе-шлаке, то между концентрациями этого оксида согласно закону распределения Нернста устанавливается определенное соотношение
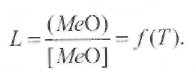 (9.47)
(9.47)
В результате реакции (9.46) жидкий металл одновременно окисляется и легируется (обычно кремнием или марганцем). Термодинамический расчет, подтверждающий ход этих реакций в указанных направлениях дан в гл. 8 (пример 8.3). Таким образом, кремнемарганцевые шлаки, имеющие большее количество кислотных оксидов (%SiO2 > % МnО), окисляют капли электродного металла при высоких температурах (т. е. осуществляется первая стадия кремнемарганцевого процесса). Поэтому они считаются активными. Наряду с окислением капли кремнемарганцевые шлаки обогащают металл кремнием и марганцем, которые, попадая в более холодный металл сварочной ванны, вызывают процессы раскисления.
Если в электродном металле содержатся легирующие элементы с большим сродством к кислороду, чем у железа, то происходит их необратимое окисление при взаимодействии с SiO2 и МnО. Поэтому при сварке легированных и высоколегированных сталей недопустимо применение кремнемарганцевых флюсов, которые хотя и имеют хорошие сварочно-технологические свойства, но весьма активны, так как содержат термически малопрочные оксиды SiO2 и МnО, выделяющие кислород в обменных реакциях.
Ввод термически более стойких кислотных оксидов AI2O3 и TiO2 позволяет несколько снизить активность флюсов, но вызывает другие реакции окисления (с участием углерода и кремния) и восстановление алюминия и титана, переходящих в металл шва из флюсов. Однако окисление AI2O3 и TiO2 происходит при более высоких температурах и по более сложной схеме:
восстановление алюминия и титана из AI2O3 и ТiO2 кремнием;
окисление легирующих элементов (С, Si, Mn, Сг) кислородом, выделяющимся при частичной диссоциации AI2O3 и ТiO2;
образование в наплавленном металле остаточного кислорода (входившего в состав AI2O3 и ТiO2), т. е. создаются включения.
Такой же результат имеет место при вводе кислотного оксида ZrO2. Итак, с увеличением количества кислотных термостойких оксидов в составе флюса (AI2O3, ZrO2, ТiO2) усиливаются процессы окисления легирующих элементов (Cr, Si, Mn, Nb) и восстанавливаются металлы Zr, Al, Ti из их оксидов. При этом растет общее содержание кислорода, а содержание других ферритизаторов и ферритной фазы уменьшается. Термодинамические расчеты, выполненные Н.Н. Потаповым, показали, что окисление хрома Сг и наиболее эффективного ферритизатора и стабилизатора ферритной фазы в аустените - ниобия Nb происходит с участием диоксида кремния SiO2, а также его монооксида SiO по следующим реакциям:
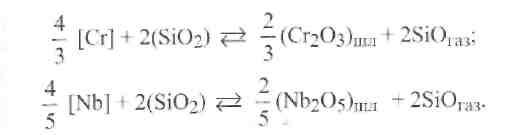
Присутствие неметаллических включений снижает сопротивляемость металла шва образованию горячих трещин, коррозионную стойкость швов и пластичность сварных соединений высоколегированных сталей.
В отличие от кислотных оксидов основные оксиды (CaO, MgO) обладают достаточной химической стойкостью во всем диапазоне сварочных температур, но не обеспечивают необходимые технологические свойства. Из работ Б.Н. Бадьянова следует, что составы флюсов для высоколегированных сталей должны создаваться на основе компромисса, причем рекомендуется, чтобы содержание главного окислителя SiO2 составляло не более 10 %, что позволит полностью связать его основными оксидами в комплексы SiO2 • СаО и т. п.
