
- •Ковалентная связь
- •Метод валентных связей
- •Сигма (s) и пи (p)-связи
- •Донорно-акцепторная связь
- •Свойства ковалентной связи
- •Полярные и неполярные молекулы
- •Относительная электроотрицательность атомов
- •2,7 Д 2,7 д
- •Ионная связь
- •Гибридизация атомных орбиталей
- •Гибридизация орбиталей и пространственная конфигурация молекул
- •Металлическая связь
- •Водородная связь
- •Типы кристаллических решеток
- •Валентность
- •Степень окисления
Лекция 3
Химическая связь и строение молекул
Учение о химической связи – центральный вопрос современной химии. Без него нельзя понять причины многообразия химических соединений, механизм их образования, строение и реакционную способность.
Образование молекул из атомов приводит к выигрышу энергии, так как в обычных условиях молекулярное состояние устойчивее, чем атомное. Учение о строении атомов объясняет механизм образования молекул, а также природу химической связи.
У атома на внешнем энергетическом уровне может содержаться от одного до восьми электронов. Если число электронов на внешнем уровне атома максимальное, которое он может вместить, то такой уровень называется завершенным. Завершенные уровни характеризуются большой прочностью. Таковы внешние уровни атомов благородных газов: у гелия на внешнем уровне два электрона (s2), у остальных – по восемь электронов (ns2np6). Внешние уровни атомов других элементов незавершенные и в процессе химического взаимодействия они завершаются. Чтобы добиться этого состояния соответствующим атомам приходится разменивать свои электроны. И, как часто случается в жизни, «те, которые имеют меньше, отдают тем, кто имеет больше».
Ковалентная связь
В 1907 г. Н.А. Морозов и позднее в 1916-1918 г.г. американцы Дж. Льюис и И. Ленгмюр ввели представление об образовании химической связи общей электронной парой и предложили обозначать валентные электроны точками

Связь, образованная электронами, принадлежащими двум взаимодействующим атомам, называется ковалентной. По представлениям Морозова-Льюиса-Ленгмюра:
при взаимодействии атомов между ними формируются поделенные – общие – электронные пары, принадлежащие обоим атомам;
за счет общих электронных пар каждый атом в молекуле приобретает на внешнем энергетическом уровне восемь электронов, s2p6;
3) конфигурация s2 p6 – это устойчивая конфигурация инертного газа и в процессе химического взаимодействия каждый атом стремится ее достигнуть;
4) количество общих электронных пар определяет ковалентность элемента в молекуле и равно оно числу электронов у атома, недостающих до восьми;
5) валентность свободного атома определяется числом неспаренных электронов.
Изображать химические связи принято по разному:
с помощью электронов в виде точек, поставленных у химического символа элемента. Тогда образование молекулы водорода можно показать схемой
Н× + Н× ® Н : Н;
с помощью квантовых ячеек (орбиталей) как размещение двух электронов с противоположными спинами в одной молекулярной квантовой ячейке
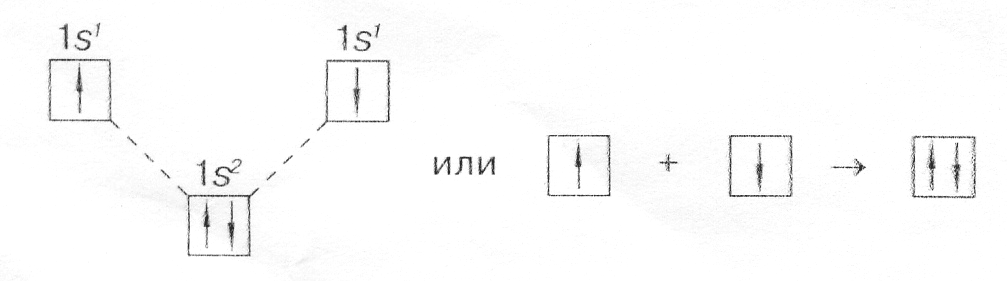
Схема расположения, показывает, что молекулярный энергетический уровень ниже исходных атомных уровней, а значит, молекулярное состояние вещества более устойчиво, чем атомное;
часто, особенно в органической химии, ковалентную связь изображают черточкой (например, Н-Н), которая символизирует пару электронов.
Ковалентная связь в молекуле хлора также осуществляется с помощью двух общих электронов, или электронной пары.

Как видно, каждый атом хлора имеет три неподеленные пары и один неспаренный электрон. Образование химической связи происходит за счет неспаренных электронов каждого атома. Неспаренные электроны связываются в общую пару электронов, называемую также поделенной парой.
Метод валентных связей
Представления о механизме образования химической связи на примере молекулы водорода распространяются и на другие молекулы. Теория химической связи, созданная на этой основе, получила название метода валентных связей (МВС). Основные положения:
1) ковалентная связь образуется в результате перекрывания двух электронных облаков с противоположно направленными спинами, причем образованное общее электронное облако принадлежит двум атомам;
2) ковалентная связь тем прочнее, чем в большей степени перекрываются взаимодействующие электронные облака. Степень перекрывания электронных облаков зависит от их размеров и плотности;
3) образование молекулы сопровождается сжатием электронных облаков и уменьшением размеров молекулы по сравнению с размерами атомов;
4) в образовании связи принимают участие s- и p-электроны внешнего энергетического уровня и d-электроны предвнешнего энергетического уровня.
Сигма (s) и пи (p)-связи
В молекуле хлора каждый его атом имеет завершенный внешний уровень из восьми электронов s2 p6 , причем два из них (электронная пара) в одинаковой степени принадлежит обоим атомам. Перекрывание электронных облаков при образовании молекулы показано на рисунке
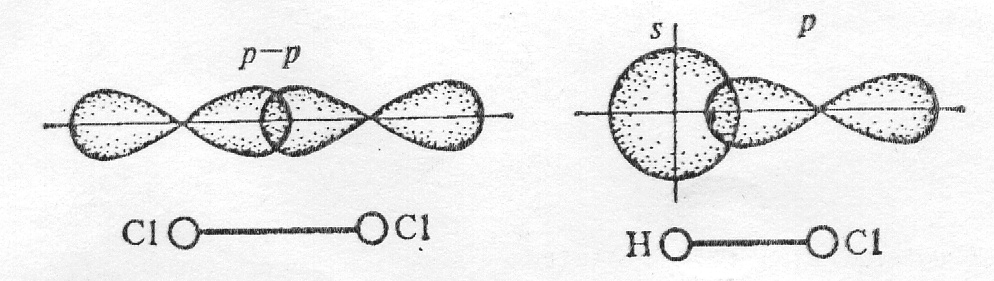
а б
Схема образования химической связи в молекулах хлора Cl2 (а) и хлороводорода HCl (б)
Химическая связь, для которой линия, соединяющая атомные ядра, является осью симметрии связывающего электронного облака, называется сигма (σ)-связью. Она возникает при «лобовом» перекрывании атомных орбиталей. Связи при перекрывании s-s-орбиталей в молекуле Н2; р-р-орбиталей в молекуле Cl2 и s-p-орбиталей в молекуле НСl являются сигма связями. Возможно «боковое» перекрывание атомных орбиталей. При перекрывании р-электронных облаков, ориентированных перпендикулярно оси связи, т.е. по оси у- и z-осям, образуются две области перекрывания, расположенные по обе стороны от этой оси. Такая ковалентная связь называется пи (p)-связью. Перекрывание электронных облаков при образовании π-связи меньше. Кроме того, области перекрывания лежат дальше от ядер, чем при образовании σ-связи. Вследствие этих причин π-связь обладает меньшей прочностью по сравнению с σ-связью. Поэтому энергия двойной связи меньше удвоенной энергии одинарной связи, которая всегда является σ-связью. Кроме того, σ-связь имеет осевую, цилиндрическую симметрию и представляет собой тело вращения вокруг линии, соединяющей атомные ядра. π-Связь, наоборот, не обладает цилиндрической симметрией.
Одинарная связь всегда является чистой или гибридной σ-связью. Двойная же связь состоит из одной σ- и одной π-связей, расположенных перпендикулярно друг относительно друга. σ-Связь прочнее π-связи. В соединениях с кратными связями обязательно присутствует одна σ-связь и одна или две π-связи.
