
- •1 Правила оформления лабораторной работы
- •2 Техника безопасности при работе в химической лаборатории
- •2.1 Общие правила работы в лаборатории химии
- •2.2 Первая помощь при травмах и отравлениях
- •Контрольные вопросы и задания
- •Обработка результатов опыта
- •Контрольные вопросы и задачи
- •Контрольные вопросы
- •5 Термохимия
- •1 Стадия -кДж;
- •2 Стадия -кДж.
- •Обработка результатов опыта
- •Контрольные вопросы
- •1 Химическая кинетика
- •Контрольные вопросы
- •2 Теория растворов
- •3 Теория электролитической диссоциации
- •Контрольные вопросы и задания
- •1.1 Окислительно-восстановительные реакции
- •1.1.1 Степень окисления
- •1.1.2 Сущность окисления-восстановления
- •1.1.3 Окислительно-восстановительные свойства элементов в зависимости от строения их атомов
- •1.1.4 Важнейшие окислители и восстановители
- •1.1.5 Типы окислительно-восстановительных реакций
- •1.1.6 Составление уравнений окислительно-восстановительных реакций
- •1.2 Гальванический элемент
- •1.3 Коррозия
- •1.4 Электролиз
- •1.4.1 Электролиз водного раствора хлорида меди
- •1.4.2 Электролиз водного раствора сульфата натрия
- •1.4.3 Электролиз водного раствора сульфата меди с медным анодом
- •Опыт 3. Восстановительные свойства отрицательных ионов галогенов.
- •Контрольные вопросы
- •Литература
3 Теория электролитической диссоциации
3.1 Электролитическая диссоциация.Электролитами, то есть проводниками второго рода, называются вещества, которые в расплавленном или растворённом состоянии проводят электрический ток за счет движения ионов. Электролитами являются водные растворы солей, кислот и оснований, молекулы которых под действием растворителя диссоциируют на ионы.
![]()
![]()
Количественно процесс диссоциации характеризуется некоторыми величинами, например, степенью электролитической диссоциации α и константой электролитической диссоциации, К.
Число, показывающее какая часть растворённого электролита находится в растворе в виде ионов, называется степенью электролитической диссоциации и выражается в %.
Электролиты считаются сильными, если значение α в их децинормальном состоянии раствора более 30 % и слабыми, если α меньше 30%.
Сильные электролиты диссоциируют практически полностью. В растворах слабых электролитов имеются и молекулы, и ионы растворённого вещества. Следовательно, диссоциация слабых электролитов представляет обратимый процесс, в результате которого устанавливается равновесие, подчиняющееся закону действия масс.
![]()
Количественно это равновесие можно характеризовать константой равновесия, которая рассчитывается по формуле 17.
![]()
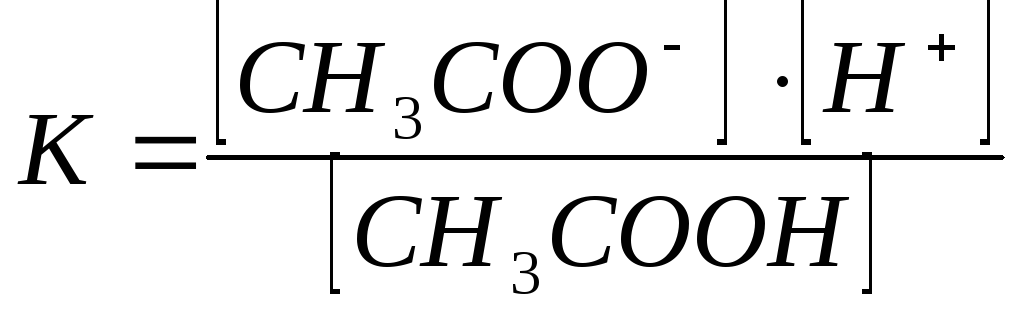 .
(17)
.
(17)
Константа равновесия в таких случаях называется константой электролитической диссоциации. Эта величина есть отношение произведения концентрации ионов к концентрации недиссоциированных молекул. Чем больше способность электролита к диссоциации, тем больше значение константы. Константа диссоциации не зависит от концентрации раствора и при постоянной температуре есть величина постоянная.
Связь
между константой диссоциации К и степенью
диссоциации электролита
![]() ,
распадающегося на два иона, описывается
законом разбавления Оствальда (формула
18)
,
распадающегося на два иона, описывается
законом разбавления Оствальда (формула
18)
![]() .
(18)
.
(18)
Если α
мала, то 1 – α ≈ 1 и тогда К = α2∙
С, откуда![]() .
.
Отсюда видно, что с уменьшением концентрации электролита в растворе степень электролитической диссоциации возрастает.
При введении в раствор слабого электролита какого-либо сильного электролита, образующего в результате диссоциации ионы, одинаковые с одним из ионов слабого (одноимённые ионы), равновесие смещается (в соответствии с принципом Ле-Шателье) в сторону образования недиссоциированных молекул слабого электролита. Например, введя ацетат натрия в раствор уксусной кислоты, мы тем самым увеличиваем концентрацию ионов CH3COO-.
![]()
Следовательно, равновесие между молекулами уксусной кислоты и её ионами сместится влево,
![]()
то есть в сторону образования недиссоциированных молекул СН3СООН. Одновременно уменьшается концентрация ионов Н+. Таким образом, степень диссоциации уксусной кислоты уменьшается. Добавление к раствору ионов ОН-, связывающих ионы Н+в недиссоциированные молекулы воды, вызовет диссоциацию кислоты и увеличение концентрации ионов СН3СОО-, то есть сместит равновесие вправо.
В растворах электролитов перенос электричества осуществляется за счёт ионов. Способность электролита пропускать электрический ток можно характеризовать его электропроводностью. Растворы электролитов обладают ионной электропроводностью.
Электропроводность
любых материалов, в том числе и растворов,
рассматривается как величина обратная
сопротивлению. За единицу электропроводности
в системе СИ принят Сименс
![]() .
.
Электропроводность растворов электролита определяется количеством ионов, которые перейдут через площадь поперечного сечения раствора в единицу времени. Это количество в основном зависит от числа ионов, находящихся в растворе в единице объёма (то есть от концентрации ионов), скорости их перемещения, заряда ионов, температуры раствора.
Величина, обратная удельному сопротивлению, называется удельной электропроводностью. Она численно равна электропроводности 1м3исследуемого раствора в единицах (Ом-1· м-1) или (См · м-1) в системе СИ.
С увеличением концентрации раствора электролита электропроводность его растёт и достигает при некоторой концентрации максимальное значение, а затем начинает падать. Такая зависимость объясняется тем, что при малых концентрациях растворов электролитов число ионов в единице объёма раствора мало и, так как ток переносится ионами, мала электропроводность раствора.
По мере увеличения концентрации раствора, растёт число ионов в единице объёма раствора и соответственно растёт электропроводность. Однако при достижении определённой концентрации раствора электропроводность начинает падать, потому что у сильного электролита возрастает влияние межионных сил, в результате чего усиливается торможение ионов, а у слабых - уменьшается степень диссоциации.
3.2 Гидролиз.Гидролиз – обменное взаимодействие ионов соли с молекулой воды, в результате которого смещается равновесие электролитической диссоциации воды.
П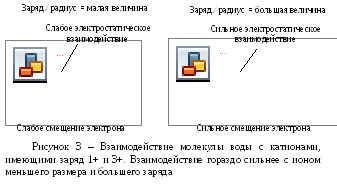 оскольку
ионы металлов несут на себе положительные
заряды, они притягивают к себе неподеленные
электронные пары молекул воды. Это
взаимодействие, называемое гидратацией,
и является главной причиной растворения
солей металлов в воде. Сила притяжения
возрастает с увеличением заряда на ионе
металла и с уменьшением его размеров.
Хорошей мерой прочности гидратации
служит отношение ионного заряда к
ионному радиусу. Когда молекула воды
взаимодействует с положительно заряженным
ионом металла, электронная плотность
оттягивается от атома кислорода, как
показано на рисунке 3.
оскольку
ионы металлов несут на себе положительные
заряды, они притягивают к себе неподеленные
электронные пары молекул воды. Это
взаимодействие, называемое гидратацией,
и является главной причиной растворения
солей металлов в воде. Сила притяжения
возрастает с увеличением заряда на ионе
металла и с уменьшением его размеров.
Хорошей мерой прочности гидратации
служит отношение ионного заряда к
ионному радиусу. Когда молекула воды
взаимодействует с положительно заряженным
ионом металла, электронная плотность
оттягивается от атома кислорода, как
показано на рисунке 3.
Смещение электронной плотности приводит к усилению поляризации связи О-Н, и в результате молекула воды, связанная с ионом металла, становится более кислой, чем молекулы воды в толще растворителя. Вследствие этого гидратированный ион металла обладает свойствами источника протонов.
Анионы связаны с молекулами воды водородной связью. Сильное влияние аниона на протон может привести к полному отрыву последнего от молекулы воды.
В зависимости от силы поляризующего влияния Кn+и Аn-на молекулуH2O, будут получаться различные результаты.
Обычно различают четыре случая взаимодействия воды и соли.
1 Соль образована сильным основанием и сильной кислотой, где катионы и анионы имеют небольшие заряды и значительные размеры. Поляризующее действие таких ионов на молекулы воды невелико, то есть взаимодействие соли с H2Oпрактически не происходит. Иными словами соли сильного основания и сильной кислоты гидролизу не подвергаются. Примеры:KNO3,KCl,NaNO3и другие. рН среды раствора примерно равен 7.
2 Соль образована слабой кислотой и сильным основанием. В этом случае поляризующее действие аниона велико (S-2,CO3-2,SO3-2), происходит гидролиз по аниону.
![]()
Например, гидролиз Na2CO3:
![]()
Так как в растворе образуется избыток гидроксид-ионов, то раствор будет иметь щелочную реакцию (pH> 7).
3 Соль образована сильной кислотой и слабым основанием. В этом случае поляризующее действие катиона значительно, гидролиз происходит по катиону.
![]()
Например, гидролиз CuSO4:
![]()
Гидролиз обусловлен образованием слабо диссоциирующих частиц (CuOH)+1. В результате равновесие электролитической диссоциации воды смещается и в растворе появляется избыток водородных ионов, поэтому реакция среды - кислая (pH< 7).
4 Если катионы и анионы обладают умеренным поляризующим действием, то в процессе обменного разложения воды участвуют и те, и другие.
Происходит гидролиз по катиону и аниону.
![]()
В этом случае рН среды раствора будет зависеть от соотношения констант гидролиза катиона и аниона, находящихся в воде. В данной реакции среда будет нейтральная, так как константы гидролиза практически равны.
Если в результате гидролиза выпадает осадок или выделяется газообразный продукт, т.е. часть ионов удаляется из сферы реакции, гидролиз может проходить практически необратимо. Необратимый гидролиз осуществляется при взаимодействии солей слабых оснований с солями слабых кислот (сульфидов, карбонатов), причем в осадок выпадают не сульфиды или карбонаты, а гидроксиды соответствующих катионов металлов (алюминия, хрома и пр.).
![]()
![]()
Количественно гидролиз характеризуется двумя величинами: степенью гидролиза (формула 19) и константой гидролиза (формулы 20,21).
![]() ,
(19)
,
(19)
где
![]() - степень гидролиза, увеличивающаяся
при повышении и температуры и разбавлении
раствора.
- степень гидролиза, увеличивающаяся
при повышении и температуры и разбавлении
раствора.
Константа гидролиза связана с ионным произведением воды КВи константой диссоциации КДслабого электролита, образующегося в результате гидролиза следующим соотношением:
![]() .
(20)
.
(20)
Если соль образована слабым основанием и слабой кислотой, т.е. гидролизу подвергается и катион, и анион, то
![]() ,
(21)
,
(21)
где Кдк и Кдо– константы диссоциации образующихся в результате гидролиза слабой кислоты и слабого основания соответственно.
Степень гидролиза связана с константой гидролиза и исходной концентрацией гидролизующихся ионов соотношением, аналогичным закону Оствальда (формула 22).
![]() .
(22)
.
(22)
3.3 Жесткость воды. Природная вода, содержащая большое количество растворенных солей Са2+, Mg2+, Fe2+, называется жесткой.
Соли, обуславливающие жесткость воды, не являются вредными для здоровья человека. Присутствие в воде избыточного количества магния ухудшает ее органолептические свойства.
Различают общую, временную, постоянную, карбонатную и некарбонатную жесткость воды.
Общей жесткостью называется суммарная концентрация ионов Са2+, Mg2+, Fe + в воде, выраженная в мг-экв/л.
Постоянной жесткостью называется часть общей жесткости, остающаяся после кипячения воды при атмосферном давлении в течение определенного времени.
Временной жесткостью называется часть общей жесткости, удаляющаяся при кипячении воды при атмосферном давлении в течение определенного времени. Она равна разности между общей и постоянной жесткостью.
Карбонатной жесткостью называется часть общей жесткости, эквивалентная концентрации карбонатов и гидрокарбонатов кальция и магния.
Некарбонатная жесткость - часть общей жесткости, равная разности между общей и карбонатной жесткостью.
Единицы измерения жесткости. Единой международной единицы измерения жесткости не существует. В Европе в качестве единицы жесткости принят 1 градус жесткости, соответствующий 1 г карбоната кальция, растворенного в 100000 г воды.
В Казахстане жесткость измеряется в миллиграмм-эквивалентах на 1 литр воды [мг-экв/л].
1 мг-экв жесткости соответствует содержанию 20,04 мг/л Са2+ или 12,16 мг/л Mg2+.
По жесткости воду делят на 6 классов:
- очень мягкая (от 0 до 1,5 мг-экв/л);
- мягкая (от 1,5 до 3 мг-экв/л);
- средней жесткости (от 3 до 4,5 мг-экв/л);
- довольно жесткая (от 4,5 до 6 мг-экв/л);
- жесткая (от 6 до 10 мг-экв/л);
- очень жесткая (свыше 10 мг-экв/л).
Жесткость питьевой воды не должна превышать 7 мг-экв/л.
В районах, богатых известняками, грунтовые воды могут содержать большие количества ионов кальция (Са2+) и гидрокарбонат-иона (НСО3-). В отличие от нерастворимого карбоната кальция, гидрокарбонат кальция - растворимое вещество. Такую воду легко умягчить простым кипячением, при котором происходит осаждение карбоната кальция и удаление избыточной двуокиси углерода.
![]()
![]()
Карбонат магния обладает заметной растворимостью и поэтому подвергается гидролизу.
![]()
Растворимость карбоната кальция и гидроксида магния значительно меньше, чем гидрокарбонатов, поэтому при нагревании жесткость воды снижается.
Лабораторная работа 4. Электролитическая диссоциация
Цель работы.Освоить составление уравнений ионообменных реакций.
Экспериментальная часть.
Смещение ионного равновесия в растворе слабого основания.
Налейте в две пробирки по 2-3 см3 0,1 М раствора гидроксида аммония (NH3.H2О) и по 1-2 капли раствора фенолфталеина. Объясните причину изменения окраски индикатора, напишите уравнение диссоциации гидроксида аммония.
В одну из пробирок прибавьте немного кристаллического хлорида аммония и взболтайте содержимое пробирки. Сравните окраски обеих пробирок, пользуясь уравнением диссоциации. Объясните причину смещения равновесия в сторону недиссоциированных молекул гидроксида аммония.
Опыт 4.Амфотерные электролиты.
Налейте в пробирку 2-3 см3 раствора сульфата цинка и по каплям прибавляйте к нему раствор гидроксида натрия. Образовавшийся осадок распределите в две пробирки и подействуйте на него в одном случае 2% раствором соляной кислоты, а в другом - 10%-ным раствором гидроксида натрия.
Составьте уравнения реакций. Почему гидроксид цинка ведет себя в кислом растворе как основание, а в щелочном - как кислота?
Опыт 5. Обменные реакции в растворах электролитов.
Налейте в две пробирки по 2-3 см3 сульфида натрия. В первую пробирку прилейте примерно столько же раствора сульфата железа (II), во вторую – растворсульфата меди (II). Наблюдайте образование осадков.
Напишите уравнения происходящих реакций в молекулярной, полной и сокращенной ионной формах.
Лабораторная работа 5. Гидролиз солей
Цель работы. Ознакомиться с типичными случаями и условиями протекания гидролиза солей.
Экспериментальная часть.
Опыт 1. Ознакомиться с типичными случаями и условиями протекания гидролиза солей.
В четыре пробирки налейте по 2 см3 свежеприготовленных растворов карбоната натрия, хлорида цинка, нитрата натрия и ацетата натрия. Определите рН растворов при помощи универсальной индикаторной бумаги. Полученные данные внесите в таблицу 7.
Таблица 7
|
Испытуемый раствор
|
Уравнение реакции диссоциации соли
|
Катионы (нионы), образующие прочные связи с водой |
Уравнение реакции гидролиза соли |
Состояние среды (рН) | |
|
Сокра-щенное |
Молеку-лярное | ||||
|
|
|
|
|
|
|
Опыт 2. Зависимость гидролиза солей от различных факторов.
К раствору ацетата натрия прилейте одну-две капли фенолфталеина. Заметьте интенсивность окраски. Нагрейте пробирку до кипения. Как меняется интенсивность окраски? Объясните полученный результат. Дайте немного остыть пробирке и охладите ее в холодной воде. Что происходит?
Налейте в пробирку 1-2 см3раствора хлорида висмута. Постепенно разбавляйте раствор дистиллированной воды до выпадения в осадок основной соли. К полученной основной соли висмута прибавьте из пипетки несколько капель концентрированной соляной кислоты до растворения осадка.
Напишите уравнение реакции гидролиза хлорида висмута. Укажите, как смещается равновесие гидролиза при разбавлении раствора соли и при увеличении концентрации соляной кислоты.
К 2-3 см3хлорида алюминия прибавьте по каплям раствор карбоната натрия. Образование осадкаAl(OH)3является результатом взаимного усиления гидролиза двух солей.
Напишите уравнение реакций между хлоридом алюминия и карбонатом натрия с образованием карбоната алюминия и последующей реакцией между Аl2(CO3)3и Н2О. Сделайте вывод о необратимости гидролиза.
