
- •Утверждено на заседании цкмс агму
- •Программа по фармацевтической химии Неорганические и металлорганические лекарственные средства
- •Органические лекарственные вещества Алифатические соединения
- •Тематический план занятий по фармацевтической химии для студентов 3 курса (осенний семестр)
- •Тематический план лекций по фармацевтической химии для студентов 3 курса (осенний семестр)
- •Правила внутреннего распорядка в аудитории Обязанности студентов
- •Обязанности дежурного
- •Правила пользования оборудовнием, посудой и реактивами в лаборатории
- •Правила техники безопасности при работе в химической лаборатории
- •Меры первой помощи при несчастных случаях
- •Форма ведения протокола лабораторного занятия по фармацевтической химии
- •Тема I. Общие методы и приемы определения подлинности, чистоты и количественного содержания лекарственных средств
- •План занятия
- •Контрольные вопросы по изучаемой теме
- •Контрольные вопросы по изучаемой теме
- •План занятия
- •Задание 1. Идентификация лекарственных препаратов химическими методами
- •Кислота бензойная (фс 9, гф х)
- •Контрольные вопросы по изучаемой теме
- •Литература:
- •План занятия
- •Общие правила проведения испытаний на чистоту и допустимые пределы примесей
- •Вопросы для подготовки к собеседованию по изучаемой теме
- •Контрольные вопросы по изучаемой теме
- •План занятия
- •Тема II. Анализ неорганических лекарственных соединений
- •Контрольные вопросы по смежным дисциплинам
- •Контрольные вопросы по изучаемой теме
- •План занятия
- •Вопросы для подготовки к собеседованию по теме «Галогены и их соединения как лекарственые средства»
- •План занятия
- •Вопросы для подготовки к собеседованию по теме «Кислород и его соединения. Соединения углерода и бора»
- •Занятие 9. Анализ неорганических лекарственных соединений кальция, магния, бария, алюминия, нитритов, тиосульфатов
- •Контрольные вопросы по смежным дисциплинам
- •Контрольные вопросы по изучаемой теме
- •План занятия
- •Вопросы для подготовки к собеседованию
- •Контрольные вопросы по смежным дисциплинам
- •Контрольные вопросы по изучаемой теме
- •План занятия
- •Вопросы для подготовки к собеседованию
- •Вопросы для подготовки к контрольной работе
- •Тестовые задания
- •28. Определите, верны или нет каждое из приведенных утверждений и причинно-следственная связь между ними.
- •Тема III. Анализ алифатических препаратов галогенопроизводных алканов, альдегидов, спиртов, углеводов, эфиров
- •Литература:
- •План занятия
- •Задание 3. Экспресс-анализ раствора гексаметилентетрамина
- •Количественное определение
- •Занятие 13. Препараты моно-, ди- и полисахаридов, спиртов, простых алифатических эфиров, сложных эфиров
- •Контрольные вопросы по смежным дисциплинам
- •Контрольные вопросы по изучаемой теме
- •План занятия
- •Декстрин
- •Задание 2. Фармакопейный анализ препарата
- •Тема IV. Препараты карбоновых кислот, аминокислот алифатического ряда, лактонов ненасыщенных полиоксикислот
- •Контрольные вопросы по смежным дисциплинам
- •Контрольные вопросы по изучаемой теме
- •План занятия
- •Задание 3. Экспресс-анализ лекарственной смеси
- •Подлинность
- •Контрольные вопросы по смежным дисциплинам
- •Контрольные вопросы по изучаемой теме
- •План занятия
- •Задание 1. Фармакопейный анализ кислоты глютаминовой ( фс 15, гф X, сокращенный вариант)
- •Подлинность.
- •Занятие 17. Контрольная работа по теме «Анализ препаратов карбоновых кислот и аминокислот, лактонов ненасыщенных полиосикарбоновых кислот»
- •Занятие 18-19. Теоретический контроль по теме «Анализ лекарственных веществ по функциональным группам»
Контрольные вопросы по изучаемой теме
Источники примесей и причины недоброкачественности лекарственных веществ.
Основные физические, физико-химические, химические методы обнаружения примесей.
Общие требования при испытании на доброкачественность. Определение допустимых и недопустимых примесей эталонным и безэталонным методом.
Эталонные растворы для испытания на основные примеси по ГФ X и ГФ XI. Классификация эталонных растворов, требования к их приготовлению.
Химические реакции, лежащие в основе определения общих примесей. Испытания на хлориды, сульфаты, соли аммония и аммиак, соли кальция, соли железа (II) и (III), соли цинка, соли тяжелых металлов (ион свинца).
Принципы расчета навески исходной соли для приготовления эталонных растворов на конкретные примеси.
Определение летучих веществ и воды: метод высушивания, метод дистилляции, метод Фишера.
Определение потери в массе при высушивании ГФ Х и ГФ XI.
Определение общей и сульфатной золы.
Определение прозрачности и степени мутности жидкостей по ГФ X и ГФ XI.
Определение цветности растворов лекарственных веществ по ГФХ и ГФХI.
Определение кислотности, щелочности и рН по ГФХ и ГФХI.
Определение растворимости лекарственных веществ по ГФХ и ГФХI.
Определение примеси мышьяка по методу Зангера-Блека (способ 1) и по методу Буго-Тиле (способ 2). Химические реакции, лежащие в основе определения.
Испытания на специфические примеси, оценка чистоты физико-химическими методами – спектрофотометрии в УФ области спектра, рефрактометрии, поляриметрии, хроматографическими методами.
Литература:
Государственная Фармакопея СССР X изд. – Медицина, 1965.
Государственная Фармакопея СССР XI изд., т. 1,2. – М.: Медицина, 1987.
Беликов В.Г. Фармацевтическая химия. – М.: Высшая школа, 1985.
Беликов В.Г. Фармацевтическая химия. – Пятигорск, 2003.
Арзамасцев А. П. Руководство к лабораторным занятиям по фармацевтической химии. – М.: Медицина, 1987.
Арзамасцев А.П. Фармацевтическая химия / учебное пособие для вузов. –М.: ГЭОТАР – Медиа, 2005.
Лабораторные работы по фармацевтической химии/под ред. В. Г. Беликова. – М.: Высшая школа, 1989.
Конспекты лекций.
План занятия
Теоретический контроль знаний студентов.
Объяснение преподавателем принципа расчета навески исходной соли для приготовления эталонного раствора.
Самостоятельная работа студентов:
Задание I. Приготовление эталонного раствора для определения примеси.
Задание 2. Определение доброкачественности воды очищенной.
Задание 3. Определение цветности резорцина.
Оформление и защита протоколов, приведение в порядок рабочего места.
Задание 1. Приготовление эталонного раствора для определения примеси (по ГФ XI) с предварительным расчетом навески исходного количества соли
(по заданию преподавателя)
Общие правила проведения испытаний на чистоту и допустимые пределы примесей
Для определения примеси в лекарственном препарате и оценки ее количества в случае использования эталонного метода проводят испытание с анализируемым раствором и с эталонным раствором, содержащим определенное количество исследуемой примеси, после чего сравнивают результаты. Сравнение проводят колориметрическим или нефелометрическим методом. Эталонный раствор – это раствор с точно известным содержанием общей примеси. Анализируемые растворы препарата готовят по методикам, указанным в соответствующих частных статьях (ФС) и, в которых указывается допустимое содержание примеси в %. В общем случае допустимый предел содержания примеси (х %) в растворе препарата, приготовленного по методике соответствующей частной статьи, рассчитывают по формуле:
х % = С * m / V
где С – предельно допустимое по ФС содержание примеси в препарате в %, m – масса препарата, взятая для испытания в граммах, V – объем растворителя, использованный для растворения взятой массы препарата в мл. Этот допустимый предел содержания примеси (х %) должен соответствовать концентрации ( % ) общей примеси в эталонном растворе, то есть определять выбор эталонного раствора Б, В или А по ОФС «Испытания на чистоту и допустимые пределы примесей».
При определении примесей в лекарственных препаратах необходимо соблюдать следующие п р а в и л а:
Вода и все реактивы должны быть свободны от ионов, на содержание которых проводится испытание.
Пробирки, в которых проводят наблюдения, должны быть бесцветными и одинакового диаметра.
Навески для приготовления эталонных растворов берут с точностью до 0,001 г.
Эталонные растворы Б и В готовят непосредственно перед применением.
Муть и опалесценцию растворов наблюдают в проходящем свете на темном фоне, а окраску – в отраженном свете на матово-белом фоне.
Прибавление реактивов к испытуемому и эталонному растворам должно проводиться одновременно и в одинаковых количествах.
При испытании на недопустимые примеси поступают следующим образом. К 10 мл испытуемого раствора прибавляют все реактивы, указанные в статье, кроме основного реактива, открывающего данную примесь. Затем раствор делят на две равные части и к одной из них прибавляют указанный в статье основной реактив. Оба раствора сравнивают между собой. Между ними не должно быть существенных различий.
При испытании на допустимые примеси поступают следующим образом. К 10 мл испытуемого раствора, приготовленного, как указано в соответствующей частной статье, прибавляют не основные и основные реактивы и сравнивают с эталоном, состоящим из 10 мл эталонного раствора и такого же количества реактивов, какое было прибавлено к испытуемому раствору.
Эталонный раствор хлор-иона (ГФ XI, с. 166)
0,659 г прокаленного хлорида натрия растворяют в воде в мерной колбе емкостью 1 л и доводят объем раствора водой до метки (раствор А). 5 мл раствора А разводят водой в мерной колбе емкостью 1 л (раствор Б). Этот раствор содержит 0,002 мг хлор-иона в 1 мл, т. е. 0,0002 %.
Эталонный раствор сульфат-иона (ГФ XI, с. 167)
1,814 г сульфата калия, высушенного при 100-105 °С до постоянной массы, растворяют в воде в мерной колбе емкостью 1 л и доводят объем раствора водой до метки (раствор А). 10 мл раствора А разводят водой в мерной колбе до 1 л (раствор Б). Этот раствор содержит 0,01 мг сульфат-иона в 1 мл, т. е. 0,001 %.
Эталонный раствор аммоний-иона (ГФ XI, с. 168)
0,628 г хлорида аммония, высушенного в эксикаторе над серной кислотой до постоянной массы, растворяют в воде в мерной колбе емкостью 1 л и доводят объем раствора водой до метки (раствор А). 10 мл раствора А разводят водой в мерной колбе емкостью 1 л (раствор Б). Этот раствор содержит 0,002 мг аммоний-иона в 1 мл, т. е. 0,0002 %.
Эталонный раствор кальций-иона (ГФ XI, с. 169)
0,749 г карбоната кальция, высушенного при 100-105°С до постоянной массы, взбалтывают в мерной колбе емкостью 100 мл с 10 мл воды, постепенно прибавляют разведенную кислоту хлороводородную до растворения и после удаления пузырьков углекислого газа доводят объем раствора водой до метки (раствор А). 10 мл раствора А разводят водой до 1 л (раствор Б). Этот раствор содержит 0,03 мг кальций-иона в 1 мл, т. е. 0,003 %.
Эталонный раствор свинец-иона (ГФ XI, с. 172)
0,915 г свежеперекристаллизованного свинца ацетата растворяют в мерной колбе емкостью 1 л, прибавляют 1 мл разведенной кислоты уксусной и доводят объем раствора водой до метки (раствор А). 1 мл раствора А разводят водой в мерной колбе до 100 мл (раствор Б). Этот раствор содержит 0,005 мг свинец-иона в 1 мл, т. е. 0,0005%. Раствор Б годен только в день его приготовления.
Эталонный раствор железо (III)-иона (ГФ XI, с. 170)
Определяют содержание железа в железоаммониевых квасцах методом, описанным для железа (III) хлорида.
Около 2,5 г препарата (точная навеска) растворяют в воде в мерной колбе вместимостью 100 мл и доводят объем раствора водой до метки. 20 мл этого раствора переносят в колбу с притертой пробкой, прибавляют 10 мл кислоты хлороводородной и 2 г калия йодида, смесь взбалтывают и оставляют в темном месте на 30 мин, затем прибавляют 50 мл воды и титруют раствором натрия тиосульфата (0,1 моль/л), индикатор – крахмал.
1 мл раствора натрия тиосульфата соответствует 0,005585 г железа.
На основании полученных результатов готовят 0,1% раствор железо (Ш) иона растворением рассчитанного количества железоаммонийных квасцов в воде в мерной колбе емкостью 100 мл. Раствор подкисляют 1 мл кислоты хлороводородной и доводят объем водой до метки (раствор А).
15 мл раствора А доводят водой в мерной колбе до 500 мл (раствор Б). 10 мл раствора Б разводят водой в мерной колбе до 100 мл (раствор В). Этот раствор содержит 0,003 мг железо (III) иона в 1 мл, т. е. 0,0003%. Раствор В пригоден только в день его приготовления.
Эталонный раствор цинк-иона (ГФ XI, с. 171)
0,625 г цинка оксида, предварительно прокаленного до постоянной массы, рстворяют в 10 мл кислоты азотной, переносят в мерную колбу вместимостью 500 мл и доводят объем раствора водой до метки (раствор А). 1 мл раствора А помещают в мерную колбу вместимостью 200 мл, прибавляют 4 капли кислоты азотной и доводят объем раствора водой до метки (раствор Б). Этот раствор содержит 0,005 мг цинк-иона в 1 мл, т. е. 0,0005%.
Задание 2. Определение доброкачественности воды очищенной (ФС 42-2619-97)
Настоящая фармакопейная статья распространяется на воду очищенную, получаемую дистилляцией, ионным обменом, обратным осмосом, комбинацией этих методов или другим способом, применяемую для приготовления неинъекционных лекарственных средств.
Описание. Бесцветная прозрачная жидкость без запаха и вкуса.
рН от 5,0 до 7,0 (к 100 мл воды прибавляют 0,3 мл насыщенного раствора калия хлорида и измеряют рН раствора потенциометрически (ГФХ1, т.1, с. 113).
Сухой остаток. 100 мл воды выпаривают на водяной бане досуха и сушат при 100-105°С до постоянной массы. Остаток не должен превышать 0,001 %.
Восстанавливающие вещества. 100 мл воды доводят до кипения, прибавляют 1 мл 0,01 М раствора калия перманганата и 2 мл кислоты серной разведенной, кипятят 10 мин, розовая окраска должна сохраняться.
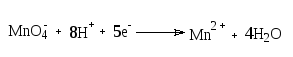
Диоксид углерода. При взбалтывании воды с равным объемом известковой воды в наполненном доверху и хорошо закрытом сосуде не должно быть помутнения в течение 1 часа.
![]()
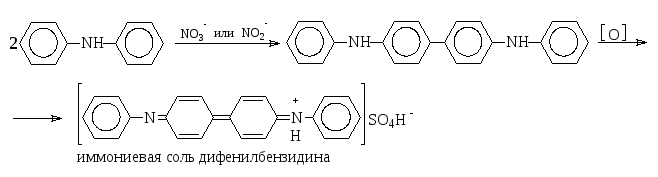
Нитраты и нитриты. К 5 мл воды осторожно прибавляют 1 мл свежеприготовленного раствора дифениламина; не должно появляться голубого окрашивания.
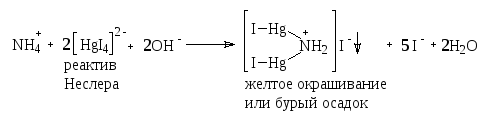
Аммиак. К 10 мл воды прибавляют 0,15 мл реактива Несслера, перемешивают и через 5 минут сравнивают с раствором, состоящим из смеси 1 мл эталонного раствора Б, содержащего 0,002 мг аммоний-иона в 1 мл, 9 мл воды, свободной от аммиака, и такого же количества реактива, какое прибавлено к испытуемому раствору. Окраска, появившаяся в испытуемом растворе, не должна превышать эталон (0,00002% в препарате).
Хлориды. К 10 мл воды прибавляют 0,5 мл кислоты азотной, 0,5 мл раствора серебра нитрата, перемешивают и оставляют на 5 мин. Не должно быть опалесценции.
![]()
Сульфаты. К 10 мл воды прибавляют 0,5 мл кислоты хлороводородной разведенной и 1 мл раствора бария хлорида, перемешивают и оставляют на 10 мин. Не должно быть помутнения.
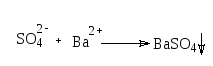
Кальций. К 10 мл воды прибавляют 1 мл раствора аммония хлорида, 1 мл раствора аммиака и 1 мл раствора аммония оксалата, перемешивают и оставляют на 10 мин. Не должно быть помутнения.
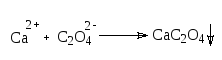
Тяжелые металлы. К 10 мл воды прибавляют 1 мл кислоты уксусной разведенной, 2 капли раствора натрия сульфида, перемешивают и оставляют на 1 мин.
Наблюдение окраски производят по оси пробирки диаметром около 1,5 см, помещенной на белой поверхности. Не должно быть окрашивания.
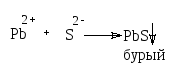
Микробиологическая чистота. Должна соответствовать требованиям, предъявляемым к питьевой воде (не более 100 микроорганизмов в 1 мл) при отсутствии бактерий сем. Еnterobаctеriасеае, Staphу1ососсus аureus, Рseudomonas aeruginosa. Испытания проводят в соответствии со статьей «Испытание на микробиологическую чистоту» (ГФ XI, т.2, с. 193).
Использование и хранение. Используют свежеприготовленной или хранят в закрытых емкостях, изготовленных из материалов, не изменяющих свойств воды и защищающих от инородных частиц и микробиологических загрязнений.
Задание 3. Определение цветности и прозрачности раствора резорцина (ГФ X, ст. 577, с. 587)
Раствор 1 г резорцина в 20 мл свежепрокипяченной и охлажденной очищенной воды должен быть прозрачным, и окраска его не должна быть интенсивнее окраски эталона № 5а или 5в. Эталонный раствор 5а или 5в готовят по ГФХI, т.1, с. 194 «Определение окраски жидкостей».
