
Акватерм Водоподготовка Беликов
.pdf
Введение
|
олгие годы и столетия водоподготовка не |
были направлены на реализацию потребностей |
|
|
выделялась как отрасль техники и еще ме- |
водоподготовки. Напротив, внимание к этой отрас- |
|
|
Днее – как отрасль химической технологии. |
ли и, стало быть, финансирование проявлялись в |
|
|
Использовались эмпирически найденные приемы |
наименьшем объеме, по остаточному принципу. |
|
|
и способы очистки воды, главным образом, проти- |
Испытания, выпавшие на долю России за пос- |
|
|
воинфекционные. И потому история водоподготов- |
ледние 12–15 лет, в полной мере познала и водо- |
|
|
ки – это история приспособления для подготовки и |
подготовка. Одно из печальных следствий такого |
|
|
очистки воды известных химических процессов и |
положения – отсутствие на рынке универсальных |
|
|
технологий, нашедших или находящих свое при- |
изданий по водоподготовке. |
|
10 |
|||
менение. |
В этих условиях Издательский Дом «Аква- |
||
Подготовка воды для питьевого и промышлен- |
Терм», публикуя справочник, надеется привлечь |
||
|
ного водоснабжения принципиально отличается от |
к нему внимание как специалистов, так и людей, |
|
|
других областей химической технологии: процес- |
только начинающих свой путь в водоподготовке. |
|
|
сы водоподготовки протекают в больших объемах |
О последней группе необходимо сказать особо. |
|
|
воды и при очень малых количествах растворенных |
И заказчики, и поставки водоподготовительного |
|
|
веществ. Значит, большие расходы воды требуют |
оборудования все больше, если можно так выра- |
|
|
устройства крупногабаритного оборудования, а |
зиться, индивидуализируются. В прошлые годы |
|
|
малое количество извлекаемых из воды веществ |
поставки были, как правило, оптовыми, а теперь, |
|
|
неизбежно влечет за собой применение «тонких» |
в основном, – мелкооптовые и одиночные. Не го- |
|
|
методов обработки воды. |
воря о том, что совсем недавно отсутствовало рос- |
|
|
После обработки в системах и на станциях во- |
сийское производство бытовых фильтров и систем |
|
|
доподготовки требуется вода со степенью чисто- |
автономного водоснабжения, по определению пос- |
|
|
ты, недоступной, да чаще всего и ненужной, для |
тавляемых в одном или нескольких экземплярах. |
|
|
большей части химических продуктов. Например, |
Да и импорт такого оборудования был весьма ску- |
|
|
стандартное требование – предел содержания же- |
ден. Значит, в водоподготовку вовлекается мно- |
|
|
леза в питьевой воде и питательной воде энерге- |
жество людей, ранее с ней незнакомых. |
|
|
тических объектов, равный 0,3 мг/л, означает чис- |
Кроме того, при малочисленности специалис- |
|
|
тоту в 0,00003%! |
тов по водоподготовке водой занимаются многие |
|
|
В настоящее время усиленно разрабатывают- |
инженеры, получившие образование по другим |
|
|
ся научные основы технологий обработки воды, |
специальностям. |
|
|
учитывающие указанную специфику этой отрасли |
Поэтому текст издания содержит сведения не |
|
|
техники. И такая работа далека от завершения, |
только справочного характера для состоявшихся |
|
|
если можно вообще говорить об окончательном |
специалистов, но и сведения, включаемые обычно |
|
|
познании воды. |
в учебники для высших и средних учебных заведе- |
|
|
Было бы громадным преувеличением утверж- |
ний, а также данные, позволяющие потребителю |
|
|
дать, что передовые научные и конструкторские |
ориентироваться в обильном количестве материа- |
|
|
силы, лучшие машиностроительные мощности |
лов и конструкций для водоподготовки. |
ВОДОПОДГОТОВКА
Библиотека «Аква-Терм»

|
|
|
|
|
Введение |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|||
Вряд ли можно назвать легкой задачу удов- |
воды) может применяться конкретный метод, воду |
|
|||||
летворения запросов таких разнообразных групп |
какого качества можно получить этим методом. |
|
|||||
читателей – свести воедино специальные, научно- |
Надеемся также, что специалисты в описаниях ме- |
|
|||||
популярные и просто популярные тексты. Вам – чи- |
тодов найдут некоторые новые для себя частности |
|
|||||
тателям – судить, удалось ли издательству (и в ка- |
и детали. |
|
|
|
|
||
кой мере) решить эту задачу. |
|
Часть вторая описывает фильтрующие матери- |
|
||||
В соответствии с вышесказанным книга постро- |
алы: наполнители осветлительных фильтров, сор- |
|
|||||
ена следующим образом. |
|
бенты, иониты. |
|
|
|
|
|
Глава первая части первой рассказывает о воде |
В списке литературы приведены почти все ос- |
|
|||||
как особом веществе, особом «рабочем теле» всех |
новополагающие монографии, |
энциклопедичес- |
|
||||
производств, о ее качестве, примесях и их влия- |
кие издания, справочники как новые, к сожале- |
|
|||||
нии на здоровье людей и работу промышленного |
нию, немногочисленные, так и ранее изданные, но |
|
|||||
оборудования. Представлены |
разные системы |
сохраняющие и сегодня свою полезность. Ссылки |
|
||||
классификации природных вод. Глава вторая пос- |
на некоторые публикации, касающиеся частных |
|
|||||
вящена рассмотрению нормативов качества воды. |
вопросов, но безусловно необходимые, даны в тек- |
|
|||||
Приводится наиболее полный перечень действую- |
сте книги. |
|
|
|
|
||
щих нормативных документов, регламентирующих |
В Приложения вынесены справочные мате- |
|
|||||
качество природных вод, используемых для подго- |
риалы об ионитах, о терминах водоподготовки, |
|
|||||
товки питьевой воды и воды для промышленнос- |
единицах измерения величин, встречающихся в |
|
|||||
ти и энергетики, а также документов, определяю- |
технической литературе и документации, методах |
|
|||||
щих требования разных потребителей к качеству |
определения некоторых параметров, и даны при- |
|
|||||
подготовленной воды. Публикуется перечень со- |
меры расчетов фильтров. Приведены реквизиты |
|
|||||
ответствующих документов. В сопоставлении с |
информационных организаций. |
|
|
|
|
||
российскими рассмотрены некоторые зарубежные |
Расширенное детализированное |
оглавление, |
|
||||
нормы. Сопоставлены российские и международ- |
кроме своего прямого назначения, может служить |
|
|||||
ные нормы и рекомендации, касающиеся качества |
в некотором роде предметным указателем. |
|
|||||
питьевой воды и воды, расфасованной в емкости. |
Цель издательства состоит в том, чтобы чита- |
|
|||||
В третьей главе дан перечень нормативных доку- |
тель получил сведения о нормировании качества |
11 |
|||||
ментов, регламентирующих аналитические методи- |
воды для разных пользователей, о современных |
||||||
ки по качеству воды. Обращено внимание на то, что |
технологиях водоподготовки. Ввиду чрезвычай- |
||||||
воду для энергетических потребителей нужно ана- |
ной сложности этой задачи были поставлены оп- |
|
|||||
лизировать не только по тем показателям, которые |
ределенные границы: здесь нет информации об |
|
|||||
определяются при получении питьевой воды. Необ- |
отстаивании, коагулировании |
в осветлителях, |
|
||||
ходимо также определять некоторые примеси при- |
известковании, содоизвестковании |
и некоторых |
|
||||
родных вод – при нагреве воды в теплогенераторах |
других технологиях и конструкциях, |
традиционно |
|
||||
и теплоиспользующих аппаратах эти примеси мо- |
называющихся «предочисткой». Также нет данных |
|
|||||
гут служить источниками коррозионных и накипных |
о методах и конструкциях, нашедших применение |
|
|||||
проявлений. В связи с этим предложен примерный |
в основном в «большой» энергетике. Рассмотре- |
|
|||||
состав прописи анализов воды для энергетичес- |
ны и представлены методы, применяющиеся для |
|
|||||
ких потребителей воды. Показано, как соотносятся |
подготовки воды в коммунальном водоснабжении, |
|
|||||
между собою показатели качества воды, опреде- |
в котельных, оборудованных паровыми котлами с |
|
|||||
ленные разными методиками. |
|
давлением пара до 3,9 МПа, водогрейными кот- |
|
||||
Глава четвертая содержит описание наиболее |
лами с теплопроизводительностью до 209 МВт и |
|
|||||
часто применяющихся методов |
водоподготовки: |
температурой сетевой воды на выходе из котла не |
|
||||
химическая или физическая природа процессов, |
более 180°С, и системах теплоснабжения. |
|
|||||
лежащих в их основе, технология, материалы, |
Нет сведений о термических методах водо- |
|
|||||
конструкции, оборудование, схемы. Показаны при- |
подготовки: дегазации (деаэрации), дистилляции, |
|
|||||
нципы расчетов технологии и оборудования. Пред- |
даны краткие сведения о коррозии оборудования. |
|
|||||
ставлены возможности каждого метода обработки |
Не затронуты обширные темы: технология, реаген- |
|
|||||
воды. |
|
ты и оборудование, обеспечивающие оптимальный |
|
||||
Здесь сделана попытка представить начинаю- |
водно-химический режим теплоэнергетического |
|
|||||
щим «водникам» облик, суть методов водоподго- |
оборудования, очистка сточных вод от оборудова- |
|
|||||
товки. Но, возможно, и опытные специалисты уви- |
ния и систем водоподготовки. |
|
|
|
|
||
дят пользу в системном описании каждого метода: |
Публикация выписок из нормативных докумен- |
|
|||||
в каких условиях (при каком качестве исходной |
тов в данном издании не может служить основа- |
|
|||||
ВОДОПОДГОТОВКА
Библиотека «Аква-Терм»

Введение
нием для читательских ссылок в своих работах и |
Полные тексты нормативных документов пуб- |
суждениях. Здесь извлечения из официальных |
ликуются в официальных изданиях Минздравсоц- |
изданий помещены в качестве справок соответс- |
развития (б. Минздрава РФ), Госстандарта России, |
твенно Закону РФ № 5352 от 9 июля 1993 г. «Об |
Госстроя России и Госгортехнадзора России. Рек- |
авторском праве и смежных правах», ст. 8. Тем бо- |
визиты издательских центров этих государствен- |
лее, что проверка правильности ссылок – вне пре- |
ных учреждений – в Приложении 10. |
делов возможностей издательства. |
|
12
ВОДОПОДГОТОВКА
Библиотека «Аква-Терм»
Часть первая
1. Природные
воды. Примеси.
Качество
ряются газы земной атмосферы и, вероятно, всетаки частицы стенок сосуда. В воде есть и «собственные» примеси: при обычной температуре из каждого миллиарда молекул воды образуется два иона – Н+ и ОН-. Ион Н+ немедленно присоединяется к молекуле воды, образуя ион гидроксония Н3О+.
1.1.2. Строение молекул и ассоциатов природной воды
1.1. Свойства воды |
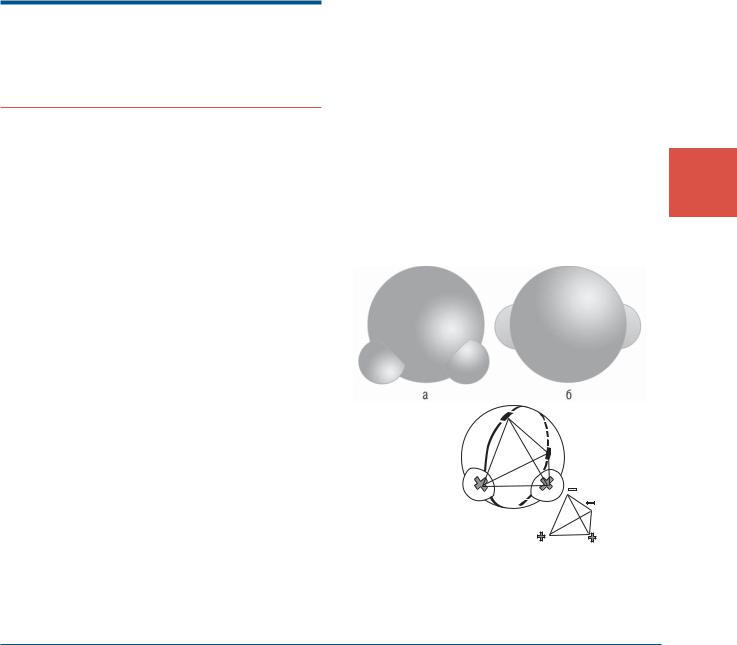
Самая простая принятая сегодня модель моле- |
13 |
|||||
|
кулы воды – тетраэдр (рис. 1.1, 1.2). В действитель- |
||||||
ода – самое аномальное вещество прироности одиночные молекулы воды при нормальных |
|
||||||
ды. Это расхожее выражение связано с тем, |
температуре и давлении не существуют. Есть не- |
|
|||||
Вчто свойства воды во многом не соответс- |
|
|
|
|
|
|
|
твуют физическим законам, которым подчиняются |
|
|
|
|
|
|
|
другие вещества. |
|
|
|
|
|
|
|
1.1.1. Химически чистая вода |
|
|
|
|
|
|
|
Прежде всего необходимо напомнить: когда мы |
|
|
|
|
|
|
|
говорим о природной воде, все суждения должны |
|
|
|
|
|
|
|
быть отнесены не к воде как таковой, а к водным рас- |
|
|
|
|
|
|
|
творам разных, фактически всех, элементов Земли. |
|
|
|
|
|
|
|
До сих пор получить химически чистую воду не |
|
|
|
|
|
|
|
удалось. Например, в одном из опытов немецкий |
|
|
|
|
|
|
|
химик В.Ф. Кольрауш подвергал воду 42 циклам |
|
|
|
|
|
|
|
дистилляции подряд, причем вода находилась в |
|
|
|
|
|
|
|
сосуде, с которым ученый работал до этого опы- |
|
|
|
|
|
|
|
та в течение 10 лет. Следовательно, можно было |
|
|
|
|
|
|
|
предположить, что из стенок сосуда в выпарива- |
|
|
|
|
|
|
|
емую воду ничего не перейдет. Степень чистоты |
в |
|
|||||
воды, полученной в опыте Кольрауша и опреде- |
|
|
|
|
|
|
|
ленной по электропроводимости, оказалась в 100 |
Рис 1.1. Тетраэдр (модель): |
|
|||||
раз больше, чем у монодистиллированной (один |
а – вид на молекулу воды со стороны атомов водорода; |
|
|||||
цикл дистилляции) воды. |
б – вид на молекулу воды со стороны атома кислорода; |
|
|||||
Но все-таки эту воду нельзя назвать абсолютно |
в – заряды (электроны, расположенные в молекуле |
|
|||||
чистой: в дистиллированной воде сразу же раство- |
воды в виде тетраэдра) |
|
|||||
ВОДОПОДГОТОВКА
Библиотека «Аква-Терм»
Часть первая
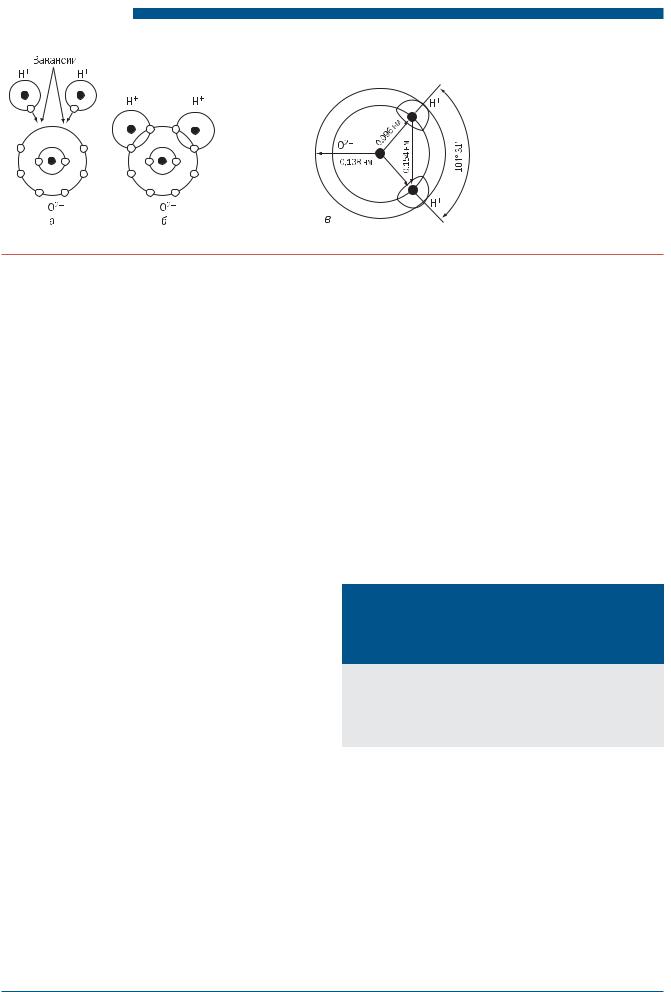
Рис. 1.2. Схема процесса образования из одного атома кислорода и двух атомов водорода (а) молекулы воды (б); в – молекула воды и ее размеры
|
сколько гипотез, описывающих строение и свойс- |
1.1.4. Физические свойства воды |
|
||||||||||||
|
тва ассоциатов воды. Однако единое понимание |
Полярная асимметричная структура воды и раз- |
|||||||||||||
|
пока не достигнуто. |
|
|
|
|
|
|
нообразие ее ассоциатов обусловливают удиви- |
|||||||
|
Существует и вполне обоснованное мнение о |
тельные аномальные физические свойства воды. |
|||||||||||||
|
том, что в воде, кроме ионов Н+, Н |
О+ и ОН- (отвле- |
Вода достигает наибольшей плотности при |
||||||||||||
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
каясь от инородных примесей), содержатся и дру- |
плюсовой температуре, у нее аномально высокие |
|||||||||||||
|
гие ионы: Н |
О + и Н |
О -. По этой гипотезе в воде |
теплота испарения и теплота плавления, удельная |
|||||||||||
|
9 |
4 |
|
7 |
4 |
|
|
|
|
|
|
|
|
|
|
|
идет реакция: |
|
|
|
|
|
|
|
|
теплоемкость, температура кипения и замерзания. |
|||||
|
|
|
|
|
|
|
|
|
|
|
Например, можно сравнить воду с аналогичными |
||||
|
|
Н |
О |
+ + Н |
О |
- = 8 Н |
О. |
(1.1) |
водородными соединениями подгруппы кислорода |
||||||
|
|
9 |
4 |
|
7 |
4 |
2 |
|
|
|
периодической системы элементов Д.И. Менделе- |
||||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
Не лишено основания предположение ряда уче- |
ева (табл. 1.1). |
|
|
|
|
|||||||||
|
ных-физиков: из-за асимметричного расположе- |
|
|
|
|
|
|||||||||
14 |
|
|
|
|
|
||||||||||
ния электрических зарядов в молекуле воды все |
|
|
|
|
|
||||||||||
Таблица 1.1 |
|
|
|
|
|||||||||||
молекулы связаны друг с другом – каждый из ио- |
|
|
|
|
|||||||||||
|
нов водорода одной молекулы притягивает к себе |
Зависимость температур замерзания и кипения некоторых |
|||||||||||||
|
электроны атомов кислорода в соседних молеку- |
соединений водорода от молекулярной массы |
|
||||||||||||
|
лах. И можно сказать: все молекулы воды связаны |
|
|
|
|
|
|||||||||
|
в одну пространственную сетку, то есть океан – одна |
|
|
|
|
||||||||||
|
Соединения |
Молекулярная |
Температура, °С |
||||||||||||
|
гигантская молекула. Но |
составные части |
этой |
элементов |
масса |
|
|
|
|||||||
|
замерзания |
|
кипения |
||||||||||||
|
макромолекулы находятся в постоянных измене- |
подгруппы |
|
|
|||||||||||
|
|
|
|
|
|||||||||||
|
ниях в зависимости от внешних условий (темпера- |
кислорода |
|
|
|
|
|||||||||
|
туры и др.). |
|
|
|
|
|
|
|
|
|
с водородом |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2Te |
130 |
–51 |
|
–4 |
|
|
|
|
|
|
|
|
|
|
|
H2Se |
81 |
–64 |
|
–42 |
|
1.1.3. Состав природной воды. |
|
H2S |
34 |
–82 |
|
–61 |
||||||||
|
|
H2O |
18 |
0 |
|
+100 |
|||||||||
|
Изотопы |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вследствие существования изотопов водоро- |
|
|
|
|
|
|||||||||
|
да и кислорода молекулярная масса воды может |
|
|
|
|
|
|||||||||
|
отличаться от 18. В природной воде найдены три |
Исходя из температур кипения и замерзания |
|||||||||||||
|
изотопа водорода и три изотопа кислорода. Ис- |
гидридов серы H2S, селена H2Se и теллура H2Te, |
|||||||||||||
|
кусственно созданы два изотопа водорода и пять |
вода (гидрид кислорода) должна была бы кипеть |
|||||||||||||
|
изотопов кислорода. Теоретически сегодня можно |
при температуре минус 80°С и замерзать при ми- |
|||||||||||||
|
говорить о 135 различных видах воды. Но только |
нус 100°С. В действительности вода кипит при |
|||||||||||||
|
девять из них устойчивые. |
|
|
|
|
+100°С и замерзает при 0°С. |
|
|
|
||||||
|
Соотношение этих стабильных изотопов в при- |
Наибольшая плотность воды при температуре |
|||||||||||||
|
родной воде, % мол.: |
|
|
|
|
|
|
+4°С обеспечивает жизнь в воде зимой. Плотность |
|||||||
|
1Н 16О – 99,73; |
1Н 18О |
– 0,20; |
1Н 17О – |
0,04; |
чистой воды, свободной от воздуха, при атмос- |
|||||||||
|
2 |
|
|
|
2 |
|
|
|
2 |
|
|
|
|
|
|
|
1Н2Н16О ~0,03%. Другие изотопы присутствуют в |
ферном давлении 0,1 МПа равна 1,00000 г/мл. При |
|||||||||||||
|
ничтожном количестве. |
|
|
|
|
|
любых других температурах плотность меньше. |
||||||||
ВОДОПОДГОТОВКА
Библиотека «Аква-Терм»

|
|
Часть первая |
|
|
|
|
|
||
|
|
|
|
|
Большая удельная теплоемкость – 4,1855 Дж/(г ·°С) |
Истинные растворы, где примеси находятся в |
|
||
при 15°С – способствует регулированию темпера- |
молекулярно-растворенном виде или в виде ио- |
|
||
туры на Земле из-за медленного нагревания и ос- |
нов, – это гомогенные системы. Гетерогенные сис- |
|
||
тывания масс воды. У ртути, к примеру, удельная |
темы – коллоиды (размер частиц: 10-2–10-1 мкм) |
|
||
теплоемкость при 20°С – только 0,1394 Дж/(г ·°С). |
или суспензии (частицы >10-1 мкм). Суспензии мо- |
|
||
Вообще теплоемкость воды более чем вдвое |
гут быть представлены взвесями, эмульсиями, пе- |
|
||
превышает теплоемкость любого другого хи- |
нами (частный случай эмульсий). |
|
||
мического соединения. Этим можно объяснить |
1.2.2. Системы классификации |
|
||
выбор воды в качестве рабочего тела в энер- |
|
|||
гетике. |
Вода – один из лучших растворителей. Изна- |
|
||
Аномальное свойство воды – расширение объ- |
чально в Мировом океане были – в той или иной |
|
||
ема на 10% при замерзании обеспечивает пла- |
степени – растворены все вещества Земли. И это |
|
||
вание льда, то есть опять сохраняет жизнь подо |
растворение продолжается: количество поровых |
|
||
льдом. |
вод илов и горных пород составляет около 19% |
|
||
Еще одно чрезвычайно важное свойство воды – |
всей гидросферы. |
|
||
исключительно большое поверхностное натяже- |
Уже несколько столетий разрабатываются сис- |
|
||
ние. Молекулы на поверхности воды испытывают |
темы классификации природных вод и способы |
|
||
действие межмолекулярного притяжения с одной |
как можно более краткой характеристики качест- |
|
||
стороны. Так как у воды силы межмолекулярно- |
ва воды (индекс качества воды). Выделено 625 и |
|
||
го взаимодействия аномально велики, то каждая |
даже более классов, групп, типов и разновиднос- |
|
||
«плавающая» на поверхности воды молекула как |
тей вод. В.И. Вернадский считал, что число видов |
|
||
бы втягивается внутрь слоя воды. У воды поверх- |
природных вод больше 1500 единиц. |
|
||
ностное натяжение равно 72 мН/м при 25°С. В час- |
Однако чем более детально разрабатывалась |
|
||
тности, этим свойством объясняется шаровая фор- |
классификация вод, тем больше исследовате- |
|
||
ма воды в условиях невесомости, поднятие воды в |
ли удалялись от желаемой краткости и ясности |
|
||
почве и в капиллярных сосудах деревьев, расте- |
в определении качества воды. Оказалось невоз- |
|
||
ний и т.д. Для сравнения: у этилового спирта при |
можным оценить пригодность воды для питьевых, |
|
||
этой же температуре поверхностное натяжение в |
технических, других целей только на основе пред- |
15 |
||
3,5 раза меньше. |
ложенных универсальных индексов воды. По-пре- |
|||
|
жнему качество воды, пригодность ее для исполь- |
|||
|
зования оценивается по комплексу показателей, и |
|
||
1.2. Классификация |
нужно признать, что такой подход дает лишь при- |
|
||
близительное знание о качестве воды. Этим, в час- |
|
|||
природных вод |
тности, можно объяснить большое (до нескольких |
|
||
|
десятков) количество нормируемых показателей |
|
||
1.2.1. Дисперсные системы |
для каждого из возможных применений. Говорить |
|
||
о качестве воды имеет смысл лишь в связи с конк- |
|
|||
Природная вода – сложная дисперсная систе- |
ретной областью ее дальнейшего использования. |
|
||
ма, содержащая множество разнообразных мине- |
К настоящему времени создано несколько де- |
|
||
ральных и органических примесей. |
сятков классификационных систем, рассматрива- |
|
||
Дисперсная система состоит из мелких частиц |
ющих большей частью подземные воды и служа- |
|
||
вещества, распределенного в другом веществе |
щих основой для понимания взглядов авторов на |
|
||
(среде). Система называется гомогенной, если |
генезис подземных вод, на то, какие составляю- |
|
||
внутри нее нет поверхностей раздела, отделяю- |
щие подземных вод и вообще природных вод глав- |
|
||
щих друг от друга части системы, различающиеся |
ные или более важные. Почти все они создавались |
|
||
по свойствам. Гетерогенные системы – системы, |
гидрогеологами и отражают их пристрастия. |
|
||
внутри которых есть такие поверхности раздела. |
Для водоподготовки эти системы имеют опос- |
|
||
Гомогенная система – однофазная, гетерогенная – |
редованное значение – для сравнительного анали- |
|
||
состоит из не менее двух фаз. |
за разных вод в основном в учебных и статисти- |
|
||
При размере частиц примесей воды меньше |
ческих целях. |
|
||
10-3 мкм – это гомогенная система (однофазная из |
Сегодня наиболее употребительны классифи- |
|
||
двух или более индивидуальных веществ). Если |
кационные системы С.А. Щукарева, О.А. Алёкина |
|
||
размер частиц ≥10-3 мкм, то примеси образуют с |
и Л.А. Кульского. Ниже рассмотрены также систе- |
|
||
водой гетерогенную (неоднородную многофазную) |
мы А.И. Перельмана и фирмы Rohm & Haas («Ром |
|
||
систему. |
и Хаас», США). |
|
||
ВОДОПОДГОТОВКА
Библиотека «Аква-Терм»

Часть первая
|
Классификация С.А. Щукарева |
Методы обработки воды, определенные |
||
|
Классификация основана на принципе преобла- |
Л.А. Кульским на основе фазово-дисперсного ана- |
||
|
дания одного или нескольких из трех главных кати- |
лиза примесей воды, описаны ниже (предложения |
||
|
онов (Na+, Ca2+, Mg2+) и трех главных анионов (Cl-, |
Кульского дополнены А. Ашировым – V и VI группы). |
||
|
SО |
2-, HCO -). Вода относится к тому или другому |
Часть перечисленных методов применяется в |
|
|
4 |
3 |
специальных промышленных системах и не при- |
|
|
классу в зависимости от содержания упомянутых |
|||
|
ионов в количестве, превышающем 25%-экв. (сум- |
меняется в коммунальном и энергетическом водо- |
||
|
мы процент-эквивалентов анионов и катионов в |
снабжении. |
||
|
отдельности принимают за 100). Комбинируя типы |
Группа I. Воздействие на взвеси (например, |
||
|
вод по содержанию катионов, получают 49 классов |
седиментация, осветление во взвешенном слое, |
||
|
вод. Например, вода может называться гидрокар- |
осадительное центрифугирование, центробежная |
||
|
бонатной натриево-кальциевой или сульфатно- |
сепарация в гидроциклонах, флотация, фильтро- |
||
|
гидрокарбонатной кальциевой. |
вание на медленных фильтрах и на скорых филь- |
||
|
По общей минерализации каждый класс разде- |
трах по безнапорной схеме и др.). |
||
|
лен на группы: А – менее 1,5 г/л; В – от 1,5 до |
Группа II. Воздействие на коллоидные примеси, |
||
|
10 г/л; С – от 10 до 40 г/л и D – более 40 г/л. |
в том числе высокомолекулярные соединения и |
||
|
Классификация Щукарева очень проста и удоб- |
вирусы: коагуляция, флокуляция, электрокоагуля- |
||
|
на для сопоставления различных по химическому |
ция, электроискровой (разрядный) метод, биохи- |
||
|
составу вод, но громоздка (49 классов, 4 группы). |
мический распад, адсорбция на высокодисперсных |
||
|
Кроме того, деление на классы носит формаль- |
материалах, в том числе глинистых минералах, ио- |
||
|
ный характер, вследствие чего часть классов – не- |
нитах, окисление (хлорирование, озонирование), |
||
|
реальная. |
воздействие ультрафиолетовым, γ- и β-излуче- |
||
|
|
|
нием, потоками нейтронов и др., ультразвуковая |
|
|
Классификация Л.А. Кульского |
обработка, обработка ионами тяжелых металлов |
||
|
Практический интерес представляет фазо- |
(меди, серебра и др.). |
||
|
во-дисперсная классификация примесей воды, |
Группа III. Воздействие на растворенные органи- |
||
|
разработанная Л.А. Кульским (табл. 1.2). Для |
ческие вещества и газы: десорбция газов и легко- |
||
16 |
||||
задач, связанных с очисткой воды, эта класси- |
летучих органических соединений путем аэрирова- |
|||
фикация полезна тем, что, определив фазово- |
ния, термической и вакуумной отгонки, адсорбция |
|||
|
дисперсное состояние примесей в воде и ус- |
на активных углях, природных и синтетических ио- |
||
|
тановив ее принадлежность к какой-то группе, |
нитах и других высокопористых материалах, экстра- |
||
|
можно предварительно выбрать комплекс ме- |
кция не смешивающимися с водой органическими |
||
|
тодов и стадий очистки воды. При этом фазо- |
растворителями, эвапорация (азеотропная отгонка, |
||
|
во-дисперсное состояние примесей должно ус- |
пароциркуляция), пенная флотация, ректификация, |
||
|
танавливаться после каждой стадии обработки |
окисление (жидкофазное, радиационное, электро- |
||
|
воды и учитываться при проектировании всей |
химическое, биологическое, парофазное, хлором, |
||
|
схемы водоподготовки. |
озоном, диоксидом хлора и др.). |
||
Таблица 1.2
Классификация вод по фазово-дисперсному состоянию примесей
Группа |
Наименование примесей |
Размер частиц, мкм |
Характеристика примесей |
|
|
|
|
Гетерогенная система |
|
|
|
|
|
|
|
I |
Взвеси |
>10-1 |
Суспензии и эмульсии, обусловливающие мутность воды; |
|
|
|
микроорганизмы и планктон |
|
|
|
|
II |
Коллоидно-растворенные |
10-1–10-2 |
Коллоиды и высокомолекулярные соединения, обусловливающие |
|
вещества |
|
окисляемость и цветность воды; вирусы |
|
|
|
|
Гомогенная система |
|
|
|
|
|
|
|
III |
Молекулярно-растворенные |
10-2–10-3 |
Газы, растворимые в воде; органические вещества, придающие |
|
вещества |
|
воде запах и привкус |
|
|
|
|
IV |
Вещества, |
<10-3 |
Соли, кислоты, основания, придающие воде жесткость, щелочность |
|
диссоциированные на ионы |
|
и минерализованность |
|
(электролиты) |
|
|
|
|
|
|
|
|
|
|
ВОДОПОДГОТОВКА
Библиотека «Аква-Терм»

Группа IV. Воздействие на примеси ионогенных неорганических веществ: ионный обмен, электродиализ, реагентная обработка, кристаллизация.
Группа V. Воздействие на воду: дистилляция, вымораживание, экстракция кристаллогидратами или смешивающимися с водой органическими растворителями, магнитная обработка, обратный осмос, напорная фильтрация.
Группа VI. Воздействие на водную систему в целом: закачка в подземные горизонты, в глубины морей, захоронение, сжигание. Эти методы применяются только в том случае, если методы первых пяти групп экономически неприемлемы.
Классификация фирмы Rohm & Haas («Ром и Хаас»), США
Классификация вод по материалам фирмы Rohm & Haas подобна классификации Кульского, но дополнительно содержит полезные сведения – табл. 1.3. (Цит. по: В.А. Кишневский).
Часть первая
Классификация О.А. Алёкина
Классификация О.А. Алёкина с поправкой Е.В. Посохова и Ж.С. Сыдыкова сочетает принципы деления вод по преобладающим ионам и по соотношению между ними. Все воды делятся на три класса по преобладающему аниону: гидрокарбонатные (карбонатные), сульфатные и хлоридные. Внутри каждого класса выделяют три группы по преобладанию одного из катионов: кальций, магний, натрий (или натрий + калий).
Классификация А.И. Перельмана
Определенный интерес представляет классификация А.И. Перельмана, выделившего шесть главных таксонов, каждый из которых определяется на основе особого критерия:
группа – температура; тип – окислительно-восстановительные усло-
вия; класс – щелочно-кислотные условия;
Таблица 1.3
Классификация примесей вод по силам, удерживающим их в воде, и методы их удаления
Фазовая характеристика |
Гетерогенные системы |
|
Гомогенные системы |
|
|
|
Группа |
I |
II |
III |
IV |
|
17 |
|
|
|
|
|
|
|
Физико-химическая |
Грубодисперсные |
Примеси коллоидной |
Примеси молекулярной |
Примеси ионной степени |
|
|
характеристика |
примеси: суспензии, |
степени дисперсности: |
степени дисперсности: |
дисперсности: соли, |
|
|
|
эмульсии, планктон, |
органические и |
газы, органические |
кислоты, основания |
|
|
|
|
|||||
|
патогенные |
неорганические |
вещества, соли, |
|
|
|
|
микроорганизмы |
вещества, вирусы, |
кислоты, щелочи, не |
|
|
|
|
|
бактерии |
перешедшие в ионное |
|
|
|
|
|
|
состояние |
|
|
|
|
|
|
|
|
|
|
Поперечный размер |
>10-1 |
10-1–10-2 |
10-2–10-3 |
<10-3 |
|
|
частички, мкм |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Фильтрация |
Ультрафильтрация |
Обратный осмос, нанофильтрация |
|
|
|
|
(механическое удаление) |
|
|
|
|
|
|
Коагуляция |
Десорбция газов и |
Перевод ионов в |
|
|
|
|
|
|
веществ, эвапорация |
малорастворимые |
|
|
|
|
|
трудно-летучих веществ |
соединения |
|
|
|
|
|
|
|
|
|
|
|
Окисление хлором, озоном, перманганатом |
|
|
|
|
|
|
|
|
|
|
|
|
|
Адсорбция на |
Адсорбция на активных |
Фиксация на твердой |
|
|
|
|
гидроксидах и |
углях и других |
фазе ионитов |
|
|
Методы удаления |
|
дисперсных минералах |
материалах |
|
|
|
примесей из воды |
Агрегация при помощи флокулянтов |
Ассоциация молекул |
Моляризация и |
|
|
|
|
(анионных и катионных) |
|
|
комплексо-образование |
|
|
|
|
|
|
|
|
|
|
Флотация |
Электро-форетические |
Экстракция |
Сепарация ионов при |
|
|
|
|
методы |
органическими |
различном фазовом |
|
|
|
Электролиз сине- |
|
|
|||
|
|
растворителями |
состоянии воды |
|
|
|
|
зеленых водорослей |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Бактерицидное |
Вирулицидное |
Биохимический распад |
Использование |
|
|
|
воздействие |
воздействие |
|
подвижности ионов в |
|
|
|
|
|
|
электрическом поле |
|
|
|
|
|
|
|
|
|
Силы, удерживающие |
Гидродинамические |
Электростатические |
Вандерваальсовые |
Ионные силы растворов |
|
|
примеси в воде |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ВОДОПОДГОТОВКА
Библиотека «Аква-Терм»

Часть первая
|
семейство – общая минерализация; |
При содержании в воде взвешенных веществ |
|
|
род – растворенное органическое вещество; |
менее 2–3 мг/л или больше указанных значений, |
|
|
вид – ведущие катионы и анионы (кроме Н+ и |
но условный диаметр частиц меньше 1 · 10-4 мм, |
|
|
ОН-). |
определение загрязненности воды производят |
|
|
В этой классификации, в отличие от многих |
косвенно по мутности воды. |
|
|
других, в том числе описанных классификаций |
1.3.2. Мутность и прозрачность |
|
|
Щукарева и Алёкина, учитываются температура, |
||
|
органические вещества, газы. А.И. Перельман |
Мутность воды вызвана присутствием тонкодис- |
|
|
предложил также изображать воду в виде шести- |
персных примесей, обусловленных нерастворимы- |
|
|
значного числа – по количеству таксонов и разно- |
ми или коллоидными неорганическими и органи- |
|
|
видностей, которых в каждом таксоне – не более |
ческими веществами различного происхождения. |
|
|
девяти. |
Качественное определение проводят описательно: |
|
|
|
мутность не заметна (отсутствует), слабая опа- |
|
|
|
лесценция, опалесценция, слабомутная, мутная и |
|
|
1.3. Физико-химические |
сильная муть. |
|
|
В России мутность чаще всего измеряют в не- |
||
|
показатели качества |
фелометрических единицах мутности НЕФ (NTU) |
|
|
природных вод |
для небольших значений в пределах 0–40 НЕФ |
|
|
|
(NTU), например для питьевой воды. В условиях |
|
|
Под качеством природной воды в целом пони- |
большой мутности обычно применяется измере- |
|
|
мается характеристика ее состава и свойств, оп- |
ние единиц мутности по формазину (ЕМФ). Преде- |
|
|
ределяющая ее пригодность для конкретных видов |
лы измерений – 40–400 ЕМФ. |
|
|
водопользования (ГОСТ 17.1.1.01–77), при этом |
Индикатор по НЕФ (NTU) – рассеивание излуче- |
|
|
критерии качества представляют собой признаки, |
ния, по ЕМФ – ослабление потока излучения. Соот- |
|
|
по которым производится оценка качества воды. |
ношение различных единиц измерения в П.1.3.4. |
|
|
1.3.1. Взвешенные примеси |
Наряду с мутностью, особенно в случаях, когда |
|
|
вода имеет незначительные окраску и мутность, и |
||
18 |
|||
Взвешенные твердые примеси, присутствую- |
их определение затруднительно, пользуются пока- |
||
щие в природных водах, состоят из частиц гли- |
зателем «прозрачность». |
||
|
ны, песка, ила, суспендированных органических и |
Мера прозрачности – высота столба воды, при |
|
|
неорганических веществ, планктона и различных |
которой можно наблюдать опускаемую в воду |
|
|
микроорганизмов. Взвешенные частицы влияют |
белую пластину определенных размеров (диск |
|
|
на прозрачность воды. |
Секки) или различать на белой бумаге шрифт |
|
|
Содержание в воде взвешенных примесей, из- |
определенного размера и типа (шрифт Снел- |
|
|
меряемое в мг/л, дает представление о загрязнен- |
лена). Результаты выражаются в сантиметрах |
|
|
ности воды частицами в основном условным диа- |
(табл. 1.5). |
|
|
метром более 1·10-4 мм – табл. 1.4. |
Дополнительно см. П.1.34. |
Таблица 1.4
Характеристика вод по содержанию взвешенных примесей
Размер частиц |
Гидравлическая крупность |
Примесь (условно) |
Время осаждения частиц |
(приблизительный), мм |
(скорость осаждения в лабораторном |
|
на 1 м |
|
цилиндре в течение 2 ч), мм/с |
|
|
|
|
|
|
1,0 |
100 |
Крупный песок |
10 с |
|
|
|
|
0,5 |
53 |
Средний песок |
20 с |
|
|
|
|
0,1 |
6,9 |
Мелкий песок |
2,5 мин |
|
|
|
|
0,050–0,027 |
1,7–0,5 |
Крупный ил |
10–30 мин |
|
|
|
|
0,010–0,005 |
0,070–0,017 |
Мелкий ил |
4–18 ч |
|
|
|
|
0,0027 |
0,005 |
Крупная глина |
2 сут |
|
|
|
|
0,0010–0,0005 |
0,00070–0,00017 |
Тонкая глина |
0,5–2 мес |
|
|
|
|
0,0002–0,000001 |
0,000007 |
Коллоидные частицы |
4 года |
|
|
|
|
ВОДОПОДГОТОВКА
Библиотека «Аква-Терм»

Часть первая
Таблица 1.5
Характеристика вод по прозрачности
Прозрачность |
Единица измерения, см |
|
|
Прозрачная |
Более 30 |
|
|
Маломутная |
Более 25 до 30 |
|
|
Средней мутности |
Более 20 до 25 |
|
|
Мутная |
Более 10 до 20 |
|
|
Очень мутная |
Менее 10 |
|
|
1.3.3. Запах
Характер и интенсивность запаха природной воды определяют органолептически. По характеру запахи делят на две группы:
естественного происхождения (живущие и отмершие в воде организмы, загнивающие растительные остатки и др.) – табл.1.6;
искусственного происхождения (примеси промышленных и сельскохозяйственных сточных вод).
Интенсивность запаха по ГОСТ 3351-74* оценивают в шестибалльной шкале – табл. 1.7.
Запахи второй группы (искусственного происхождения) называют по определяющим запах веществам: хлорный, бензиновый и т.д.
Таблица 1.6
Запахи естественного происхождения
Обозначение запаха |
Характер запаха |
Примерный род запаха |
|
|
|
|
|
|
|
А |
Ароматический |
Огуречный, цветочный |
|
|
|
|
|
|
|
Б |
Болотный |
Илистый, тинистый |
|
|
|
|
|
|
|
Г |
Гнилостный |
Фекальный, сточный |
|
|
|
|
|
|
|
Д |
Древесный |
Запах морской щепы, древесной коры |
|
19 |
|
|
|
|
|
З |
Землистый |
Прелый, запах свежевспаханной земли, глинистый |
|
|
|
|
|||
|
|
|
|
|
П |
Плесневый |
Затхлый, застойный |
|
|
|
|
|
|
|
Р |
Рыбный |
Запах рыбьего жира, рыбы |
|
|
|
||||
|
|
|
|
|
С |
Сероводородный |
Запах тухлых яиц |
|
|
|
|
|
|
|
Т |
Травянистый |
Запах скошенной травы, сена |
|
|
|
|
|
|
|
Н |
Неопределенный |
Запахи естественного происхождения, не подходящие под предыдущие определения |
|
|
|
|
|
|
|
Таблица 1.7
Характеристика вод по интенсивности запаха
Интенсивность запаха, |
Характеристика |
Описательные определения |
баллы |
|
|
0 |
Запаха нет |
Отсутствие ощутимого запаха |
|
|
|
1 |
Очень слабый |
Запах, не замечаемый потребителем, но обнаруживаемый опытным |
|
|
исследователем |
|
|
|
2 |
Слабый |
Запах, не привлекающий внимания потребителя, но обнаруживаемый им, если |
|
|
указать на него |
|
|
|
3 |
Заметный |
Запах, легко обнаруживаемый и могущий дать повод относиться к воде с |
|
|
неодобрением |
|
|
|
4 |
Отчетливый |
Запах, обращающий на себя внимание и делающий воду неприятной для питья |
|
|
|
5 |
Очень сильный |
Запах сильный настолько, что делает воду непригодной для питья |
|
|
|
ВОДОПОДГОТОВКА
Библиотека «Аква-Терм»
