
2л3
.pdf
Применение диоксида титана в
фармации
•TiO2 – используется в качестве добавки в полимеры (полиэтилен, полипропилен) для придания им непрозрачности, чтобы защитить лекарственное средство от света (таблетки, покрытые оболочкой). После покрытия такой
оболочкой лекарственные средства можно не хранить в защищенном от света месте.

Циркониевый браслет
•Цирконий не играет биологической роли в организме. Металлический цирконий и его нерастворимые соединения (оксид, силикат) обладают высокой биологической инертностью.

Ядовитость ванадия
•Установлено, что ванадий может тормозить синтез жирных кислот, подавлять образование холестерина. Ванадий ингибирует ряд ферментных систем, тормозит фосфорилирование и синтез АТФ,
стимулирует активность моноаминоксидазы и окислительное фосфорилирование.
•При остром воздействии токсических доз ванадия отмечаются местные воспалительные реакции кожи и слизистых оболочек глаз, верхних дыхательных путей, скопление слизи в бронхах и альвеолах, лейкопения и анемия.

Применение метаванадата аммония в
фармации
•NH4VO3 – как сильный окислитель
используется в качестве титрованного раствора для количественного определения лекарственных веществ,
обладающих восстановительными свойствами (ванадатометрия),
например, изониазида

Применение метаванадата аммония в
фармации
•VO3- + 2H+ + e → VO2 + H2O
•NH4VO3 – входит в состав молибденованадиевого реактива (МВР)
((NH4)2MoO4 + NH4VO3) – используется для
обнаружения фосфат-ионов
•PO43- + МВР = желтое окрашивание
•VitB6 + NH4VO3 = сине-фиолетовая окраска

Применение соединений молибдена в
фармации
•((NH4)2MoO4 + NH4VO3) – молибденовованадиевый реактив – обнаружение PO43-
•(NH4)2MoO4 – обнаружение PO43-, скополамина
•H3PO4 + 12(NH4)2MoO4 + 21HNO3 → (NH4)3PO4·12MoO3↓ + 21NH4NO3 + 12H2O желтый
•H3PO4·12MoO3 – фосфорномолибденовая кислота –
общеалкалоидный осадительный реактив

Применение соединений вольфрама в
фармации
•H3PO4·12WO3 – фосфорновольфрамовая кислота – общеалкалоидный осадительный
реактив
•H8[Si(W2O7)6] – кремневольфрамовая кислота – общеалкалоидный осадительный
реактив

Гетерополикислоты
Гетерополикислоты – это комплексные
соединения анионного типа, содержащие во
внутренней координационной сфере в
качестве лигандов анионы неорганических
изополикислот (молибденовых,
вольфрамовых, реже ванадиевых, ниобиевых
и др.), а в качестве атома-
комплексообразователя (гетеро-атома)
служат P(V), As(V), Si(IV), Ge(IV), Ti(IV), Ce(IV).
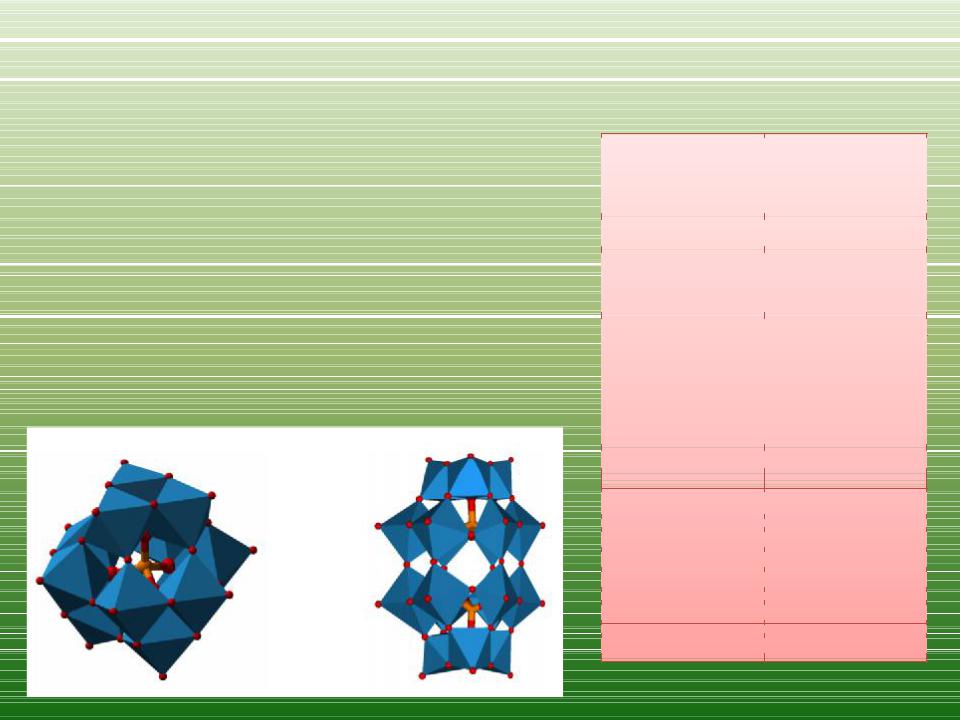
Гетерополикислоты
|
|
pH |
Основные |
||||||
• |
Гетероатом = p-элемент |
компоненты |
|||||||
|
|||||||||
1,0 |
[PW |
12 |
O |
]3− |
|||||
• |
Металл = d-элемент |
|
|
|
40 |
|
|||
|
[PW |
|
O ]3−, |
||||||
|
|
2,2 |
|
12 |
|
40 |
|
||
|
|
[P W |
21 |
O ]6−, |
|||||
• |
Атомы кислорода |
|
2 |
|
71 |
||||
|
[PW |
|
O ]7− |
||||||
|
|
|
|
11 |
|
39 |
|
||
|
|
|
[PW |
|
O ]3−, |
||||
• |
Атомы водорода |
|
|
12 |
|
40 |
|
||
3,5 |
[P2W21O71]6−, |
||||||||
|
|
[PW |
11 |
O |
]7−, |
||||
|
|
|
|
|
39 |
|
|||
|
|
|
[P W |
18 |
O ]6−, |
||||
|
|
|
2 |
|
62 |
||||
|
|
|
[P W |
19 |
O |
]10− |
|||
|
|
|
2 |
|
67 |
||||
|
|
|
[P W |
21 |
O ]6−, |
||||
|
|
5,4 |
2 |
|
71 |
||||
|
|
[PW |
11 |
O |
]7−, |
||||
|
|
|
|
|
39 |
]6− |
|||
|
|
|
[P W |
18 |
O |
||||
|
|
|
2 |
|
62 |
||||
|
|
7,3 |
[PW O |
]9− |
|||||
|
|
|
|
9 |
|
34 |
|
||
|
|
8,3 |
PO43−, WO42− |
||||||

Применение сульфата церия (IV) в
количественном анализе
•Ce(SO4)2 – как сильный окислитель
используется в качестве титрованного раствора для количественного определения лекарственных веществ,
обладающих восстановительными
свойствами, H2O2, ионов: As3+; I-; Sb3+; Mo5+; Sn2+; S2O32-; Tl+; и т.д. (цериметрическое титрование)
