
1_kollok_Belki_fermenty
.docxИз других гликопротеинов, выполняющих ряд важнейших биологических функций, следует отметить все белки плазмы крови (за исключением альбуминов), трансферрин, церулоплазмин, гонадотропный и фолликуло-стимулирующие гормоны, некоторые ферменты, а также гликопротеины в составе слюны (муцин), хрящевой и костной тканей и яичного белка (овомукоид). Углеводные компоненты, помимо информативной функции, значительно повышают стабильность молекул, в состав которых они входят, к различного рода химическим, физическим воздействиям и предохраняют их от действия протеиназ, определяя тем самым биологическую роль гликопротеинов. Являясь составной частью клеточной мембраны, гликопротеины участвуют, кроме того, в иммунологических реакциях, ионном обмене, процессах межклеточной адгезии и т.д.
№20.Протеогликаны.
Протеогликаны — гликопротеины с высокой степенью гликозилирования, углеводные остатки которых представляют собой длинные неразветвленные полисахаридные цепи — гликозаминогликаны, образованные чередующимися остатками гексозамина и уроновой кислоты (глюкуроновой, идуроновой или галактуроновой) либо галактозы. Гликозаминогликановые цепи гликопротеинов зачастую сульфированы[1].
Протеогликаны являются одним из основных компонентов внеклеточного матрикса соединительной ткани.
Протеогликаны состоят из сердцевинных белков (лат. core protein) с молекулярной массой от 10 до 600 кДа, с которыми ковалентно связаны несколько гликозаминогликановых цепей (до 80 гликозидных звеньев массой до 50 - 60 кДа); число связанных с белком полисахаридных цепей варьирует от одной (декорин фибробластов) до ста и выше (аггрекан хрящевой ткани). Такое строение обуславливает высокую молекулярную массу протеогликанов (у аггрекана до 5 МДа), при этом на белковую часть приходится ~5-10% и на углеводную ~90-95% массы.
Сердцевинные белки протеогликанов, как и другие белки, синтезируются рибосомами шероховатого эндоплазматического ретикулума и транспортируются в аппарат Гольджи, где происходит их гликозилирование. На первой стадии происходит «наращивание» на сериновом остатке сердцевинного белка «связующего тетрасахарида» (англ. proteoglycan linkage tetrasaccharide) «ксилоза-галактоза-галактоза-глюкуроновая кислота»(ß1-4Xyl ß1-3Gal ß1-3Gal GlcA), после чего соответствующими гликозилтрансферазами осуществяется наращивание специфичной для данного протеогликана гликозиламиногликановой цепи.
№21.Мукополисахаридозы.
Мукополисахаридозы или сокращенно МПС, или MPS (от (мукополисахариды + -ōsis)) — группа метаболических заболеваний соединительной ткани, связанных с нарушением обмена кислых гликозаминогликанов (GAG, мукополисахаридов), вызванных недостаточностью лизосомных ферментов обмена гликозаминогликанов. Заболевания связаны с наследственными аномалиями обмена, проявляются в виде «болезни накопления» и приводят к различным дефектам костной, хрящевой, соединительной тканей.
Виды заболеваний
В зависимости от характера ферментативного дефекта выделяют несколько основных типов мукополисахаридозов:
I тип — синдром Гурлер (мукомполисахаридоз I H — Hurler), синдром Гурлера-Шейе (мукополисахаридоз I H/S — Hurler-Scheie), синдром Шейе (мукополисахаридоз I S — Scheie). Обусловлен дефицитом альфа-L-идуронидазы (фермент катаболизма мукополисахаридов). Заболевание постепенно приводит к накоплению в тканях гепарансульфата и дерматансульфата. Выделяют три фенотипа: синдром Гурлера, синдром Шейе и синдром Гурлера-Шейе.
II тип — синдром Хантера
III тип — синдром Санфилиппо
IV тип — синдром Моркио
V тип — синдром Шейе
VI тип — синдром Марото—Лами
VII тип — синдром Слая дефицит р-глюкуронидазы
№22.Хромопротеины.
Сложные белки, как было отмечено, содержат два компонента – простой белок и небелковое вещество. Последнее называют простетической группой (от греч. prostheto – присоединяю). Простетические группы, как правило, прочно связаны с белковой молекулой. Далее представлены сведения о химической природе и биологической роли некоторых сложных белков.
ХРОМОПРОТЕИНЫ
Хромопротеины (от греч. chroma – краска) состоят из простого белка и связанного с ним окрашенного небелкового компонента. Различают гемопротеины (содержат в качестве простетической группы железо), маг-нийпорфирины и флавопротеины (содержат производные изоаллоксазина). Хромопротеины наделены рядом уникальных биологических функций: они участвуют в таких фундаментальных процессах жизнедеятельности, как фотосинтез, дыхание клеток и целостного организма, транспорт кислорода и диоксида углерода, окислительно-восстановительные реакции, свето-и цветовосприятие и др.
Таким образом, хромопротеины играют исключительно важную роль в процессах жизнедеятельности. Например, подавление дыхательной функции гемоглобина путем введения оксида углерода (СО) либо утилизации (потребление) кислорода в тканях путем введения синильной кислоты или ее солей (цианидов), ингибирующих ферментные системы клеточного дыхания, моментально приводит к смерти организма.
Хромопротеины являются непременными и активными участниками аккумулирования энергии, начиная от фиксации солнечной энергии в зеленых растениях и утилизации ее до превращений в организме животных и человека. Хлорофилл (магнийпорфирин) вместе с белком обеспечивает фотосинтетическую активность растений, катализируя расщепление молекулы воды на водород и кислород (поглощением солнечной энергии). Гемопротеины (железопорфирины), напротив, катализируют обратную реакцию – образование молекулы воды, связанное с освобождением энергии.
№23.Строение гемоглобина.
Гемоглобин-белок, включающий 4 гемсодержащие белковые субъединицы. Между собой протомеры соединяются гидрофобными, ионными, водородными связями по принципу комплементарности. При этом они взаимодействуют не произвольно, а определенным участком - контактной поверхностью. Этот процесс высокоспецифичен, контакт происходит одновременно в десятках точек по принципу комплементарности. Взаимодействие осуществляют разноименно заряженные группы, гидрофобные участки, неровности на поверхности белка.
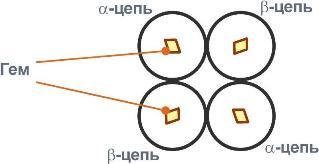
Белковые субъединицы в нормальном гемоглобине могут быть представлены различными типами полипептидных цепей: α, β, γ, δ, ε, ξ (соответственно, греч. - альфа, бета, гамма, дельта, эпсилон, кси). В состав молекулы гемоглобина входят по две цепи двух разных типов.
Гем соединяется с белковой субъединицей, во-первых, через остаток гистидина координационной связью железа, во-вторых, через гидрофобные связи пиррольных колец и гидрофобных аминокислот. Гем располагается как бы "в кармане" своей цепи и формируется гемсодержащий протомер.
Нормальные формы гемоглобина
Существует несколько нормальных вариантов гемоглобина:
HbР – примитивный гемоглобин, содержит 2ξ- и 2ε-цепи, встречается в эмбрионе между 7-12 неделями жизни,
HbF – фетальный гемоглобин, содержит 2α- и 2γ-цепи, появляется через 12 недель внутриутробного развития и является основным после 3 месяцев,
HbA – гемоглобин взрослых, доля составляет 98%, содержит 2α- и 2β-цепи, у плода появляется через 3 месяца жизни и к рождению составляет 80% всего гемоглобина,
HbA2 – гемоглобин взрослых, доля составляет 2%, содержит 2α- и 2δ-цепи,
HbO2 – оксигемоглобин, образуется при связывании кислорода в легких, в легочных венах его 94-98% от всего количества гемоглобина,
HbCO2 – карбогемоглобин, образуется при связывании углекислого газа в тканях, в венозной крови составляет 15-20% от всего количества гемоглобина.
Патологические формы гемоглобина
HbS – гемоглобин серповидно-клеточной анемии.
MetHb – метгемоглобин, форма гемоглобина, включающая трехвалентный ион железа вместо двухвалентного. Такая форма обычно образуется спонтанно, в этом случае ферментативных мощностей клетки хватает на его восстановление. При использовании сульфаниламидов, употреблении нитрита натрия и нитратов пищевых продуктов, при недостаточности аскорбиновой кислоты ускоряется переход Fe2+ в Fe3+. Образующийся metHb не способен связывать кислород и возникает гипоксия тканей. Для восстановления ионов железа в клинике используют аскорбиновую кислоту и метиленовую синь.
Hb-CO – карбоксигемоглобин, образуется при наличии СО (угарный газ) во вдыхаемом воздухе. Он постоянно присутствует в крови в малых концентрациях, но его доля может колебаться от условий и образа жизни.
Угарный газ является активным ингибитором гем-содержащих ферментов, в частности, цитохромоксидазы 4-го комплекса дыхательной цепи.
HbA1С – гликозилированный гемоглобин. Концентрация его нарастает при хронической гипергликемии и является хорошим скрининговым показателем уровня глюкозы крови за длительный период времени.
№24.Производные гемоглобина.
В соответствии с функциональным назначением гемоглобина в физиологических условиях в организме образуются такие его производные, как: оксигемоглобин, карбгемогло-бин, и в следовых количествах — карбоксигемоглобин и метгемоглобин.
Оксигемоглобин (НbO2) образуется при обогащении крови кислородом в легких, за счет присоединения кислорода к гему гемоглобина при помощи координационных связей железа без изменения валентности железа.
Оксигемоглобин очень лабильное соединение и, поступая с кровью к тканям, где давление кислорода значительно ниже, чем в легких, он легко диссоциирует на свободный гемоглобин и кислород. Кислород утилизируется в процессе клеточного дыхания, а гемоглобин вступает в соединение с углекислым газом, образуя карбгемоглобин (НbСO2). Это также непрочное соединение, которое легко отдает углекислый газ при поступлении крови в легкие. Связь с углекислым газом образует не гем, а глобин за счет свободных аминогрупп аминокислот.
Карбоксигемоглобин (НbСО) — это соединение гемоглобина с окисью углерода. Образуется в результате диссимиляции гемоглобина и в норме не превышает 2% от общей массы гемоглобина. Карбоксигемоглобин, в отличие от других производных гемоглобина, является очень прочным соединением. СО образует ковалентную связь с гемоглобином, блокируя ассоциацию с ним кислорода. Сродство СО к гемоглобину более чем в 200 раз выше сродства кислорода. При отравлении угарным газом (СО), когда образуются значительные количества карбоксигемоглобина, гемоглобин теряет способность связывать кислород. Кроме того, СО способен попадать в клетки и ингибировать дыхательную цепь в митохондриях. Все это приводит к тканевой гипоксии, ацидозу, депрессии центральной нервной системы, блокаде дыхательного центра и наступает смерть от удушья.
Метгемоглобин (МетНb)—образуется при окислении двухвалентного железа гема в трехвалентное. При этом отмечается и переход окраски из красной в коричнево-зеленоватую. В норме метгемоглобин образуется за счет процессов аутоокисления и не превышает 2% от общей массы гемоглобина, так как небольшое количество образуемого трехвалентного железа до двухвалентного восстанавливает фермент метгемоглобин-редуктаза. Этот фермент позволяет поддерживать уровень MetHb в крови на очень низких цифрах.
При патологии количество МетНb в крови возрастает. Развивается состояние метгемоглобинемии, которое может быть следствием генетической патологии — генетически обусловленным дефицитом MetHb-редуктазы, либо носить приобретенный характер. Например, при отравлении окислами азота, цианидами и др. Образующиеся значительные количества метгемоглобина могут вызвать смерть от недостатка кислорода, так как метгемоглобин лишен способности связываться с кислородом.
№25,26.Липопротеины.
Липопротеи́ны (липопротеиды) — класс сложных белков, простетическая группа которых представлена каким-либо липидом. Так, в составе липопротеинов могут быть свободные жирные кислоты, нейтральные жиры, фосфолипиды, холестериды.
Липопротеины представляют собой комплексы, состоящие из белков (аполипопротеинов; сокращенно — апо-ЛП) и липидов, связь между которыми осуществляется посредством гидрофобных и электростатических взаимодействий.
Липопротеины подразделяют на свободные, или растворимые в воде (липопротеины плазмы крови, молока и др.), и нерастворимые, т. н. структурные (липопротеины мембран клетки, миелиновой оболочки нервных волокон, хлоропластов растений).
Среди свободных липопротеинов (они занимают ключевое положение в транспорте и метаболизме липидов) наиболее изучены липопротеины плазмы крови, которые классифицируют по их плотности. Чем выше содержание в них липидов, тем ниже плотность липопротеинов. Различают липопротеины очень низкой плотности (ЛПОНП), низкой плотности (ЛПНП), высокой плотности (ЛПВП) и хиломикроны. Каждая группа липопротеинов очень неоднородна по размерам частиц (наиболее крупные — хиломикроны) и содержанию в ней апо-липопротеинов. Все группы липопротеинов плазмы содержат полярные и неполярные липиды в разных соотношениях.
Виды липопротеиновВид Размеры Функция
Липопротеины высокой плотности (ЛВП) 8-11 нм Транспорт холестерина от периферийных тканей к печени
Липопротеины низкой плотности (ЛНП) 18-26 нм Транспорт холестерина, триацилглицеридов и фосфолипидов от печени к периферийным тканям
Липопротеины промежуточной (средней) плотности ЛПП (ЛСП) 25-35 нм Транспорт холестерина, триацилглицеридов и фосфолипидов от печени к периферийным тканям
Липопротеины очень низкой плотности (ЛОНП) 30-80 нм Транспорт холестерина, триацилглицеридов и фосфолипидов от печени к периферийным тканям
Хиломикроны 75-1200 нм Транспорт холестерина и жирных кислот, поступающих с пищей, из кишечника в периферические ткани и печень
Нековалентная связь в липопротеинах между белками и липидами имеет важное биологическое значение. Она обусловливает возможность свободного обмена липидов и модуляцию свойств липопротеинов в организме.
Липопротеины являются:
структурными элементами мембран клеток животных организмов;
транспортными белками, транспортирующими холестерин и другие стероиды, фосфолипиды и др.
№27.Биологические мембраны.
Кле́точная мембра́на (или цитолемма, или плазмалемма, или плазматическая мембрана) отделяет содержимое любой клетки от внешней среды, обеспечивая её целостность; регулируют обмен между клеткой и средой; внутриклеточные мембраны разделяют клетку на специализированные замкнутые отсеки — компартменты или органеллы, в которых поддерживаются определённые условия среды.
Клеточная стенка, если таковая у клетки имеется (обычно есть у растительных клеток), покрывает клеточную мембрану.
Клеточная мембрана представляет собой двойной слой (бислой) молекул класса липидов, большинство из которых представляет собой так называемые сложные липиды — фосфолипиды. Молекулы липидов имеют гидрофильную («головка») и гидрофобную («хвост») часть. При образовании мембран гидрофобные участки молекул оказываются обращены внутрь, а гидрофильные — наружу. Мембраны — структуры инвариабельные, весьма сходные у разных организмов. Некоторое исключение составляют, пожалуй, археи, у которых мембраны образованы глицерином и терпеноидными спиртами. Толщина мембраны составляет 7—8 нм.
Биологическая мембрана включает и различные белки: интегральные (пронизывающие мембрану насквозь), полуинтегральные (погруженные одним концом во внешний или внутренний липидный слой), поверхностные (расположенные на внешней или прилегающие к внутренней сторонам мембраны). Некоторые белки являются точками контакта клеточной мембраны с цитоскелетом внутри клетки, и клеточной стенкой (если она есть) снаружи. Некоторые из интегральных белков выполняют функцию ионных каналов, различных транспортеров и рецепторов.
Функции
барьерная — обеспечивает регулируемый, избирательный, пассивный и активный обмен веществ с окружающей средой. Например, мембрана пероксисом защищает цитоплазму от опасных для клетки пероксидов. Избирательная проницаемость означает, что проницаемость мембраны для различных атомов или молекул зависит от их размеров, электрического заряда и химических свойств. Избирательная проницаемость обеспечивает отделение клетки и клеточных компартментов от окружающей среды и снабжение их необходимыми веществами.
транспортная — через мембрану происходит транспорт веществ в клетку и из клетки. Транспорт через мембраны обеспечивает: доставку питательных веществ, удаление конечных продуктов обмена, секрецию различных веществ, создание ионных градиентов, поддержание в клетке оптимального pH и концентрации ионов, которые нужны для работы клеточных ферментов.
Частицы, по какой-либо причине неспособные пересечь фосфолипидный бислой (например, из-за гидрофильных свойств, так как мембрана внутри гидрофобна и не пропускает гидрофильные вещества, или из-за крупных размеров), но необходимые для клетки, могут проникнуть сквозь мембрану через специальные белки-переносчики (транспортеры) и белки-каналы или путем эндоцитоза.
При пассивном транспорте вещества пересекают липидный бислой без затрат энергии по градиенту концентрации путем диффузии. Вариантом этого механизма является облегчённая диффузия, при которой веществу помогает пройти через мембрану какая-либо специфическая молекула. У этой молекулы может быть канал, пропускающий вещества только одного типа.
Активный транспорт требует затрат энергии, так как происходит против градиента концентрации. На мембране существуют специальные белки-насосы, в том числе АТФаза, которая активно вкачивает в клетку ионы калия (K+) и выкачивают из неё ионы натрия (Na+).
матричная — обеспечивает определенное взаиморасположение и ориентацию мембранных белков, их оптимальное взаимодействие.
механическая — обеспечивает автономность клетки, ее внутриклеточных структур, также соединение с другими клетками (в тканях). Большую роль в обеспечение механической функции имеют клеточные стенки, а у животных — межклеточное вещество.
энергетическая — при фотосинтезе в хлоропластах и клеточном дыхании в митохондриях в их мембранах действуют системы переноса энергии, в которых также участвуют белки;
рецепторная — некоторые белки, находящиеся в мембране, являются рецепторами (молекулами, при помощи которых клетка воспринимает те или иные сигналы).
Например, гормоны, циркулирующие в крови, действуют только на такие клетки-мишени, у которых есть соответствующие этим гормонам рецепторы. Нейромедиаторы (химические вещества, обеспечивающие проведение нервных импульсов) тоже связываются с особыми рецепторными белками клеток-мишеней.
ферментативная — мембранные белки нередко являются ферментами. Например, плазматические мембраны эпителиальных клеток кишечника содержат пищеварительные ферменты.
осуществление генерации и проведения биопотенциалов.
С помощью мембраны в клетке поддерживается постоянная концентрация ионов: концентрация иона К+ внутри клетки значительно выше, чем снаружи, а концентрация Na+ значительно ниже, что очень важно, так как это обеспечивает поддержание разности потенциалов на мембране и генерацию нервного импульса.
маркировка клетки — на мембране есть антигены, действующие как маркеры — «ярлыки», позволяющие опознать клетку. Это гликопротеины (то есть белки с присоединенными к ним разветвленными олигосахаридными боковыми цепями), играющие роль «антенн». Из-за бесчисленного множества конфигурации боковых цепей возможно сделать для каждого типа клеток свой особый маркер. С помощью маркеров клетки могут распознавать другие клетки и действовать согласованно с ними, например, при формировании органов и тканей. Это же позволяет иммунной системе распознавать чужеродные антигены.
Структура и состав биомембран
Мембраны состоят из липидов трёх классов: фосфолипиды, гликолипиды и холестерол. Фосфолипиды и гликолипиды (липиды с присоединёнными к ним углеводами) состоят из двух длинных гидрофобных углеводородных «хвостов», которые связаны с заряженной гидрофильной «головой». Холестерол придаёт мембране жёсткость, занимая свободное пространство между гидрофобными хвостами липидов и не позволяя им изгибаться. Поэтому мембраны с малым содержанием холестерола более гибкие, а с большим — более жёсткие и хрупкие. Также холестерол служит «стопором», препятствующим перемещению полярных молекул из клетки и в клетку. Важную часть мембраны составляют белки, пронизывающие её и отвечающие за разнообразные свойства мембран. Их состав и ориентация в разных мембранах различаются.
Клеточные мембраны часто асимметричны, то есть слои отличаются по составу липидов, переход отдельной молекулы из одного слоя в другой (так называемый флип-флоп) затруднён.
№28.Липосомы.
Липосомы — самопроизвольно образующиеся в смесях фосфолипидов с водой замкнутые пузырьки. Их стенка состоит из одного или нескольких бислоёв фосфолипидов (слоёв толщиной в две молекулы), в которые могут быть встроены другие вещества (например, белки). Внутри липосом содержится вода или раствор.
Диаметр липосом варьирует от 20 нм (моноламеллярные везикулы, стенка состоит из одного бислоя) до 10-50 мкм (мультиламеллярные везикулы, стенка состоит из десятков или сотен бислоёв).
Применение в медицине
С помощью липосом изучают воздействие на мембраны витаминов, гормонов, антибиотиков и других препаратов. Для ядовитых препаратов важным является точная их доставка к больному органу или ткани, минуя остальные части организма. Липосомы успешно используются, как носители лекарств, поскольку:
по химическому составу липосомы сходны с природными мембранами клеток;
липосомы универсальны, что позволяет переносить широкий спектр медицинских химических препаратов;
не вызывают аллергических реакций.
Липосомы широко применяются в экспериментальной онкологии. Однако есть ряд трудностей использования липосом в медицине. Во-первых, липосомы поглощаются клетками ретикуло-эндотелиальной системы, причём большее их количество находится в печени, селезенке, костном мозге, лимфатических узлах и кровотоке. Поэтому доставка лекарственных препаратов с помощью липосом в другие органы и части организма является более сложной задачей. Во-вторых, липопротеины, обмениваясь с липосомами липидами, способствуют разрушению липосом и вытеканию наружу их содержимого. Также стоит задача увеличения сроков хранения липосом после их приготовления.
№29.Ферменты.
Ферме́нты, или энзи́мы (от лат. fermentum, греч. ζύμη, ἔνζυμον — закваска) — обычно белковые молекулы или молекулы РНК (рибозимы) или их комплексы, ускоряющие (катализирующие) химические реакции в живых системах. Реагенты в реакции, катализируемой ферментами, называются субстратами, а получающиеся вещества — продуктами. Ферменты специфичны к субстратам (АТФаза катализирует расщепление только АТФ, а киназа фосфорилазы фосфорилирует только фосфорилазу).
Ферментативная активность может регулироваться активаторами и ингибиторами (активаторы — повышают, ингибиторы — понижают).
Белковые ферменты синтезируются на рибосомах, а РНК — в ядре.
Термины «фермент» и «энзим» давно используют как синонимы (первый в основном в русской и немецкой научной литературе, второй — в англо- и франкоязычной).
Наука о ферментах называется энзимологией, а не ферментологией (чтобы не смешивать корни слов латинского и греческого языков).Содержание [убрать]
1 История изучения
2 Функции ферментов
3 Классификация ферментов
4 Соглашения о наименовании ферментов
5 Кинетические исследования
6 Структура и механизм действия ферментов
6.1 Активный центр ферментов
История изучения
Термин фермент предложен в XVII веке химиком ван Гельмонтом при обсуждении механизмов пищеварения.
В кон. ХVIII — нач. XIX вв. уже было известно, что мясо переваривается желудочным соком, а крахмал превращается в сахар под действием слюны. Однако механизм этих явлений был неизвестен[1].
В XIX в. Луи Пастер, изучая превращение углеводов в этиловый спирт под действием дрожжей, пришёл к выводу, что этот процесс (брожение) катализируется некой жизненной силой, находящейся в дрожжевых клетках.
Более ста лет назад термины фермент и энзим отражали различные точки зрения в теоретическом споре Л. Пастера с одной стороны, и М. Бертло и Ю. Либиха — с другой, о природе спиртового брожения. Собственно ферментами (от лат. fermentum — закваска) называли «организованные ферменты» (то есть сами живые микроорганизмы), а термин энзим (от греч. ἐν- — в- и ζύμη — дрожжи, закваска) предложен в 1876 году В. Кюне для «неорганизованных ферментов», секретируемых клетками, например, в желудок (пепсин) или кишечник (трипсин, амилаза). Через два года после смерти Л. Пастера в 1897 году Э. Бухнер опубликовал работу «Спиртовое брожение без дрожжевых клеток», в которой экспериментально показал, что бесклеточный дрожжевой сок осуществляет спиртовое брожение так же, как и неразрушенные дрожжевые клетки. В 1907 году за эту работу он был удостоен Нобелевской премии. Впервые высокоочищенный кристаллический фермент (уреаза) был выделен в 1926 году Дж. Самнером. В течение последующих 10 лет было выделено еще несколько ферментов, и белковая природа ферментов была окончательно доказана.
№30.Свойства ферментов.
Ферменты называют катализаторами белковой природы, так как они в миллионы раз ускоряют течение отдельных химических реакций. Благодаря этой способности ферменты играют важнейшую роль в обмене веществ, во взаимодействии организма с внешней средой. Таким образом, первым свойством ферментов, отличающим их от химических катализаторов, является колоссальное ускорение течения реакций.
Вторым свойством ферментов является строгая специфичность их действия. Например, мальтаза разлагает мальтозу и не действует на близкий дисахарид сахарозу. Действие ферментов направлено на совершенно определенные химические связи.
Третьим свойством ферментов является их большая зависимость (лабильность) от ряда внешних воздействий — температуры, рН среды, окислительно-восстановительных условий, примесей некоторых веществ и др.
По степени чувствительности к температуре ферменты делят на две группы: термолабильные и термостабильные. Первые переносят кратковременное нагревание до 55— 65 °С, при более высокой температуре они инактивируются. Вторые переносят нагревание до температуры ~75°С.
Примером высокоустойчивого к нагреванию внеклеточного фермента является а-амилаза.
Интересен вопрос о происхождении ферментов. По представлению некоторых ученых ферменты возникли на Земле одновременно или даже раньше, чем первичные формы жизни. По-видимому, предшественниками их являлись неорганические катализаторы или органические соединения с низким молекулярным весом. Однако они обладали малой специфичностью и слабым каталитическим действием и по существу еще не являлись ферментами.
Соединение таких катализаторов с белками положило начало возникновению ферментов. В дальнейшем первичные ферменты подвергались естественному отбору и сохранялись только те, которые улучшали жизненные процессы организмов.
№31.Химическая природа ферментов.
Изучение механизма химической реакции, катализируемой ферментом наряду с определением промежуточных и конечных продуктов на разных стадиях реакции подразумевает точное знание геометрии третичной структуры фермента, природы функциональных групп его молекулы, обеспечивающих специфичность действия и высокую каталитическую активность на данный субстрат, а также химической природы участка (участков) молекулы фермента, который обеспечивает высокую скорость каталитической реакции. Обычно молекулы субстрата, участвующие в ферментативных реакциях, по сравнению с молекулами ферментов имеют относительно небольшие размеры. Таким образом, при образовании фермент-субстратных комплексов в непосредственное химическое взаимодействие вступают лишь ограниченные фрагменты аминокислотной последовательности полипептидной цепи — «активный центр» — уникальная комбинация остатков аминокислот в молекуле фермента, обеспечивающая непосредственное взаимодействие с молекулой субстрата и прямое участие в акте катализа[8].
