
- •Лабораторный практикум
- •1.2 Блок-схема фотоколориметра кфк-2
- •1.3 Порядок работы на фотоколориметре кфк-2
- •1.4 Блок- схема установки монохроматора ум-2
- •1.5 Порядок титрования на ум-2
- •Лабораторная работа № 1 фотометрический анализ красителей по методу собственного поглощения
- •Лабораторная работа № 2 анализ смеси красителей с непересекающимися спектрами на фотоколориметре кфк-2
- •Красителей в анализируемой смеси
- •Лабораторная работа № 3 анализ смеси красителей с пересекающимися спектрами на фотоколориметре кфк-2
- •Экстинкции анализируемых веществ
- •Лабораторная работа № 4 определение хрома дифенилкарбазидным методом
- •Лабораторная работа № 5 определение железа в виде трисульфосалицилата
- •Лабораторная работа № 6 определение меди методом дифференциальной фотометрии
- •Вопросы к отчету по теме «Фотометрический метод анализа»
- •Дополнительные вопросы
- •Лабораторная работа № 7 фотометрическое титрование солей железа с сульфосалициловой кислотой
- •Вопросы к отчету по лабораторной работе «Фотометрическое титрование на фотоколориметре кфк-2»
- •Лабораторная работа № 8 фотометрическое титрование смеси протолитов на монохроматоре ум-2
- •Вопросы к отчету по лабораторной работе
- •Лабораторная работа № 9 турбидиметрический анализ сульфат-ионов
- •Вопросы к отчету по лабораторной работе «Турбидиметрический анализ сульфат-ионов»
- •3 Абсорбционная спектроскопия
- •3.2 Использование спектров поглощения для определения константы диссоциации кислотно-основных индикаторов
- •При различном положении равновесия
- •3.3 Блок-схема однолучевого спектрального прибора
- •3.4 Порядок работы на однолучевом спектрофотометре ум-2
- •Блок-схема двухлучевого спектрофотометре сф-10
- •3.6 Порядок работы на спектрофотометре сф-10
- •Лабораторная работа № 10 запись спектров поглощения на однолучевом спектрофотометре
- •Анализ смеси невзаимодействующих красителей с пересекающимися спектрами на однолучевом спектрофотометре ум-2
- •Лабораторная работа № 12 анализ смеси невзаимодействующих красителей с пересекающимися спектрами на двухлучевом спектрофотометре сф-10
- •Вопросы к отчету по работе
- •Лабораторная работа № 13
- •Определение константы диссоциации
- •Кислотно-основных индикаторов
- •Спектрофотометрическим методом
- •Вопросы к отчету по работе
- •4 Инфракрасная спектроскопия
- •4.1 Теоретические основы
- •Связь с-н в метане
- •И деформационных колебаний
- •5,6-Эпокси-цис-циклооктена
- •4.2 Расшифровка инфракрасных спектров
- •4.3 Блок-схема спектрометра мом-2000
- •4.4 Порядок включения и записи спектров на спектрометре мом-2000
- •Лабораторная работа № 14 идентификация органических соединений методом инфракрасной спектроскопии
- •Вопросы к отчету по работе
- •5 Пламенная фотометрия
- •5.1 Теоретические основы
- •5.2. Схема пламенного фотометра
- •5.3 Порядок работы на пламенном фотометре
- •Лабораторная работа № 15 определение элементов методом пламенной фотометрии
- •Вопросы к отчету по лабораторной работе
- •Скорость химической реакции зависит от следующих факторов:
- •В кинетических методах анализа используются различные методы определения концентрации. Среди них выделяют три основные группы методов:
- •По методу тангенсов:
- •Лабораторная работа № 16
- •По методу тангенсов
- •Анализируемого вещества
- •Вопросы к отчету по лабораторной работе
- •Библиографический список
- •Оглавление
- •Учебное издание
В кинетических методах анализа используются различные методы определения концентрации. Среди них выделяют три основные группы методов:
метод тангенсов,
метод фиксированного времени,
метод фиксированной концентрации.
Метод тангенсов
Метод тангенсов применяется для различных типов реакций. Он состоит из нескольких этапов:
Через определённые промежутки времени измеряют концентрацию одного из образующихся веществ х.
Строят графики зависимости концентрации х от времени. При этом необходимо иметь не менее трёх стандартных растворов, рисунок 6.1, а, б.
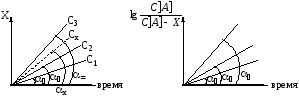
а) б)
Рисунок 6.1 – Кинетические кривые для определения концентрации
По методу тангенсов:
а – графики для дифференциальных методов;
б – графики для интегральных методов
Вместо концентрации образующегося вещества на оси ординат можно откладывать любую пропорциональную ей величину (например, оптическую плотность).
Определяют (tg α) тангенсы углов наклона соответствующих прямых и строят градуировочные графики tg α – С (рисунок 6.2).
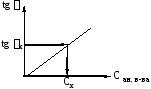
Рисунок 6.2 – Градуировочный график для определения концентрации
по методу тангенсов
4) Используя градуировочный график, определяют концентрацию анализируемого вещества в пробе.
Достоинством метода тангенсов является его высокая точность.
Метод фиксированного времени
Этот метод заключается в том, что реакцию проводят в строго определённый промежуток времени и по окончании этого времени определяют концентрацию одного из реагирующих веществ. На практике измеряют какую-либо физическую величину в какой-то определённый момент времени (рисунок 6.3).
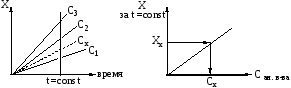
Рисунок 6.3 – Кинетические кривые для определения концентрации
по методу фиксированного времени
Вместо концентрации можно измерять любое свойство, связанное линейной зависимостью с концентрацией.
Этот метод более прост в выполнении по сравнению с методом тангенсов, но менее точен.
Метод фиксированной концентрации
В этом методе измеряют время необходимое для того, чтобы концентрация одного из реагирующих веществ достигла заданного значения. Между величиной, обратной этому времени и концентрацией анализируемого вещества существует прямолинейная зависимость (рисунок. 6.4).
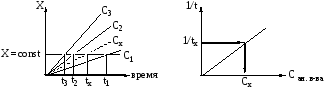
Рисунок 6.4 - Кинетические кривые для определения концентрации
по методу фиксированной концентрации
По сравнению с методом тангенсов он более простой, но менее точен. В случае если ни один из этих методов не даёт хорошей воспроизводимости, используют метод добавок.
Сущность метода: скорость реакции определяют дважды: в анализируемом растворе и в том же растворе, но с добавкой известного количества вещества. Используют чаще графический метод определения концентрации (рисунок 6.5).
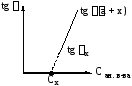
Рисунок 6.5 - Графический метод определения концентрации
по методу добавок
Кинетические реакции можно применять для фиксирования точки эквивалентности, при этом точность титриметрических методов увеличивается. Это титрование называется каталиметрическое.
При каталиметрическом титровании раствор катализатора титруют раствором ингибитора или наоборот. В первом случае скорость уменьшается, во втором – увеличивается. По изменению скорости в зависимости от объёма титранта строят графики и определяют точку эквивалентности (рисунок 6.6).
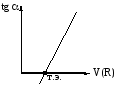
Рисунок 6.6 – Кривая каталиметрического титрования
Каталиметрическое титрования применяется для титрования разбавленных растворов (Сmin=10-6 моль/дм3).
Кинетические методы анализа обладают рядом достоинств: высокая чувствительность (Сmin=10-6 ÷10-7 моль/дм3), что позволяет определять микро-примеси; широкая область применения (возможен анализ более 40 элементов таблицы Менделеева); достаточная селективность. К недостаткам следует отнести высокую погрешность кинетических методов анализа (± 10 %).
