
- •Основы термодинамики
- •Глава 1. Основные понятия.
- •Глава 2. Температура. I закон термодинамики.
- •Neкипение 1 27,102 -246,048
- •Если в наличии конечное изменение состояния, то имеем конечный процесс 1→2
- •Для газов величину γ можно определить, измеряя скорость звука в газе :
- •Глава 3. Термохимия.
- •Для облегчения расчетов следует поступать так
- •Глава 4. Второй закон.
- •Легко сообразить, чтобы дать ответ на поставленный вопрос, необходимо взять
- •Глава 5. Процессы в неизолированных системах.
- •Глава 6. Равновесие в однокомпонентных гетерогенных системах. Уравнение Клапейрона – Клаузиуса
- •Глава 7. Термодинамические свойства многокомпонентных систем. Растворы. Химический потенциал.
- •Полный дифференциал внутренней энергии открытой системы можем записать
- •Глава 8. Термодинамика смесей идеальных газов.
- •Глава 9. Смеси жидкостей.
- •Глава 10. Реальные растворы.
- •Как было отмечено ранее, выражение
- •Заметим, что производная от экстенсивной функции по числу молей I–ого компонента является парциальной мольной величиной только в случае постоянства вышеуказанных независимых переменных:
- •Глава 11. Коллигативные свойства растворов.
- •После логарифмирования и дифференцирования имеем
- •Глава 12. Растворы электролитов – термодинамика.
- •Глава 13. Гетерогенное равновесие многокомпонентных систем без химических реакций.
- •Глава 14. Термодинамические свойства реального газа. Летучесть.
- •Если газ реальный и работа его изотермического изменения объема
- •Как мы узнаем ниже, разность е(р) – е(1) умноженная на 2f ( f – число Фарадея, равное 96487 кулонов/г-экв ) как раз равна работе расширения водорода при 25 0с от давления р до 1 атм
- •Глава 15. Термодинамика системы с химической реакцией.
- •Задача легко решается для идеально-газовой смеси, поскольку для нее
- •Глава 16. Тепловая теорема Нернста
- •Проблема возникает при интегрировании уравнения
- •Так как
- •По соотношению Максвелла
- •Глава 17. Элементы термодинамики неравновесных систем.
- •Глава 18. Неравновесные явления в растворах электролитов.
- •Это уравнение Нернста – Эйнштейна связывает коэффициент диффузии иона с его электрической подвижностью.
- •Глава 19. Равновесные электрохимические системы
- •Глава 20. Неравновесные электрохимические системы, основы электрохимической кинетики.
После логарифмирования и дифференцирования имеем
![]()
Но ![]() , поэтому
, поэтому
![]()
а по уравнению Клапейрона – Клаузиуса
![]()
и ![]()
Интегрируем в пределах от х1 = 1 до xi и TV1 до T и, полагая ΔV H1 не зависящей от температуры, имеем
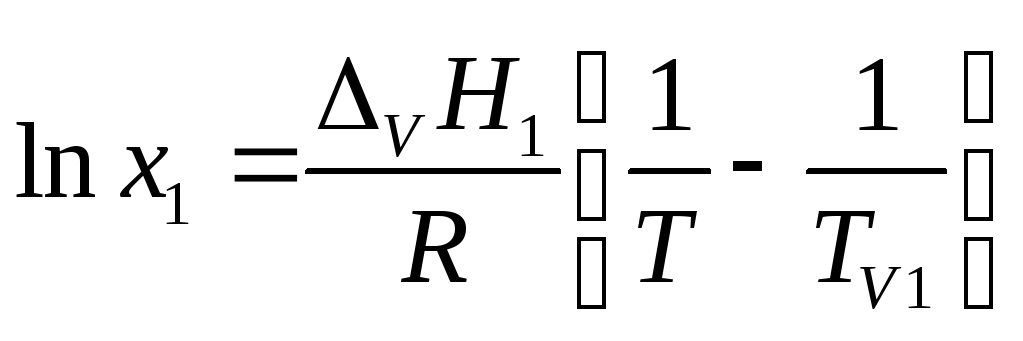 или
или
![]()
Обозначим Т
– ТV1
= ΔT
– это повышение температуры кипения
и, положив приближенно ![]() получим
получим
![]() а
поскольку
а
поскольку![]()
имеем ![]()
где Е – эбулиокопическая константа растворителя.
Аналогично криоскопии эбулиоскопия позволяет определять мольную массу вещества, но нужно иметь в виду, что эбулиоскопические константы меньше криоскопических.
11.4. Термодинамика осмотического давления.
Если растворитель и раствор разделены полупроницаемой (т.е. проницаемой только для молекул растворителя) мембраной, то в силу различия химических потенциалов растворителя в растворе и чистого растворителя через мембрану будет наблюдаться массоперенос (диффузия) растворителя в раствор. Для того, чтобы прекратить массоперенос к раствору нужно приложить некоторое добавочное давление П, которое и называется осмотическим давлением.
Вант – Гофф (1885) впервые предложил для осмотического давления количественную зависимость
![]()
где с2 – концентрация растворенного вещества моль/л ( с2 = п2/V, n2 – число молей растворенного вещества, V- объем раствора), т.е. осмотическое давление в разбавленных растворах численно равно тому давлению, которое производило бы то же число молекул растворенного вещества, если бы оно в виде идеального газа занимало бы при данной температуре объем, равный объему раствора. ( Кстати, первая Нобелевская премия по химии в 1901 году была присуждена Якобу Хенрику Вант-Гоффу за открытие законов химической динамики и осмотического давления в растворах). Но аналогия между уравнением Вант-Гоффа и уравнением состояния идеального газа случайна и не имеет существенного значения. Осмотическое давление является тем добавочным давлением, которое увеличивает химический потенциал растворителя в растворе и этим компенсирует уменьшение химического потенциала растворителя, вызванное растворением второго компонента. Такая компенсация создает возможность равновесия раствора с чистым растворителем в особых условиях наличия полупроницаемой перегородки. В отсутствие последней осмотическое давление отсутствует. Итак, условие равновесия μ1= μ01 и dμ1 = dμ01, где μ01 – химический потенциал чистого растворителяпри постоянной температуре и внешнем давлении р1, в растворе же его значение μ1 изменяется с изменением х1 и давления р2, которое складывается из внешнего и осмотического р2 = р1 + π. Ищем, как меняется осмотическое давление с изменеием концентрации х1 при р1 и Т = Const. В этих условиях
![]() ,
следовательно
и
,
следовательно
и
![]() .
Имеем
.
Имеем


В
предположении, что
![]() интегрируем от
интегрируем от
![]()
до
концентрации ![]()
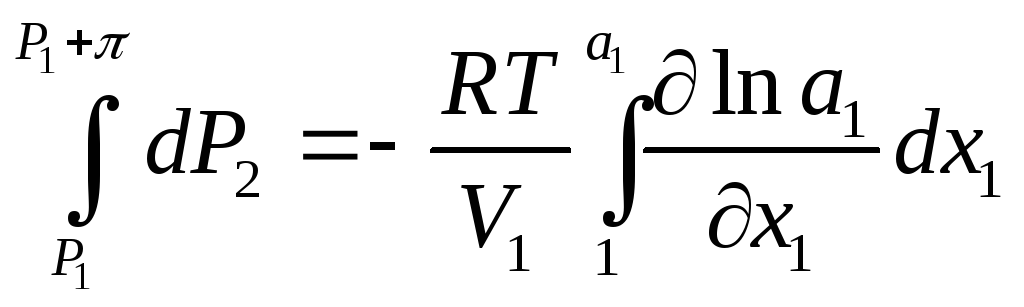 отсюда
отсюда ![]() а поскольку
а поскольку
![]() то
общее уравнение осмотического давления
то
общее уравнение осмотического давления
![]()
Если
раствор подчиняется закону Рауля, т.е.
достаточно разбавлен, то Р/Р01=1–
х2,
и ![]() если п2
<< n1
, в этом случае
если п2
<< n1
, в этом случае
![]() где
V
объем
раствора, и окончательно имеем уравнение
Вант-Гоффа
где
V
объем
раствора, и окончательно имеем уравнение
Вант-Гоффа ![]()
Осмотическое давление 1 молярного раствора равно примерно 25 атм. Осмотические эффекты чрезвычайно важны в биологических системах, поскольку большинство биологических мембран – стенки кишечника, стенки клеток – полупроницаемы.Слишком большой градиент концентрации приводит к разрыву или высушиванию клетки. Очень эффективным осмотическим устройством является человеческая почка, где кровь и моча движутся навстречу друг другу с противоположных сторон ряда полупроницаемых мембран, которые позволяют большинству ионов и низкомолекулярных продуктов обмена веществ перейти из крови в мочу и далее активно перекачивают (используя биохимические процессы) некоторые ионы (нужные Na+ и Cl - ) обратно в кровь.
Измерение осмотического давления растворов высокополимеров очень удобно для измерения их средней мольной массы, поскольку из уравнения Вант-Гоффа следует, что
![]()
где М2 – мольная масса полимера, g2 – его навеска, V – объем растворителя. Например, раствор 1,372 г полимера в 100 мл воды имеет осмотическое давление 10 мм водяного столба, тогда (Т = 300 К) :
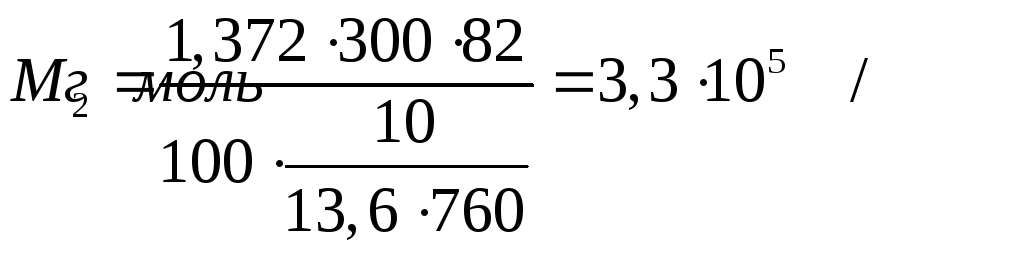
11.5. Коллигативные свойства растворов.
Подведем общий итог для некоторых свойств растворов.
Закон Рауля можно представить в виде
![]()
понижение температуры замерзания раствора
![]()
повышение температуры кипения раствора нелетучего вещества
![]()
осмотическое давление (уравнение Вант-Гоффа)
![]()
Мы видим, что эти свойства целиком определяются (для разбавленных растворов) свойствами растворителя и линейно зависят только от количества молей растворенного вещества, но не от его природы. Такие свойства, линейно зависящие от моляльности, называются коллигативными.
Коллигативные свойства позволяют получить весьма значительную информацию о частицах, присутствующих в растворах, и о природе сил, действующих в жидком состоянии вещества. Достаточно указать, что кажущееся увеличение моляльности в водных электропроводящих растворах привело Аррениуса к теории электролитической диссоциации.
Но не только вода может быть растворителем, но и серная кислота, Эксперименты показали, что при растворении N2O4 в чистой H2SO4 соответствует присутствию шести молей частиц на моль растворенной N2O4 . Можно предположить, что протекает реакция :
![]()
где все ионные частицы сольвaтированы серной кислотой. Аналогичные взаимодействия наблюдаются и для других систем, в том числе и для воды.
