
2015-СК-біохімія-07-Ензими-ІКТ---
.pdf
Національний університет біоресурсів і природокористування України
Змістовий модуль 3. Водно-мінеральний обмін. Вітаміни. Ензими.
Лекція №3 Ензими
Лектори :
Мельничук Д.О., д.б.н., професор, академік НАН України і НААН Мельничук С.Д., д.б.н., професор, член кореспондент НААН
Калачнюк Л.Г., д.б.н., професор,
Калачнюк Г.І., д.б.н., професор К. 409, 419, 421, 4-й поверх,
1
Корпус № 12 НУБіП України
Просторова структура тріозфосфат-ізомерази
Змістовий модуль 3. Водно-
мінеральний обмін. Вітаміни. Ензими.
Лекція №3 Ензими
План
1.Ензими, загальні відомості
2.Кофактори. Коензими
3.Механізм участі ензимів у біологічних реакціях (на прикладі односубстратної реакції)
4.Номенклатура та класифікація ензимів
5.Кінетичні властивості ензимів за впливу різних фізико-хімічних факторів
2
1. Ензими, загальні відомості
Живий організм вирує з метаболічною активністю.
Тисячі хімічних реакцій відбуваються дуже швидко в будь-якому заданому місці в усіх живих клітинах.
Всі такі перетворення здійснюються за допомогою ензимів – біокаталізаторів метаболічних реакцій, які за природою є
протеїнами (або РНК; ензими РНКової природи називають рибозимами).
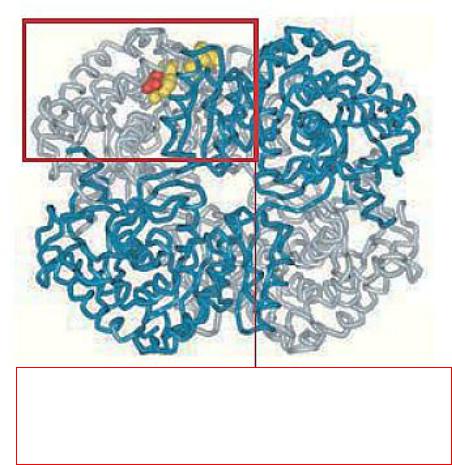
Просторова модель лактатдегідрогенази (ЛДГ) – тетрамеру (144 кДа). Червоним кольором – субстрат лактат. Жовтим кольором – коензим НАД+.
Детальніше про активний сайт ЛДГ, субстрат (лактат) і коензим НАД+
далі в слайді 16. |
3 |

І |
і |
У 1877 німецький фізіолог Вільгельм Кюне (1837– |
||
н |
1900) вперше використав термін ензим, що з грецької |
|||
с |
ενζυμον, “у заквасці", для опису ферментативного |
|||
|
||||
ф |
процесу. |
|||
т |
||||
У 1897, Едуард Бюхнер у своїй першій статті про |
||||
о |
о |
здатність дріжджових екстрактів зброджувати цукор. |
||
р |
р |
|
|
|
|
|
Він назвав ензим, який зброджує сахарозу “зимазою". |
||
|
м |
|
У 1907, Едуард Бюхнер отримав Нобелівську премію з |
|
и |
хімії “за біохімічні дослідження і відкриття вільної від |
|||
а |
||||
клітини ферментації". |
||||
ч |
|
У 19 ст., коли вивчалась ферментація цукру до спирту |
||
н |
ц |
|||
і |
за допомогою дріжджів, Луїс Пастер прийшов до |
|||
висновку, що така ферментація каталізується “живими |
||||
а |
я |
силами” дріжджових клітин, які назвав “ферментами", |
||
|
|
що були властиві (як думали) тільки живим організмам. |
||
|
|
|||
4

І |
і |
|
н |
||
с |
||
т |
ф |
|
о |
о |
|
р |
р |
|
и |
м |
|
а |
||
ч |
ц |
|
н |
і |
|
а |
я |
|
|
|
У 1926, Джеймс Самнер показав, що ензим уреаза є чистим протеїном, та
кристалізував його.
Висновок, що чисті протеїни можуть бути ензимами, був підтверджений Нортропом і Стенлі, які працювали з травними ензимами пепсином
(1930), |
трипсином |
і |
хімотрипсином.
Самнер також кристалізував ензим каталазу у 1937.
Самнер, Нортроп і Стенлі були нагороджені в 1946 Нобелівською премією з хімії.
Стрічкова молекулярна модель уреази – ензиму бактерії H. pylori.
5

Ензими РНК-природи називаються рибозимами і вважаються первісною формою ферментів, які були замінені білковими ферментами в процесі еволюції.
Терміни «ензим» і «фермент» можна використовувати як синоніми, але згідно останніх вимог журналів щодо наукових публікацій вживається «ензим».
Але наука про ферменти називається ензимологією, а не ферментологією (ймовірно щоб не змішувати корені слів латинської і грецької мов).
6

Більшість всіх процесів у біологічній клітині потребують ензимів для їх проходження з підвищеною швидкістю.
Оскільки
ензими
вибірково
каталізують
реакції з певними субстратами, то
підвищується
тільки кілька реакцій серед інших можливих, а такий набір ензимів
визначає
метаболічний шлях у клітині.
7

Ензими в більшості випадків є глобулярними протеїнами розміром від 62 амінокислотних залишків для мономеру 4-оксалокротонат таутомерази до понад 2500 залишків у синтази жирних кислот у тварин.
Ензим білкової природи
коензим (кофермент)
апофермент
Простий ензим або Простий фермент
Холофермент (складний ензим)↔
апофермент (протеїн) + коензим
8
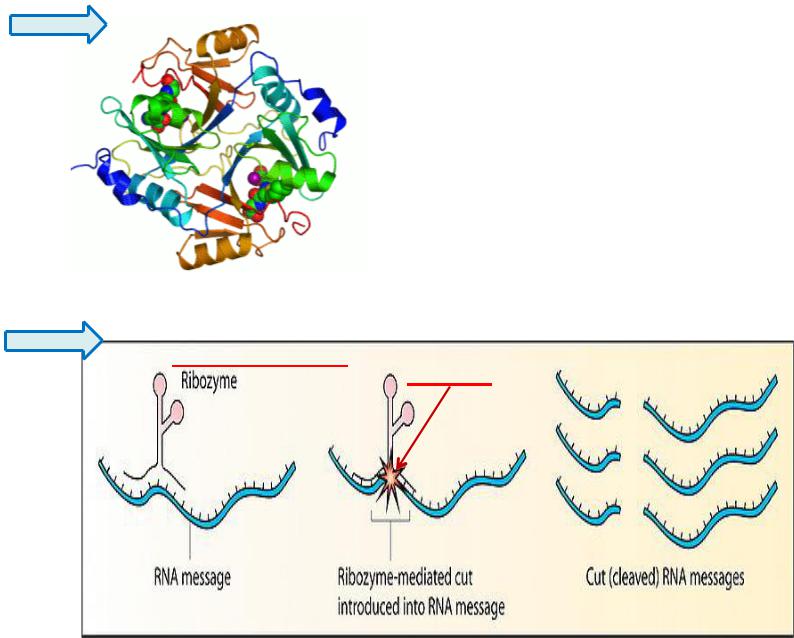
Ензим протеїнової природи
Гліоксилаза І людини. Два іони цинку
(кофактори), які необхідні ензиму для каталізу реакції, представлені у вигляді бузкових кульок, а інгібітор ензиму - S- гексилглутатіон показаний як
“заповнювач” двох активних сайтів.
Ензим РНКової природи – рибозим.
Рибозим (РНК)
розрив
мРНК |
«розрізані» мРНК |
9

В ензимних реакціях, молекули, що вступають в перетворення, називають субстратами, які згодом перетворюються в інші молекули, котрі називають продуктами.
ензим
продукти
субстрати
Схема
ензимної реакції |
10 |
|
