
Термодинамика
.docxМГТУ им. Н. Э. Баумана
Домашнее задание №1
по термодинамике:
«Газовые смеси»
Вариант №15
Студент: Романов А.С.
Группа: Э7-52
Преподаватель: Чирков А.Ю.
-2012-
Условие задания:
Сосуд разделен адиабатной перегородкой на четыре части, в каждой из которых содержатся различные газы. После того как перегородка убрана, происходит «смешение в объеме» без теплообмена с окружающей средой. Состояния газов до смешения характеризуются следующими параметрами: массой mi0, кг; объемом Vi0, м3; температурой ti0, ˚С.
Необходимо определить:
-
температуру смеси после завершения процесса смешения t;
-
давление смеси Р, МПа;
-
газовую постоянную R, Дж/(кг*К);
-
среднюю молярную массу смеси µ, кг/моль;
-
объемный состав смеси {ri};
-
молярный состав смеси {ni};
-
парциальное давление компонентов смеси {pi}, МПа;
-
приведенные объемы компонентов смеси {Vi}, МПа;
-
истинную молярную теплоемкость смеси при р=const для температуры смеси, которая устанавливается после окончания процессов смешения ср ,Дж/(кмоль*К);
-
истинную объемную теплоемкость смеси при р=const после окончания процесса смешения C , Дж/(м *К);
-
истинную массовую теплоемкость смеси при р=const после окончания процесса смешения с, Дж/(кг*К);
-
количество теплоты Q (Дж), которое необходимо отвести от 3 кмоль смеси для охлаждения их при р=const до температуры смеси 300 К;
-
количество теплоты Q (Дж), которое необходимо отвести от 4 м смеси для охлаждения их при р=const до температуры смеси 300 К;
-
количество теплоты Q (Дж), которое необходимо отвести от 5 кг смеси для охлаждения их при р=const до температуры смеси 300 К.
Исходные данные:
|
Газ |
mi0, кг |
Vi0, м3 |
ti0, ˚С |
|
O2 |
13 |
2,1 |
160 |
|
N2 |
16 |
1,6 |
260 |
|
H2 |
11 |
3,1 |
860 |
|
CO |
6 |
3,6 |
1060 |
Молярные массы газов:
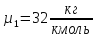 ;
;
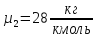 ;
;
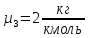 ;
;
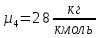
Решение:
При получении значений из таблицы используется линейная интерполяция:
 (1.1)
(1.1)
-
Температура смеси после завершения процесса смешения.
Нулевое приближение:
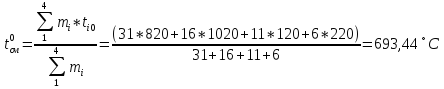
Первое приближение:
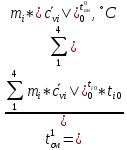 (1.2)
(1.2)
Вычислим теплоемкости, входящие формулу (1.2), необходимые для расчета суммарной внутренней энергии газов до смешения, а также температуры смеси в первом приближении:
O2:
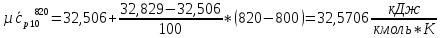
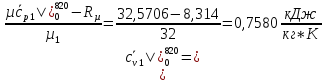
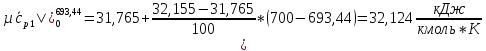
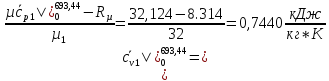
СО2:
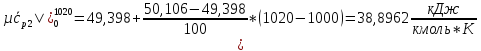
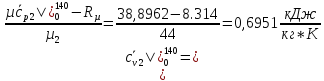
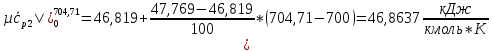
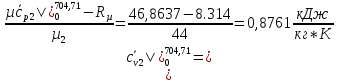
SO2:
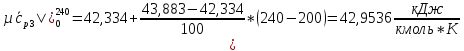
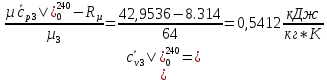

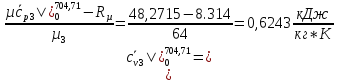
H2O:
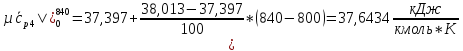
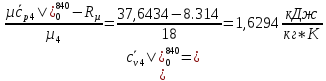
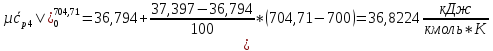
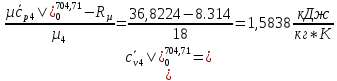
Подставим полученные значения:
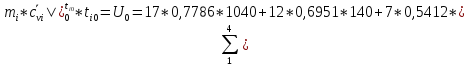
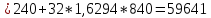 кДж – суммарная
внутренняя энергия газов до смешения
(остаётся постоянной для всех последующих
приближений).
кДж – суммарная
внутренняя энергия газов до смешения
(остаётся постоянной для всех последующих
приближений).
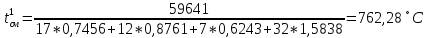
Второе приближение:
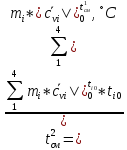 (1.3)
(1.3)
Вычислим теплоемкости, входящие формулу (1.3):
O2:
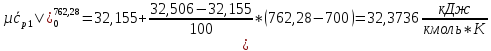
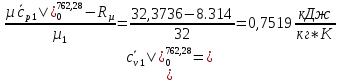
СО2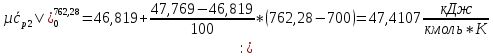
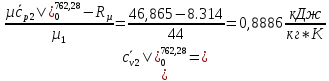
SO2:
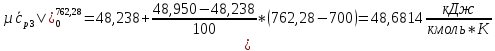
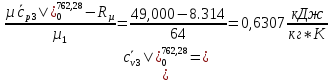
H2O:
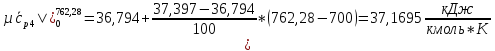

Подставим полученные значения:
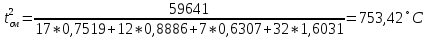
Третье приближение:
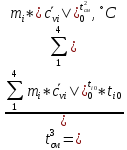 (1.3)
(1.3)
Вычислим теплоемкости, входящие формулу (1.3):
O2:
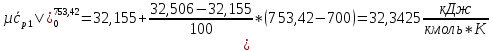
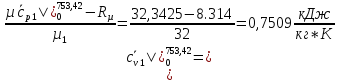
СО2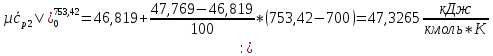
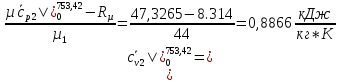
SO2:
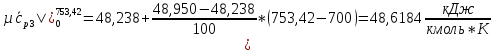
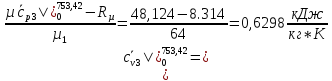
H2O:
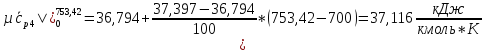
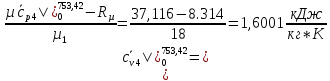
Подставим полученные значения:
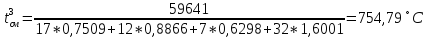
Принимаем:
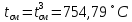
-
Давление смеси
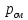 ,
МПа.
,
МПа.
Для определения давления используем формулу:
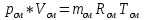
где
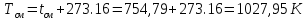
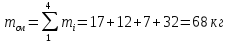 - масса смеси;
- масса смеси;
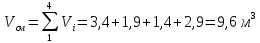 - объем смеси;
- объем смеси;
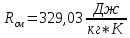 - газовая постоянная
смеси (см. пункт 3).
- газовая постоянная
смеси (см. пункт 3).
Тогда:
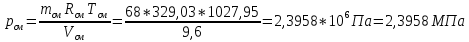
-
Постоянная газовая смеси
 .
.
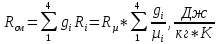
где
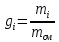 - массовая доля i-го
газа.
- массовая доля i-го
газа.
Тогда:
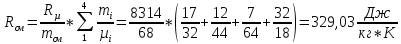 ,
,
-
Средняя молярная масса смеси -
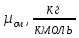 .
.
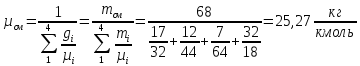
-
Состав смеси в объемных долях -

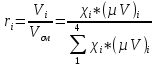
При одинаковых
температуре и давлении
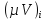 всех газов одинаково, поэтому:
всех газов одинаково, поэтому:
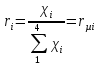 (см. пункт 6)
(см. пункт 6)
O2:
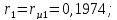
СО2:
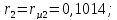
SO2:
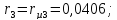
H2O:
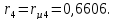
-
Состав смеси в молярных долях -
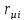 .
.
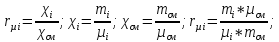
O2:
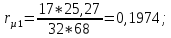
СО2:

SO2:
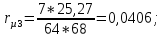
H2O:

Проверка:
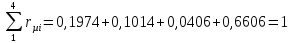 ,
верно.
,
верно.
-
Парциальные давления компонентов смеси -
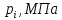 .
.
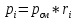
O2:
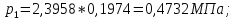
СО2:
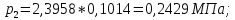
SO2:

H2O:
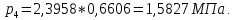
-
Парциальные объемы компонентов смеси -
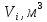 .
.
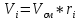
O2:
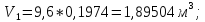
СО2:
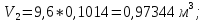
SO2:
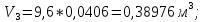
H2O:
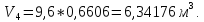
-
Истинная молярная теплоемкость смеси при
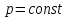 ,
установившеюся после смешения
,
установившеюся после смешения
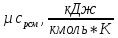 .
.
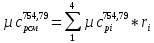
O2:
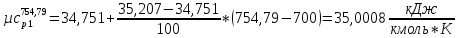
СО2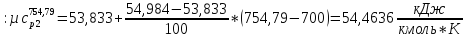
SO2:
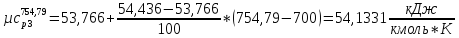
H2O:
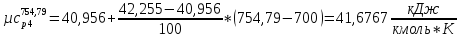
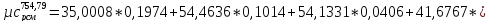
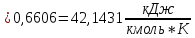
-
Истинная объемная теплоемкость смеси при
 ,
установившеюся после смешения
,
установившеюся после смешения
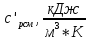 .
.
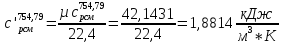 .
.
-
Истинная массовая теплоемкость смеси при
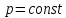 ,
установившеюся после смешения
,
установившеюся после смешения
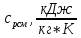 .
.
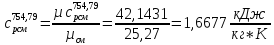 .
.
-
Количество теплоты, которое необходимо отвести от 3 кмоль смеси для ее охлаждения при
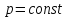 от температуры смеси до температуры
от температуры смеси до температуры
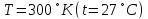 .
.
Определим среднюю молярную теплоемкость смеси при процессе:
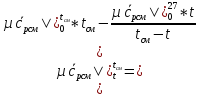
O2:
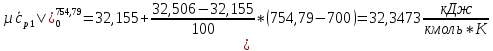
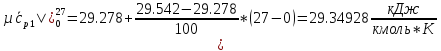
СО2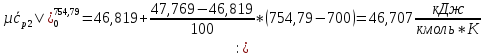
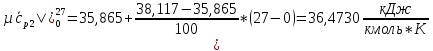
SO2:
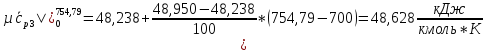
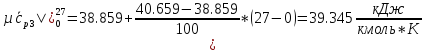
H2O:
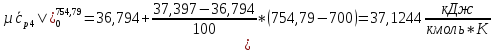
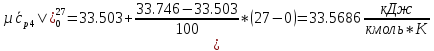
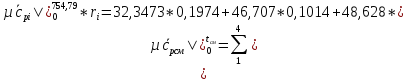
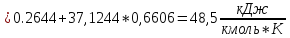
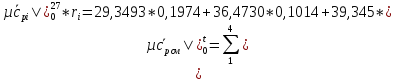
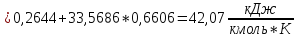
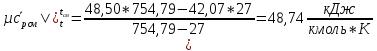
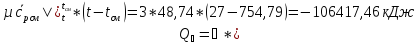 .
.
-
Кол-во теплоты, которое необходимо отвести от 4 м3 (н. у.) смеси для ее охлаждения при
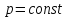 от температуры смеси до температуры
от температуры смеси до температуры
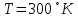
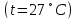 .
.
Определим среднюю объемную теплоемкость смеси при процессе:
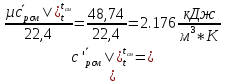 .
.
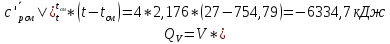 .
.
-
Кол-во теплоты, которое необходимо отвести от 5кг смеси для ее охлаждения при
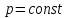 от температуры смеси до температуры
от температуры смеси до температуры
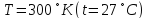 .
.
Определим среднюю массовую теплоемкость смеси при процессе:
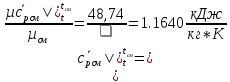
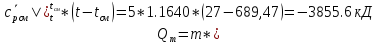
Знак минус указывает на то, что теплота отводится от смеси.
