
- •1 Требования к сырью и восстановителю при производстве губчатого железа
- •80 Железорудное сырье для процессов металлургии железа.
- •81. Топливо и восстановитель для металлургии железа
- •2 Комплексное использование сырья в аглодоменном производстве
- •3 Реакция «водяного газа»
- •4 Поведение попутных элементов при окусковании железорудного сырья
- •5 Теплообмен в шахтных печах. Структура теплового баланса доменной плавки.
2 Комплексное использование сырья в аглодоменном производстве
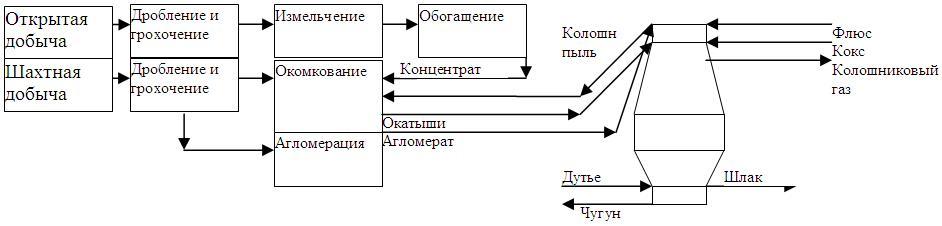
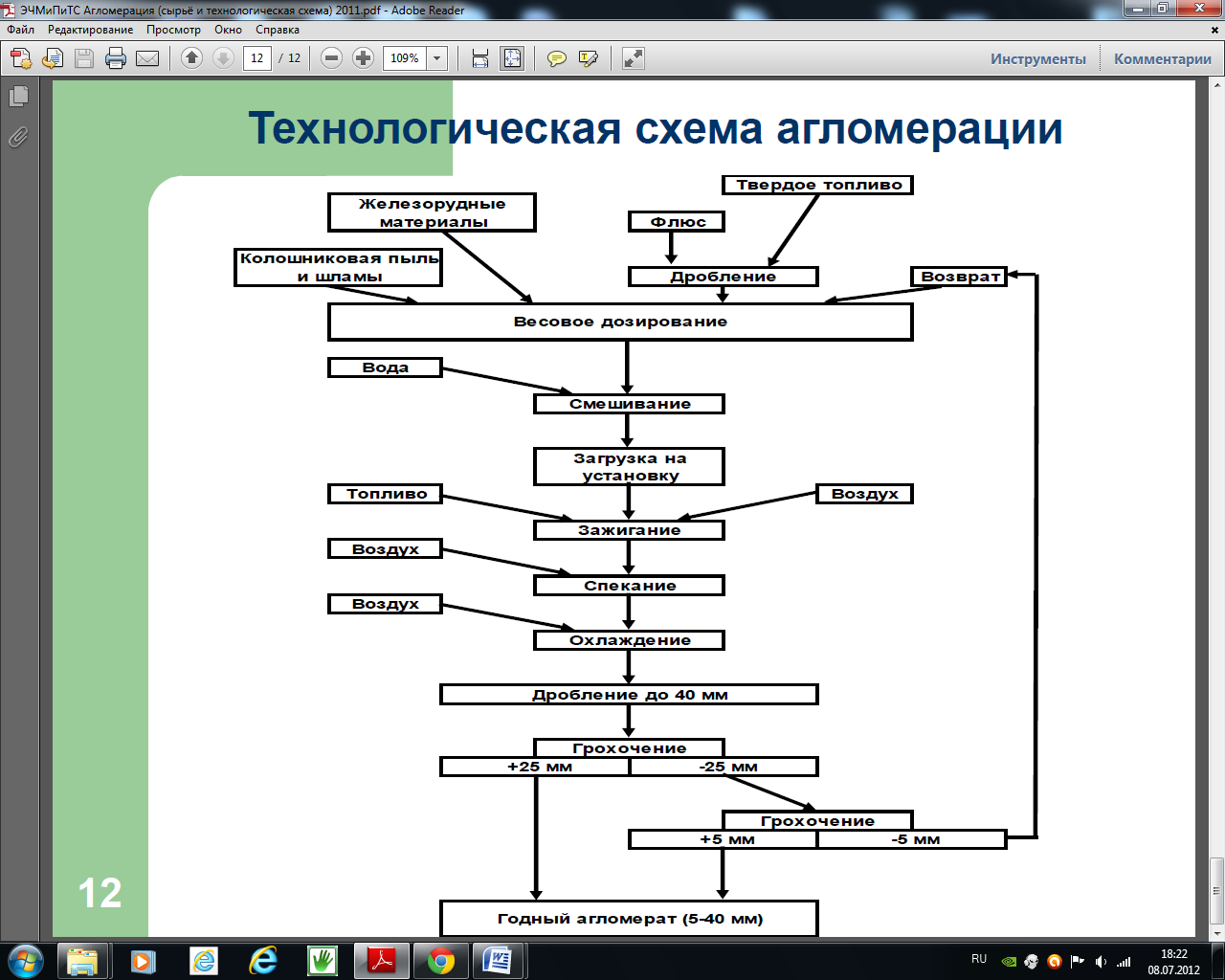
Агломерация – процесс получения кусков агломерата, методом частичного плавления мелкой руды и концентрата с топливом с последующей кристаллизацией расплава.
Состав шихты:
Железорудные материалы (40-50%):
Железная руда (крупность < 10 мм)
Железорудный концентрат (крупность < 0,07 мм)
Колошниковая пыль содержит 45% железа.
Окалина (прокатная)
Шламы (40-50% железа)
Марганцевая руда
Чугунный скрап.
Топливо 4-6%
Коксик
Антрацитовый штыб.
Флюс 15-20 %
Известняк (СаСО3)
Доломит (СаСО3 MgСО3)
Известь
Конверторный шлак
Возврат – мелкий агломерат 20-30%
До спекания проводится подготовка шихты.
Дозирование – для стабильности процесса.
Смешивание – для равномерного распределения компонентов. Производится в барабанах смесительном и окомковательном. При подаче в барабан воды, которая разбрызгивается над поверхностью шихты происходит окомкование. При оптимальной влажности 6-9% обеспечивается наибольшая газопроницаемость.
Затем производится спекание на колосниковой решетке. Сначала загружают «постель» из возврата (30-30 мм), затем шихта – 250-350 мм. Под решеткой разрежение – 7-10 кПа, чтобы воздух просасывался сквозь слой шихты. Чтобы процесс начался специальным зажигательным устройством нагревают верхний слой шихты до 1200-1300оС и топливо воспламеняется. Зона горения постепенно продвигается сверху вниз. Когда зона горения достигает постели, процесс заканчивается. Процесс идет 10-20 мин.
3 Реакция «водяного газа»
H2O + C → CO + H2
4 Поведение попутных элементов при окусковании железорудного сырья
Поведение попутных элементов при агломерации.
В ходе агломерации происходит выгорание сульфидной серы шихты. Реакция начинается при 250-280С
4FeS2+11O2=2Fe2O3+8SO2
4FeS+7O2=2Fe2O3+4SO2
Выше 1383С процесс развивается по реакциям
3FeS2+8O2=Fe3O4+6SO2
3FeS+5O2= Fe3O4+3SO2
В присутствии катализаторов (Fe2O3) до 40% SO2 окисляется до SO3. В отходящих газах установлено наличие Н2S и COS.
В зоне горения сернистые соединения захватываются из газа железистым силикатным расплавом с образованием CaS. При температурах 900-1000С известь, известняк и ферриты поглощают SO2 из газа
СаО+ SO2+1/2Н2О = СаSO30.5 Н2О
СаSO30.5 Н2О= СаSO3+0.5 Н2О
СаSO3+1/2O2= СаSO4
Таким образом, высокая основность шихты ухудшает десульфурацию.
Удалению сульфидной серы способствует повышенные расходы топлива.
Удаление мышьяка, цинка, свинца при агломерации практически не имеет места.
Однако при вводе в шихту хлорирующих добавок (СаСl2) образуются летучие хлориды. В этих условиях удается удалить до 90% Pb, 65%Zn, 60%As.
Поведение попутных элементов при получении окатышей.
В обычных условиях окислительного упрочняющего обжига удаляется только сера.
Фосфор, мышьяк, цинк из окатышей не удаляются.
При получении неофлюсованных окатышей из сернистых концентратов степень удаления серы – 95-99%. Окислительная атмосфера обеспечивает высокую степень окисления серы и переводу ее в газовую фазу в виде SO2. Однако в присутствии известняки степень десульфурации снижается. Двуокись серы поглощается окислами железа, кальция, магния, ферритами и силикатами кальция
СаО+ SO2 0,5О2= СаSO4
СаСО3+ SO2 + 0,5О2= СаSO4+СО2
СаОFe2O3+ SO2 0,5О2= СаSO4+ Fe2O3
Сульфат кальция – устойчивое соединение.
На содержание серы оказывает влияние температурный режим и особенно скорость нагрева и конечная температура обжига. Если нагрев ведется медленно, то вся сера переходит в сульфат кальция. Разложение сульфата кальция интенсифицируется с ростом температуры. Но при оплавлении окатышей десульфурация осложняется. Десульфурация ухудшается и при увеличении основности. Замена известняка доломитом снижает содержание серы, так как сульфат магния менее прочен, чем сульфат кальция.
