
Особенности характеристических спектров.
1. В отличие от оптических линейчатых спектров с их сложностью и разнообразием, рентгеновские характеристические спектры различных элементов отличаются простотой и однообразием. С ростом атомного номера Z элемента они монотонно смещаются в коротковолновую сторону.
2. Характеристические спектры разных элементов имеют сходный характер (однотипны) и не меняются, если интересующий нас элемент находится в соединении с другими. Это можно объяснить лишь тем, что характеристические спектры возникают при переходах электронов во внутренних частях атома, частях, имеющих сходное строение.
3. Характеристические спектры состоят из нескольких серий: К, L, М, ... Каждая серия — из небольшого числа линий: Ка, Кβ, Кγ, ... La, Lβ, Ly, ... и т. д. в порядке убывания длины волны λ.
Анализ характеристических спектров привел к пониманию, что атомам присуща система рентгеновских термов К, L, М, ...(рис.13.6). На этом же рисунке показана схема возникновения характеристических спектров. Возбуждение атома возникает при удалении одного из внутренних электронов (под действием электронов или фотонов достаточно большой энергии). Если вырывается один из двух электронов K-уровня (n = 1), то освободившееся место может быть занято электроном из какого-либо более высокого уровня: L, M, N, и т. д. В результате возникает K-серия. Подобным же образом возникают и другие серии: L, М, ...
С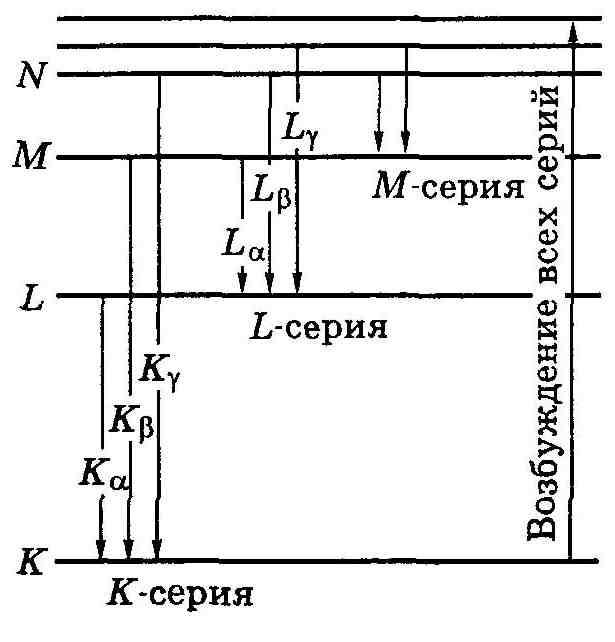 ерияК,
как
видно из рис.13.6, непременно сопровождается
появлением и остальных серий, поскольку
при испускании ее линий освобождаются
электроны на уровнях L,
М и
др., которые в свою очередь будут
заполняться электронами с более высоких
уровней.
ерияК,
как
видно из рис.13.6, непременно сопровождается
появлением и остальных серий, поскольку
при испускании ее линий освобождаются
электроны на уровнях L,
М и
др., которые в свою очередь будут
заполняться электронами с более высоких
уровней.
Молекулярные спектры. Виды связи в молекулах ,энергия молекулы, энергия колебательного и вращательного движения.
Молекулярные спектры.
Молекулярные спектры - оптические спектры испускания и поглощения, а также комбинационного рассеяния света (См. Комбинационное рассеяние света), принадлежащие свободным или слабо связанным между собой Молекулам. М. с. имеют сложную структуру. Типичные М. с. — полосатые, они наблюдаются в испускании и поглощении и в комбинационном рассеянии в виде совокупности более или менее узких полос в ультрафиолетовой, видимой и близкой инфракрасной областях, распадающихся при достаточной разрешающей силе применяемых спектральных приборов на совокупность тесно расположенных линий. Конкретная структура М. с. различна для различных молекул и, вообще говоря, усложняется с увеличением числа атомов в молекуле. Для весьма сложных молекул видимые и ультрафиолетовые спектры состоят из немногих широких сплошных полос; спектры таких молекул сходны между собой.
Из решения уравнения Шредингера для молекул водорода при указанных выше предположениях получается зависимость собственных значений энергии от расстояния R между ядрами, т. е. Е = E(R).
Энергия молекулы
|
Е ≈ Еэл + Екол + Евращ, |
(13.45) |
где Еэл — энергия движения электронов относительно ядер; Екол — энергия колебаний ядер (в результате которых периодически изменяется относительное положение ядер); Евращ — энергия вращения ядер (в результате которых периодически изменяется ориентация молекулы в пространстве).
В формуле (13.45) не учтены энергия поступательного движения центра масс молекул и энергия ядер атомов в молекуле. Первая из них не квантуется, поэтому ее изменения не могут привести к возникновению молекулярного спектра, а вторую можно не учитывать, если не рассматривать сверхтонкую структуру спектральных линий.
Доказано, что Еэл >> Екол >> Евращ, при этом Еэл ≈ 1 – 10 эВ. Каждая из входящих в выражение (13.45) энергий квантуется и им соответствует набор дискретных уровней энергии. При переходе из одного энергетического состояния в другое поглощается или испускается энергия ΔЕ = hν. Из теории и эксперимента следует, что расстояние между вращательными уровнями энергии Δ Евращ гораздо меньше расстояния между колебательными уровнями Δ Екол, которое, в свою очередь, меньше расстояния между электронными уровнями Δ Еэл.
Строение молекул и свойства их энергетических уровней проявляются в молекулярных спектрах - спектрах излучения (поглощения), возникающих при квантовых переходах между уровнями энергии молекул. Спектр излучения молекулы определяется структурой ее энергетических уровней и соответствующими правилами отбора (например, изменение квантовых чисел, соответствующих как колебательному, так и вращательному движению, должно быть равно ± 1). При разных типах переходов между уровнями возникают различные типы молекулярных спектров. Частоты спектральных линий, испускаемых молекулами, могут соответствовать переходам с одного электронною уровня на другой (электронные спектры) или с одного колебательного (вращательного) уровня на другой [колебательные (вращательные) спектры].
Кроме того, возможны и переходы с одними значениями Екол и Евращ на уровни, имеющие другие значения всех трех компонентов, в результате чего возникают электронно-колебательные и колебательно-вращательные спектры. Поэтому спектр молекул довольно сложный.
Типичные молекулярные спектры - полосатые, представляют собой совокупность более или менее узких полос в ультрафиолетовой, видимой и инфракрасной областях. Применяя спектральные приборы высокой разрешающей способности, можно видеть, что полосы представляют собой настолько тесно расположенные линии, что они с трудом разрешаются.
Структура молекулярных спектров различна для разных молекул и с увеличением числа атомов в молекуле усложняется (наблюдаются лишь сплошные широкие полосы). Колебательными и вращательными спектрами обладают только многоатомные молекулы, а двухатомные их не имеют. Это объясняется тем, что двухатомные молекулы не имеют дипольных моментов (при колебательных и вращательных переходах отсутствует изменение дипольного момента, что является необходимым условием отличия от нуля вероятности перехода).
Молекулярные спектры применяются для исследования строения и свойств молекул, используются в молекулярном спектральном анализе, лазерной спектроскопии, квантовой электронике и т.д.
ВИДЫ СВЯЗЕЙ В МОЛЕКУЛАХ Химическая связь — явление взаимодействия атомов, обусловленное перекрыванием электронных облаков связывающихся частиц, которое сопровождается уменьшениемполной энергии системы. Ионная связь — прочная химическая связь, образующаяся между атомами с большой разностью электроотрицательностей, при которой общаяэлектронная пара полностью переходит к атому с большей электроотрицательностью.Это притяжение ионов как разноименно заряженных тел. Электроотрицательность (χ) — фундаментальное химическое свойство атома, количественная характеристика способности атома в молекуле смещать к себе общие электронные пары. Ковалентная связь (атомная связь, гомеополярная связь) — химическая связь, образованная перекрытием (обобществлением) пары валентных электронных облаков. Обеспечивающие связь электронные облака (электроны) называются общей электронной парой. Водородная связь — связь между электроотрицательным атомом и атомом водорода H, связанным ковалентно с другим электроотрицательным атомом. Металлическая связь — химическая связь, обусловленная наличием относительно свободных электронов. Характерна как для чистых металлов, так и их сплавов иинтерметаллических соединений.
Комбинационное рассеивание света.
это рассеяние света веществом, сопровождающееся заметным изменением частоты рассеиваемого света. Если источник испускает линейчатый спектр, то при К. р. с. в спектре рассеянного света обнаруживаются дополнительные линии, число и расположение которых тесно связаны с молекулярным строением вещества. При К. р. с. преобразование первичного светового потока сопровождается обычно переходом рассеивающих молекул на другие колебательные и вращательные уровни, причём частоты новых линий в спектре рассеяния являются комбинациями частоты падающего света и частот колебательных и вращательных переходов рассеивающих молекул — отсюда и назв. «К. р. с.».
Для наблюдения спектров К. р. с. необходимо сконцентрировать интенсивный пучок света на изучаемом объекте. В качестве источника возбуждающего света чаще всего применяют ртутную лампу, а с 60-х гг. — лазерный луч. Рассеянный свет фокусируется и попадает в спектрограф, где спектр К. р. с. регистрируется фотографическим или фотоэлектрическим методами.
