
Э_Г_Бабенко конструкционные материалы
.pdf3.1.2. Компоненты, фазы, линии и точки диаграммы Fe–Fe3C
Компоненты сплавов. Основными компонентами железоуглеродистых сплавов являются железо и углерод.
Ж е л е з о (лат. Ferrum) открыто в III тысячелетии до н. э., это химический элемент VIII группы Периодической системы Менделеева, атомный номер 26, атомный радиус 0,127 нм, атомная масса 55,8; плотность 7,83 г/см3. Блестящий серебристо-белый металл с температурой плавления 1539 °С. Широко распространено в природе, занимая второе место (после алюминия) среди металлов.
Железо имеет аллотропные модификации (см. рис. 4), которые различаются по кристаллической структуре или по магнитным свойствам. При температуре ниже 768 °С устойчиво ферромагнитное α-железо с объемноцентрированной кубической решеткой (ОЦК). При 768 °С (точка Кюри) железо становится парамагнитным, решетка остается той же. Между 911 и 1392 °С устойчиво γ-железо с гранецентрированной кубической решеткой. Выше 1392 °С вновь образуется ОЦК-решетка.
Железо является важнейшим металлом современной техники, хотя в чистом виде практически не используется по причине низких прочностных характеристик. Оно необходимо для жизнедеятельности многих живых организмов, в том числе и человека (входит в состав гемоглобина).
Способность железа растворять углерод и другие элементы служит основой для получения разнообразных сплавов, способных выдерживать воздействие высоких и низких температур, вакуума и высоких давлений, агрессивных сред, больших переменных напряжений, ядерных излучений и др. На долю таких сплавов приходится около 95 % всей металлической продукции (стали, чугуны, ферросплавы).
У г л е р о д (лат. Carboneum) химический элемент IV группы Периодической системы Менделеева, атомный номер 6, атомный радиус 0,077 нм, атомная масса 12,011, плотность 2,5 г/см3, температура плавления
3500 °С.
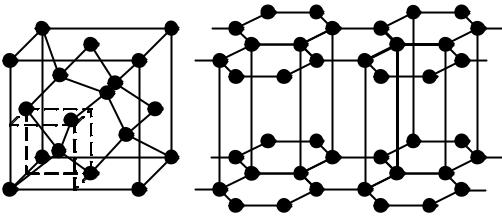
Основные кристаллические модификации углерода – алмаз и графит. В решетке алмаза все атомы углерода соединены между собой очень прочными связями и образуют в пространстве непрерывный трехмерный каркас (рис. 37, а). В графите атомы углерода располагаются параллельными слоями, причем атомы внутри слоя связаны между собой сильнее, чем один слой с другим (рис. 37, б).
Алмаз – диэлектрик, графит – хороший проводник электрического тока. Алмаз химически весьма стоек, графит при обычных условиях химически инертен, а при высоких температурах соединяется со многими элементами, является сильным восстановителем.
51
а б
Рис. 37. Кристаллические решетки: а – алмаза; б – графита
В соединениях с железом углерод приобретает металлические свойства. Он может растворяться в решетке железа по механизму внедрения, т. е. внедряться в межузельные пространства (поскольку атомный радиус углерода почти в два раза меньше, чем железа), а также образовывать химические соединения Fe3C; Fe2C и др.
Содержание углерода в земной коре 6,5·1016 т. Значительное количество (около 1013 т) входит в состав горючих ископаемых (уголь, природный газ, нефть и др.), а также в состав углекислого газа атмосферы (6·1011 т) и гидросферы (1014 т). Простейшие соединения углерода (диоксид углерода, метан) обнаружены в атмосфере почти всех планет Солнечной системы. Так, атмосфера Марса состоит в основном из диоксида углерода. Все организмы растений и животных построены из соединений углерода (средняя массовая доля углерода – 18 %).
Фазы системы Fe–Fe3C. Компоненты сплавов системы Fe–Fe3C образуют следующие фазы: жидкий раствор углерода в железе (ж), феррит (ф), аустенит (А) и цементит (ц).
Ф е р р и т (от лат. Ferrum железо) – твердый раствор внедрения углерода в α-железе, имеющем ОЦК-решетку. В ОЦК-решетке имеются свободные места (так называемые поры) размерами 0,062 нм. В работах исследователей предполагается, что меньшая часть атомов углерода в кристаллической решетке Feα находится в порах, а большая – на дефектах решетки (вакансиях, дислокациях). Максимальная растворимость углерода в низкотемпературном феррите составляет 0,02 % при 727 °С, а в высокотемпературном δ-феррите – 0,1 % при 1499 °С. При комнатной температуре феррит содержит 0,006 % углерода.
В феррите могут быть растворены кремний, марганец, фосфор и другие элементы. При t = 911…768 °С феррит парамагнитен, а от 768 °С до абсолютного нуля – ферромагнитен.
52
Феррит мягок, пластичен, имеет следующие свойства: σв = |
250 МПа; |
|||
δ = 50 %; ψ = 80 %; КСU = 2,5 МДж/м2; НВ 80. |
|
|
|
|
Микроструктура |
феррита представляет собой |
однородные зерна |
||
(рис. 38). |
|
|
|
|
А у с т е н и т |
(от имени английского |
|
|
|
ученого Робертса-Аустена) – твердый рас- |
|
|
|
|
твор углерода и других элементов в γ-желе- |
|
|
|
|
зе, имеющего ГЦК-решетку. Эта решетка в |
|
|
|
|
центре имеет пору диаметром 0,102 нм, в |
|
|
|
|
которой атом углерода с несколько боль- |
|
|
|
|
шим размером (0,154 нм) может поместить- |
|
|
|
|
ся, вызывая увеличение параметров γ-ре- |
|
|
|
|
шетки. При этом сам атом уменьшается в |
Рис. 38. Микроструктура ферри- |
|||
размерах, отдавая валентные электроны. |
||||
Искажение решетки ведет к уменьшению |
та, × 500 |
|
|
|
остальных ее пор, которые становятся не- |
|
|
|
|
доступными для других атомов углерода. |
|
|
|
|
На рис. 39 показана схема строения эле- |
|
|
|
|
ментарной ячейки аустенита, в которой |
|
|
|
|
растворен один атом углерода. Углерод в |
|
|
|
|
аустените находится в виде атомов, иони- |
|
|
|
|
зированных дважды. В то же время атомы |
|
|
|
|
железа ионизированы однократно. |
|
|
|
|
Максимальная растворимость углерода |
|
|
|
|
в аустените при t = 1147 °С равна 2,14 %. |
|
|
|
|
При снижении температуры растворимость |
Рис. 39. Кристаллическая ре- |
|||
уменьшается и при |
t = 727 °С составляет |
шетка аустенита: |
– атомы |
|
0,8 %. |
|
железа; |
– атом углерода |
|
|
|
|
|
|
При t = 727 °С вследствие аллотропиче- |
|
|
|
|
ского превращения Feγ → Feα и очень ма- |
|
|
|
|
лой растворимости углерода в α-железе |
|
|
|
|
аустенит распадается с образованием ме- |
|
|
|
|
ханической смеси феррита и цементита. |
|
|
|
|
Аустенит немагнитен, обладает по срав- |
|
|
|
|
нению с ферритом меньшим удельным |
|
|
|
|
объемом, пластичен (δ = 40…50 %), имеет |
|
|
|
|
твердость НВ 160…200. |
|
|
|
|
Микроструктура аустенита приведена на |
Рис. 40. Микроструктура аустени- |
|||
рис. 40. |
|
та, × 500 |
|
|
Ц е м е н т и т – химическое соединение железа с углеродом (карбид |
||||
железа Fe3C), содержит углерода 6,67 %, плотность 7,82 г/см3. |
|
|||
53
|
|
|
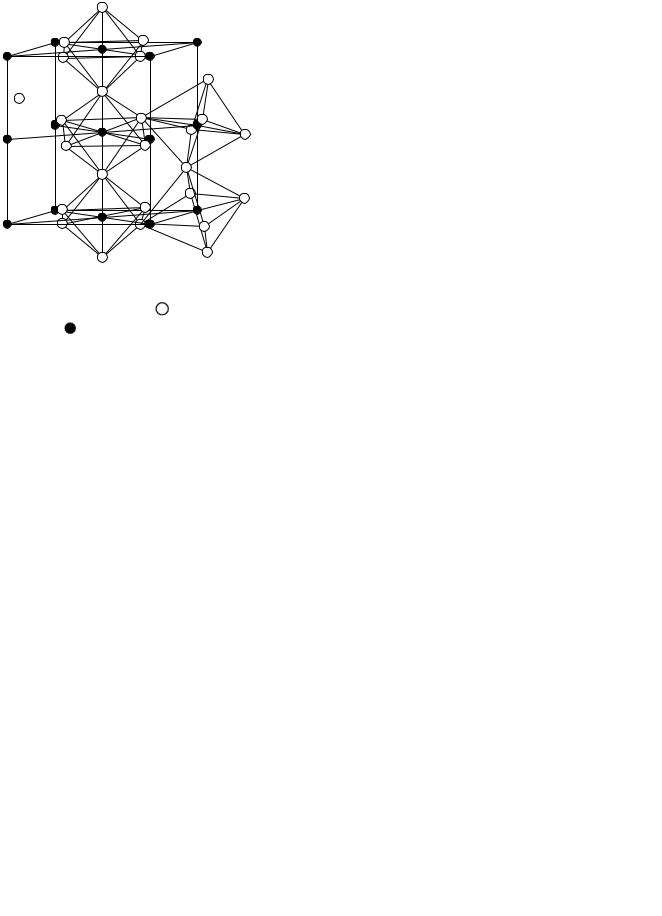
Кристаллическая |
решетка |
цементита |
|
|
|
очень сложная и состоит из ряда октаэдров, |
||
|
|
|
оси которых наклонены друг к другу (рис. 41). |
||
|
|
|
В вершинах октаэдров находятся атомы же- |
||
|
|
|
леза, каждый из которых принадлежит двум |
||
|
|
|
октаэдрам. Атом углерода находится в цен- |
||
|
|
|
тре октаэдра. |
|
|
|
|
|
Характер связи между атомами железа и |
||
|
|
|
углерода не установлен. Однако в кристал- |
||
|
|
|
лах цементита железо и углерод положи- |
||
|
|
|
тельно ионизированны, благодаря чему Fe3C |
||
|
|
|
характеризуется некоторыми металлически- |
||
|
|
|
ми свойствами (электропроводность, метал- |
||
Рис. 41. Кристаллическая ре- |
лический блеск). |
|
|
||
шетка цементита: |
– атомы |
Температура плавления цементита (око- |
|||
железа; |
– атомы углерода |
ло 1250 °С) точно не установлена, так как в |
|||
процессе нагрева он разлагается, что и искажает результаты измерений. |
|||||
Аллотропических превращений цементит не претерпевает, но при низ- |
|||||
ких температурах он слабо ферромагнитен. Магнитные свойства теряются |
|||||
при t = 727 °С. |
|
|
|
|
|
Цементит имеет высокую твердость (НВ > 800, царапает стекло), но |
|||||
очень низкую (практически нулевую) пластичность. |
|
|
|||
Он способен образовывать твердые растворы замещения. Атомы же- |
|||||
леза могут замещаться атомами других металлов (хрома, марганца, |
|||||
вольфрама, молибдена и др.), а атомы углерода – неметаллами (азотом, |
|||||
кислородом), т. е. образуется легированный цементит. Углерод в решетке |
|||||
цементита практически не растворяется. |
|
|
|||
Цементит неустойчив и при определенных условиях распадается на желе- |
|||||
зо и углерод в виде графита, что имеет очень важное практическое значение. |
|||||
В железоуглеродистых сплавах цементит может выделяться из жидкого |
|||||
раствора (в виде крупных равноосных зерен), из аустенита (в виде сетки по |
|||||
границам зерен) и из феррита (в виде очень мелких кристаллов по грани- |
|||||
цам зерен). В первом случае цементит называется первичным (Ц I), во вто- |
|||||
ром – вторичным (Ц II), в третьем – третичным (Ц III). Химические и физико- |
|||||
механические свойства всех трех типов цементита абсолютно одинаковы. |
|||||
Основные точки и линии диаграммы Fe-Fe3C. Приводимые на диа- |
|||||
грамме буквенные обозначения точек являются общепринятыми в между- |
|||||
народной практике (см. рис. 36). |
|
|
|||
Точка А (1539 °С) соответствует температуре плавления чистого желе- |
|||||
за, а точка D (≈1250 °С) – приблизительной температуре плавления це- |
|||||
ментита. При температуре 1392 °С (точка N) происходят полиморфные |
|||||
54
превращения Feα ↔ Feγ, а при t = 911 °С (точка G) – полиморфные превращения Feγ ↔ Feα.
Точка Р (727 °С) соответствует максимальному содержанию углерода
вα-железе, а точка Е (1147 °С) – максимальному содержанию углерода
вγ-железе.
При охлаждении аустенита с содержанием углерода 0,8 % в точке S (727 °С) происходит его распад на механическую смесь феррита (имеющего 0,02 % углерода) и цементита вторичного. Такая смесь называется перлитом (франц. perlite, от Perle жемчуг) и обозначается символом П:
А0,8 ↔ П (Ф0,02 + Ц II).
Следовательно, основными условиями образования перлита в железоуглеродистых сплавах являются содержание углерода в аустените 0,8 % и температура 727 °С.
Перлит чаще всего имеет пластинчатое строение и является прочной структурной составляющей: σв = 800…900 МПа, δ ≤ 16 %, НВ 180…220.
При охлаждении жидкого расплава с содержанием углерода 4,3 % в точке С (1147 °С) образуется механическая смесь аустенита с содержанием углерода 2,14 % и цементита первичного. Эта смесь называется ледебуритом (по имени немецкого металлурга А. Ледебура) и обозначается ин-
дексом Л: Л [А2,14 + ЦI].
При t = 20…25 °С ледебурит представляет собой смесь цементита и перлита. В этой структурной составляющей цементит образует сплошную матрицу, в которой размещены колонии перлита. Такое строение ледебурита служит причиной его большой твердости (НВ > 600) и хрупкости.
Линии диаграммы представляют собой семейство критических точек, в которых происходят какие-либо превращения в железоуглеродистых сплавах.
Линии АВСД и NJECF – соответственно линия ликвидус и линия солидус, показывают температуры начала и конца кристаллизации жидких сплавов. При температурах, соответствующих линии HJB, происходит перитектическое превращение. Линия МО (768 °С) указывает на температуру перехода феррита из магнитного состояния в немагнитное при нагреве и наоборот – при охлаждении. Это превращение не относится к разряду фазовой перекристаллизации. Линии GS и PG соответствуют температурам начала и конца полиморфного превращения феррита в аустенит при нагреве и аустенита в феррит – при охлаждении. Линии QP и SE указывают на предельную растворимость углерода в α- и γ-железе. Линия ECF (1147 °С) – семейство точек, при которых протекает эвтектическое превращение в сплавах. Эвтектика (от греч. eutektos легко плавящийся) – тонкая механическая
55
смесь твердых фаз, одновременно закристаллизовавшихся из расплава. При охлаждении сплава с содержанием углерода 4,3 % в точке С образуется чистая эвтектика – ледебурит. Этот сплав называют эвтектическим чугуном. Чугуны с содержанием углерода менее 4,3 % называются доэвтектическими, а при содержании более 4,3 % – заэвтектическими.
Линия PSK (727 °С) – линия эвтектоидного превращения. Эвтектоид – (от эвтектика и греч. eidos вид) аналогичная эвтектике структурная составляющая металлических сплавов, но в отличие от нее образующаяся не из жидкой, а из твердой фазы и потому имеющая более тонкое дисперсное строение. Так, при охлаждении аустенита с содержанием углерода 0,8 % в точке S образуется эвтектоид – тонкодисперсная механическая смесь феррита и цементита вторичного, называемая перлитом. Такой сплав именуется эвтектоидной сталью. Стали, имеющие углерода менее 0,8 %, называются доэвтектоидными, а более 0,8 % – заэвтектоидными.
Таким образом, в системе железо–цементит происходят три изотермических превращения:
– перитектическое на линии HJB (1499 °С)
Фн + Жв → АJ;
– эвтектическое на линии ECF (1147 °С)
Жс → [АЕ + ЦI];
– эвтектоидное на линии PSK (727 °С)
АS → (ФР + ЦII).
Рассмотрим превращения в железоуглеродистых сплавах, которые происходят при медленном охлаждении от температуры плавления.
3.1.3. Перитектическое превращение
Этот участок (левая верхняя часть диаграммы Fe-Fe3C) представлен отдельно на рис. 42.
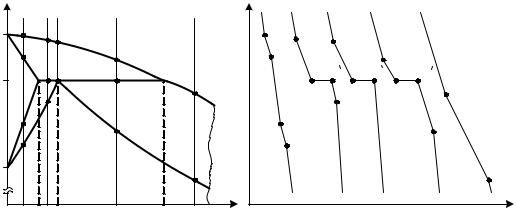
Из диаграммы видно, что кристаллизация сплавов с содержанием углерода до 0,5 % начинается по линии АВ (ликвидус). На перитектической горизонтали HJB происходит перитектическое превращение между жидкой фазой состава точки В (Ж0,5) и ферритом точки Н (Ф0,1). В результате образуется аустенит состава точки J (А0,16). Это превращение наглядно демонстрирует сплав III (содержание углерода 0,16 %), кристаллизация которого начинается в точке 8. При температуре ниже этой точки из жидкого расплава выделяются кристаллы высокотемпературного феррита. По мере понижения температуры, концентрация углерода в феррите изменяется по линии АН, а в жидкой фазе – по линии 8В, в чем можно убедиться, используя правило отрезков.
56
а |
I |
|
II |
III |
IV |
V |
б |
|
T,оС |
|
T,оС |
||||||
1539 |
А |
1 |
5 |
8 |
|
|
|
|
|
|
2 |
|
|
10 |
|
|
|
1499 |
Н 6 |
9 |
В |
13 |
||||
11 |
||||||||
|
ф |
|
7 |
J |
|
|
||
|
|
|
|
|
||||
|
3 |
|
12 |
|
|
|||
|
|
|
|
|
|
|||
1392 |
|
4 |
|
|
А |
|
|
|
N |
|
|
|
|
14 |
|
||
|
|
|
|
|
|
|
||
|
|
0,1 0,16 |
0,5 |
|
C,% |
|||
I |
|
II |
III |
|
IV |
V |
|
1 |
5 |
|
8 |
|
|
|
2 |
|
|
|
||
|
6 |
6 |
9 |
9 |
10 |
|
|
|
11 11 |
||||
|
|
|
|
7 |
|
13 |
|
|
|
|
|
|
|
|
|
3 |
|
|
|
12 |
|
|
4 |
|
|
|
|
|
|
|
|
|
|
14 |
|
|
|
|
|
|
Время |
Рис. 42. Перитектическое превращение в железоуглеродистых сплавах:
а – часть диаграммы Fe-Fe3C; б – схемы кривых охлаждения сплавов
Кристаллизация заканчивается при температуре 1499 °С (точка 9). При данной температуре феррит достигает концентрации углерода 0,1 %, а жидкость – 0,5 %. В результате происходит перитектическая реакция, при которой обе фазы полностью израсходуются и образуется аустенит с содержанием углерода 0,16 %
Ф0,1 + Ж0,5 ↔ А0,16.
Сп л а в II с содержанием углерода более 0,1 % и менее 0,16 % начинает кристаллизоваться в точке 5 с выделением кристаллов феррита. При достижении температуры 1499 °С (точка 6) сплав состоит из высокотемпературного феррита с концентрацией углерода 0,1 % и жидкой фазы с концентрацией углерода 0,5 %. Между этими фазами происходит перитектическая реакция с образованием аустенита состава точки J (0,16 % С). Но в связи с тем, что на перитектическую реакцию требуется количество феррита, равное JВ/НВ (согласно правилу отрезков), а в сплаве содержится его больше (6В/НВ), то часть феррита сохранится и по окончании перитектического превращения сплав будет состоять из аустенита и избыточного феррита, который при дальнейшем понижении температуры до точки 7 перекристаллизуется в аустенит. Ниже точки 7 сплав будет состоять только из аустенита.
Сп л а в IV с содержанием углерода более 0,16 % и менее 0,5 % начи-
нает кристаллизоваться при температуре, соответствующей точке 10. Из жидкого сплава выделяются кристаллы высокотемпературного феррита. При температуре 1499 °С (точка 11) в результате перитектической реакции образуется аустенит. Но так как на его образование требуется HJ/НВ жидкой фазы, а последней в сплаве содержится больше (Н11/НВ), то часть жидкой составляющей оказывается избыточной. В результате после перитектического превращения (точка 11) рассматриваемый сплав бу-
57
дет состоять из кристаллов аустенита и жидкой фазы, из которой при дальнейшем охлаждении до окончания кристаллизации (точка 12) выделяются кристаллы аустенита. В твердом состоянии сплав IV имеет структуру аустенита.
Сп л а в I перитектического превращения не претерпевает, так как содержание углерода в нем менее 0,1 %. В начале кристаллизации (точка 1) из расплава выделяются кристаллы высокотемпературного феррита. Кристаллизация заканчивается в точке 2. В интервале температур между точками 2 и 3 феррит охлаждается не претерпевая никаких превращений. Между температурами 3 и 4 происходит перекристаллизация по причине полиморфного превращения феррита в аустенит. Ниже температуры, соответствующей точке 4, сплав состоит только из аустенита.
Сп л а в V с содержанием углерода более 0,5 %. Такие сплавы перитектического превращения не претерпевают. В начале кристаллизации (точка 13) из расплава начинают выделяться кристаллы аустенита. Кристаллизация происходит в интервале температур, соответствующих точкам 13 и 14. При этом кристаллы аустенита имеют различную концентрацию углерода (изменяющуюся по линии J14). Ниже температуры окончания кристаллизации (точка 14) структура рассматриваемого сплава состоит только из аустенита.
Таким образом, все сплавы с содержанием углерода до 2,14 % (стали) после первичной кристаллизации имеют однофазную структуру – аустенит.
3.1.4. Эвтектоидное превращение
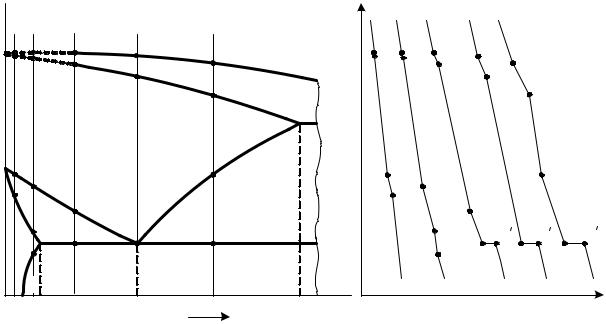
Рассмотрим превращения, происходящие в сталях при медленном охлаждении. Часть диаграммы, относящаяся к этим сплавам, приведена на рис. 43. Перитектическая часть не показана, так как была рассмотрена ранее.
С п л а в I с содержанием углерода менее 0,006 %. Сплавы с содержанием углерода менее 0,025 % называются технически чистым железом.
Кристаллизация сплава I начинается при температуре, соответствующей точке 1, и заканчивается в точке 2 образованием аустенита. В процессе кристаллизации состав жидкой фазы изменяется по линии ликвидус, а твердой (аустенит) – по линии солидус. Поэтому кристаллы аустенита, образовавшиеся в начале процесса кристаллизации, имеют концентрацию углерода, меньшую по сравнению с кристаллами, образующимися при более низкой температуре, т. е. аустенит формируется с переменным составом по углероду.
58
о |
I |
II |
III |
IV |
V |
|
|
T,оС |
I |
II |
III |
IV |
V |
|
|
T, С |
|
|
|
|
|
|
|
|
|
|
|||||
1539 |
1 |
5 |
10 |
14 |
16 |
|
|
|
1 |
5 |
10 |
14 |
16 |
|
|
2 |
6 |
|
|
|
|
|
2 |
6 |
11 |
|
|
|
|||
А |
11 |
|
|
|
|
|
15 |
|
|
|
|||||
|
|
|
15 |
17 |
|
|
|
|
|
|
|
17 |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
E |
1147 |
|
|
|
|
|
|
|
911 |
3 |
7 |
|
|
|
|
|
|
|
3 |
|
|
|
18 |
|
G |
4 |
12 |
|
18 |
|
|
|
|
|
7 |
|
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|
12 |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
8 |
13 |
|
19 |
727 |
|
|
|
|
8 |
|
13 |
S |
19 |
|
9 |
P |
S |
|
K |
|
|
9 |
|
||||||
|
|
|
|
|
|
|
13 |
|
S |
19 |
|||||
|
|
|
|
|
|
|
|
|
|||||||
600 |
Q |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,8 |
|
|
2,14 |
|
|
|
|
|
|
|
Время |
|
0,006 0,02 |
|
|
C,% |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 43. Часть диаграммы Fe-Fe3 С до 2,14 % С (стали) и кривые охлаждения сплавов
При очень медленном охлаждении в интервале температур между точками 2 и 3 происходит некоторое выравнивание состава за счет диффузии углерода. Однако этот процесс до температуры, соответствующей точке 3 (находящейся на линии GS), завершиться не успевает.
Как отмечалось ранее, линия GS соответствует семейству критических точек, в которых происходит смена решеток γ-железа в α-железо. Если в железе углерод отсутствует, то переход Feγ ↔ Feα совершается при температуре 911 °С (точка G). При наличии в железе углерода температура полиморфного превращения понижается по линии GS, а при концентрации 0,8 % (точка S) и более – по линии SK (727 °С). Ниже этой температуры в углеродистых сталях Feγ не существует.
Следовательно, в рассматриваемом сплаве I в точке 3 начинается выделение кристаллов феррита в составе аустенита, причем первыми полиморфное превращение претерпевают решетки аустенита с меньшим содержанием углерода. Так как растворимость углерода в феррите очень мала (при температуре точки 3 менее 0,006 % – линия PG), то его излишки вытесняются из решетки Feα и за счет диффузии перераспределяются в оставшемся аустените, который при этой температуре может растворить углерода около 2 % (линия SE). Таким образом, переход аустенита в феррит происходит во всем объеме не сразу, а в интервале температур 3–4. Поскольку к окончанию перекристаллизации (точка 4) феррит не достигает предельной концентрации, то до полного охлаждения никаких фазовых превращений в нем происходить не будет.
С п л а в II с содержанием углерода более 0,006 % и менее 0,02 %. От температуры начала кристаллизации (точка 5) и до температуры, соот-
59
ветствующей точке 8, в сплаве происходят процессы, аналогичные процессам, происходящим в сплаве I до линии PG. В результате структура состоит из чистого феррита. При охлаждении сплава до температуры 9, фазовых превращений в нем не происходит, но размеры решетки Feα уменьшаются. Поэтому при температуре, соответствующей точке 9, наступает предельная растворимость углерода в Feα (линия QP). По этой причине при дальнейшем понижении температуры, углерод из решетки феррита вытесняется и идет на образование мелких кристаллов цементита третичного (ЦIII), который выделяется по границам зерен феррита. Этот цементит понижает пластичность низкоуглеродистой стали, что отрицательно сказывается при холодной штамповке.
При ускоренном охлаждении выделение третичного цементита задерживается, и он может не выделиться совсем.
Сплавы с содержанием углерода более 0,02 %. Стали с указанным содержанием углерода характерны тем, что в них происходит эвтектоидное превращение (линия PSK, 727 °С). Эвтектоидное превращение состоит в распаде аустенита, содержащего 0,8 % С (точка S), на смесь феррита состава точки P (0,02 % С) и цементита вторичного (6,67 % С):
А0,8 ↔ Ф0,02 + Fe3C.
Точка S называется эвтектоидной точкой, а сталь с содержанием углерода 0,8 % – эвтектоидной сталью или перлитом (П). Стали с содержанием углерода до 0,8 % относятся к группе доэвтектоидных, а содержанием углерода более 0,8 % – к группе заэвтектоидных.
Рассмотрим подробнее эвтектоидное превращение при образовании перлита в эвтектоидной стали.
С п л а в IV – эвтектоидная сталь (С = 0,8 %).
Кристаллизация сплава начинается при температуре, соответствующей точке 14, и заканчивается в точке 15 с образованием аустенита. До температуры критической точки S (727 °С) сталь не претерпевает никаких фазовых превращений.
При температуре 727 °С (точка S) во всем объеме аустенита начинается эвтектоидное превращение, которое подчиняется общим законам кристаллизации и происходит путем образования центров кристаллизации феррита и цементита с последующим ростом кристаллов этих фаз.
В связи с тем, что углерод в аустените распределен неравномерно (наличие флуктуаций), появление центров кристаллизации существенно облегчается. При этом ведущей фазой при превращении является цементит, зародыши которого возникают по границам зерен аустенита. Зародыши зерен цементита растут в форме тонких пластин, направленных вглубь зерен аустенита. Для роста пластинки цементита необходимо, чтобы к ней диффундировал углерод из соседних участков. В результате аустенит, расположенный около пластинки, обедняется углеродом, перестраивается решетка (Feγ ↔ Feα), и в результате этого создаются условия для образо-
60
