
6ГЦ конд
.pdf
ЛЕКЦІЯ
Шестичлені ГЦ з одним ГА, що конденсовані з бензольним ядром
5 |
4 |
|
5 |
4 |
|
|
6 |
5 |
4 |
6 |
|
3 |
6 |
|
|
3 |
7 |
|
3 |
|
b |
|
|
|
|
|
|
|
|
7 |
a |
2 |
7 |
|
N |
2 |
8 |
|
2 |
N |
|
|
N |
||||||
|
|
|
|||||||
8 |
|
8 |
|
|
|
9 |
|
||
1 |
|
1 |
|
|
10 |
1 |
|||
|
|
|
|
|
|
|
|
||
хінолін |
|
ізохінолін |
|
|
|
акридин |
|
||
бензо[b]піридин бензо[c]піридин
Хінолін
Хінолін вперше виділили з кам’яновугільної смоли (Рунге, 1834 р.). Похідні – з нафти.
Цикл хіноліну – основна частина алкалоідів групи хініну. Хінолінові основи – безбарвні рідини з характерним запахом, летючі з водяною парою. Вони менш розчинюються в воді, ніж піридинові основи.
Методи здобування
Будова хіноліну підтверджується рядом його синтезів, з яких найважливіший – синтез Скраупа.
1)Синтез Скраупа – конденсація α, β – ненасиченого альдегіду (кетону) з
аніліном або з первинними ароматичними амінами, в яких ортоположення не зайнято. Реакція відбувається під дією H+ в присутності
[O]
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
O |
|
|
|
C |
|||||
+ H2C |
|
C |
|
C |
|
H |
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
[O] |
|
|
|
|
|||||||
|
|
|
|
|
|
|||||||||
|
|
H |
|
|
|
|
|
|
CH |
|||||
|
|
|
|
|
H |
|
|
|
||||||
NH2 |
|
|
|
|
|
|
|
N |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Механізм:
|
|
|
|
|
|
|
OH |
H |
|
|
|
|
|
OHC |
|
C |
|
OHC |
|
|
|
|
|
|
||
|
H |
|
|
CH |
2 H |
|
CH2 |
|
|
|
|
|
|
||||
+ |
CH |
|
|
|
|
|
||
|
|
|
|
|
|
|
||
|
CH2 |
|
|
|
CH |
2 |
|
CH2 |
NH2 |
|
|
|
|
|
N |
||
|
|
|
N |
|
|
|||
|
|
|
|
|
H |
|
|
H |
|
|
|
H |
|
|
|
|
|
|
|
|
C |
|
[O] |
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
-H2O |
|
|
|
CH2 |
|
|
|
|
-H+ |
|
|
N |
|
|
|
N |
|
|
|
|
H |
|
|
|
|
|

2
(H+ - H2SO4 або H3PO4; [O] – As2O5, R-NO2, що відповідає ароматичному аміну, який використовується в реакції. Амін, що утворюється при відновленні R-NO2, приймає участь в реакції на стадії конденсації).
FeSO4 – перенесення кисню, стримує бурне протікання реакції. В класичному синтезі хіноліну за Скраупом використовуються:
|
|
|
|
|
|
|
H2C |
|
H |
CH2 |
Ph-NO2 / FeSO4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
95% H2SO4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
OH OH OH |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кіпятять у зворотному |
|
|
|
|
η=84-91% |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
холодильнику |
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
||
H2C |
|
|
CH2 + H2SO4 |
|
|
|
|
H2C |
|
C |
|
CH |
|
|
|
|
|
H2C |
|
C |
|
C |
|
||||||||||||||
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
O |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
OH OH OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2)Реакція Дебнера-Міллера. Базується на реакції Скраупа а)
+ 2 H3C |
|
C |
O |
+ H SO |
|
t |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|||||
|
|
4 |
|
|
|
|
|
|
|
|||
|
|
|
H |
2 |
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
N |
CH3 |
||||
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H хінолідін |
||
Механізм:
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
O |
|||
2 H3C |
|
C |
|
|
|
H3C |
|
C |
|
C |
|
C |
|
|
||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
H |
|
|
|
|
H H |
H |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
OHC |
|
|
|
|
|
|
|
|
|
|
|
OHC |
|
|
|||||||
|
CH HCl |
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
||||||||
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ZnCl2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
||||
|
|
|
|
HC |
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
NH2 |
CH3 |
|
|
|
|
|
|
|
N |
CH3 |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
||||||
PhN=CH-CH3 |
PhNHCH3 |
+ |
N |
CH3 |
N |
CH3 |
H |
|
|
|

3
б)
H C |
|
C |
|
CH |
|
|
|
|
H SO |
|
|
|
H3C |
|
C |
|
C |
|
C |
|
CH3 |
||||||
+ |
3 |
|
|
|
|
|
|
3 |
+ H3C |
|
CHO |
2 |
4 |
|
|
+ |
|
|
H H |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||||||||
NH2 |
|
|
|
|
|
|
|
|
|
|
NH2 |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
CH3
N CH3
Властивості
0,958 |
0,772 |
|
0,989 |
|
0,978 |
0,917 |
|
0,789 |
|
N |
N |
1,003 1,633
Безбарвна ридина
1) |
Цикл; |
I. |
AE; |
|
2) |
Супряджений; |
II. |
SE в 8, 5, 6; |
|
III. |
SN в 2, 4 |
|||
|
|
3)4n+2=10 => n=2 I. Основність
1)H-X |
O2N |
( X - Cl-, HSO4-, NO3-,O 


 NO2 )
NO2 )
N |
O2N |
|
N |
H |
|
2)CH3I 




N I
I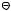
CH3
3)H2O2
CH3COOH
N
O

4
II.SE (в 6, 8 іноді 5)
1)Нітрування в бензольне ядро
NO2
|
HNO3 |
NO3 |
H2SO4 |
|
+ |
|
|
конц |
|
||
|
|
|
|
|
|
N |
|
N |
20оС, |
N |
N |
|
|
H |
1 година |
|
|
|
|
|
|
NO2 |
2) Сульфурування
220-230oC |
|
300oC |
H2SO4(к) |
|
N |
|
|
|
N |
SO3H |
SO3H |
|
|
|
300oC |
|
|
N
3) Ацилювання
|
|
|
|
R |
O |
|
|
|
|
|
C |
|
|
|
|
O |
|
|
RCOCl |
R |
C |
Cl |
|
|
|
|
|
||
N |
|
N |
|
|
N |
|
|
SO3H |
|
|
SO3H |
III.SN в 2
1)Амінування
|
NaNH2 |
|
|
|
|
130oC |
|
|
|
N |
N |
NH2 |
N |
NH |
|
|
|
H |
|
2) Оксилювання
KOH(тв)
250-260oC
N |
N |
OH |

5
3) Алкилювання
|
|
CH3Li |
|
|
|
|
|
-LiH |
|
|
|
|
N |
|
N |
CH3 |
|
H |
C O |
|
OH |
|
|
H |
|
|
|
||
|
|
-H2O |
|
C CH2 |
|
|
N |
C |
CH |
N |
|
|
|
H2 |
2 |
|
H |
|
Ph C OH |
|
|
||
|
|
|
|
|
|
|
N |
C |
C Ph |
|
|
|
|
H |
H |
|
|
бензилиденхінальдін
IV. |
Окислення |
|
|
|
|
|
COOH |
|
HNO3(KMnO4), t |
|
хінолінова |
|
сильні [O] |
|
кислота |
|
|
|
|
|
N |
N |
COOH |
V. |
Відновлення |
|
|
|
Na+C2H5OH |
|
H /Ni, 300oC |
|
|
2 |
|
|
N |
N |
N |
|
|
H |
H |
H2/Ni, 300oC
Хінолін використовують, як розчинник та вихідна речовина в синтезі лікарських речовин.
Похідні хіноліну
1) Хінальдін
N CH3
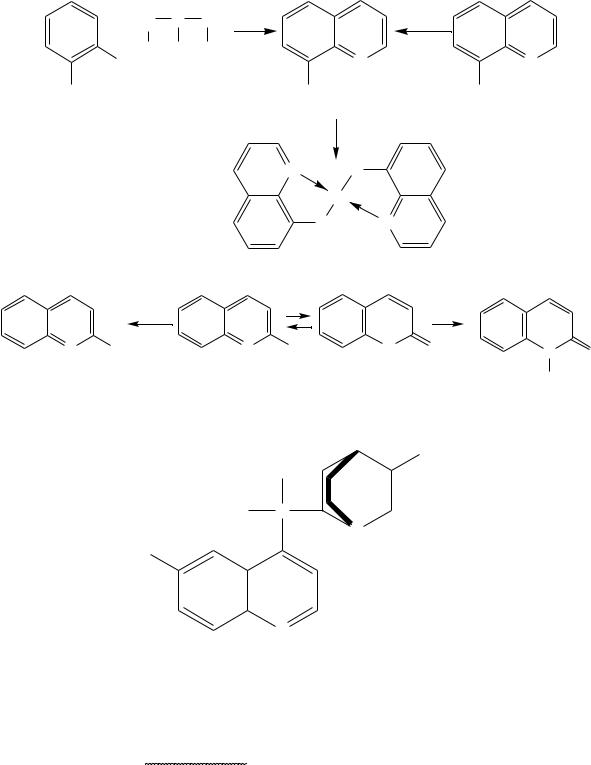
6
2) Оксин (8-оксіхінолін) – жовтувата кристалічна речовина
H C |
H |
CH2 |
|
|
|
|
|
C |
H SO |
KOH(тв) |
|
||||
+ |
2 |
|
|
2 |
4 |
|
|
|
|
|
|
|
t |
|
|
|
OH OH OH |
НБ |
|
|
|||
|
|
N |
N |
||||
NH2 |
|
|
|
|
|||
OH |
|
|
|
|
OH |
|
SO3H |
|
|
|
|
|
рКа=9,7(слабка кислота) |
|
|
|
|
|
|
|
|
MgCl2 |
|
|
|
|
|
|
|
2NaOH |
|
Нерозчинні комплекси |
|
|
N |
O |
|
||
з Ме (в аналітичній хімії) |
|
|
|
|
|
||
|
|
|
|
|
|
Mg |
|
|
|
|
|
|
O |
N |
|
3) α-ОН (α-NH2)хінолін – подвійна реакційна здатність
|
CH2N2 |
|
|
|
CH3J |
|
|
|
|
|
|
|
|
|
|
|
-N2 |
|
|
|
-HJ |
|
|
N |
OCH3 |
N |
OH |
N |
O |
N |
O |
|
|
|
|
H |
|
|
|
CH3
4) Хінін – для лікування малярії
H |
|
|
C |
|
CH2 |
|
||
|
||
OH |
|
|
H C
N
H3CO
N
Ізохінолін Добувають з кам’яновугільної смоли. Безбарвна речовина, Ттопл=23°С.
Схожа на хінолін. Більша кількість алкалоїдів – похідні ізохіноліну. Методи здобування
1.Реакція Бішлера-Напіральського – дегідратація ацильних похідних β- фенілетиламіну P2O5 в киплячому ксилолі

7
|
|
|
|
|
|
|
|
|
|
|
H2 |
|
|
|
|
|
|
|
|
H2 |
|
|
|
|
|
|
|
||
H2 |
|
|
|
|
|
O |
|
|
|
|
C |
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
||
|
|
R' |
|
C |
|
|
|
|
|
|
CH |
|
P O |
|
|
CH |
|
|
|
|
|
|
|
||||||
C |
|
|
|
|
|
H |
|
|
|
|
|
|
|
2 |
2 5 |
|
|
|
2 |
Pd |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
H |
N |
H |
N |
-H2 |
|
N |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
O |
|
C |
|
|
|
або POCl3 |
C |
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
R' |
|
|
|
|
|
R' |
2. |
Реакція Ц.Померанца, П.Фріч, 1893р. – конденсація |
|
||||||||||
|
аренкарбальдегіду з ацеталями α-аміноальдегідів з подальшою |
|
||||||||||
|
циклізацією пр.-ту |
|
|
|
|
|
|
|
|
|||
|
|
|
H |
|
OC H |
C2H5O |
|
OC2H5 |
|
|
||
|
|
|
|
2 |
5 |
H |
C |
|
|
|||
|
|
H2N |
C |
CH |
OC2H5 |
|
|
|
R |
|||
|
|
|
|
|
|
H CH |
R |
HX |
||||
|
|
|
R |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
N |
|
-2C2H5OH |
N |
|
C |
|
|
|
|
|
|
C |
|
|||
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Властивості |
|
|
|
|
|
|
5 |
4 |
|
|
|
|
|
|
|
|
|
|
6 |
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
I AE - 2 |
|
|
|
N |
2 |
|
|
|
|
|
|
II SE – 6(5, 7) іноді 4 |
|
|
7 |
|
|
|
|
|
|
|
|
|
III SN – в Py (1, 3) |
|
|
|
8 |
1 |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
||
AE |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HX |
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
N |
X |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
H |
|
(X - NO3, Cl, OSO3H) |
|
||
|
|
|
|
|
|
|
|
|
|
|||
pKBH+=5,14 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3X |
|
|
|
|
X |
|
|
|
|
|
|
|
-HX |
|
|
|
N |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
CH3COOH |
|
|
|
|
|
|
|
|
||
|
|
H2O2 |
|
|
|
N |
|
|
NO2 |
|
||
|
|
|
|
|
O |
|
|
|
|
|||
SE |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HNO3(к) |
|
|
|
|
|
+ |
|
|
|
|
|
|
H2SO4(к) |
|
|
|
|
N |
|
|
N |
|
|
|
|
O2N |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
SO3H |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
||
|
|
H2SO4 |
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
N |
|
|
|
HO3S |
|
|
|
|
|
|
|
|
|
|

8
S |
|
NaNH2 |
|
|
|
N |
|
|
|
|
NH |
|
N |
|
|
N |
|
|
|
|
NH2 |
NH |
|
|
|
KOH, t |
|
|
|
|
N |
|
|
N |
NH |
|
|
|
OH |
|
O |
|
CH3Li |
|
H2C=O |
|
|
N |
-HLi |
N |
NaOC2H5 |
N |
|
|
|
|
CH |
|
HC CH2 |
|
|
|
3 |
|
|
Окислення |
|
|
|
|
|
|
|
|
HOOC |
|
COOH |
|
|
HNO3(к) |
|
+ |
|
|
|
або KMnO4 |
|
||
|
N |
N |
|
||
|
|
|
|
||
|
|
|
HOOC |
|
COOH |
|
|
|
цинхомеронова |
фталева |
|
Відновлення |
|
|
|
|
|
|
|
H2/Ni |
|
H2/Ni |
|
|
N |
|
NH |
NH |
|
Похідні ізохіноліну Найважливіші з ізохінолінових алкалоїдів – алкалоїди опіуму. Опій –
це суміш, до якої надходять папаверин(1%), наркотин (9-10%) та інші похідні бензилізохіноліну.
1) Папаверін
H3CO
N
H3CO
CH2
OCH3
OCH3

2) Морфін
CH3
N
RO |
O |
|
OR' |
||
|
R=R’=H (безбарвна кристалічна речовина)
3)Кодеїн
R=CH3; R’=H
4)Героїн (солянокислий диацетилморфін) R=R’=COCH3
|
|
|
Акридин |
|
|
|
AE – 10; SE – 1, 3, 7, 9; SN - 5 |
||||
6 |
5 |
4 |
|
0,94 |
0,70 |
7 |
|
3 |
1,00 |
|
|
|
|
|
|
|
|
8 |
N |
2 |
0,92 |
|
N |
9 |
1 |
|
|
||
10 |
|
|
|
||
|
|
|
|
1,01 |
1,71 |
|
|
Здобування |
|
||
CH3 |
|
|
COOH |
|
P2O5 |
1) |
KMnO4 |
H |
|
||
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
або H2SO4 |
|
N |
|
|
N |
|
|
H |
|
|
H |
|
|
H |
OH |
|
|
H |
Cl |
|
|
PCl5 |
|
|
|
|
|
-POCl3 |
|
|
|
|
N |
|
|
N |
|
|
H |
|
|
H |
|
H |
H |
|
|
|
|
|
|
[O] |
|
|
|
|
|
FeCl3 |
|
|
|
|
N |
|
|
N |
|
|
H акрідан |
|
|
|
|
|
H |
H |
|
|
|
2) |
O |
|
|
|
|
+ HC |
+ |
|
-NH3 |
|
|
|
OH |
|
|
H2N |
|
H N |
NH |
H N |
NH |
-2H2O |
|
2 |
2 |
2 |
2 |
|
|
9
0,94
 1,00
1,00
0,92
1,01
O
C
SnCl2
HCl
N
H акрідон
[H]
Na/Hg+
-HCl
N |
NH2 |

Властивості Слабка основа, АЕ – HX, RX, CH3COOH/H2O2
COOH HOOC
KMnO4 |
KMnO4 |
|
N |
N |
COOH |
HOOC |
N |
|
Na/C2H5OH
N |
N |
|
|
H |
|
|
|
O |
|
O |
|
K2Cr2O7+ |
+ |
N |
|
|
|
CH3COOH |
|
N |
N |
|
|
N |
|
|
|
|
|
|
H |
|
|
|
O |
|
C4H9 |
|
н-C4H9Li |
|
|
N |
N |
|
|
Li |
|
|
NH4 |
|
NaNH2 |
|
|
N |
N |
|
Похідні акридину 1. Акріхін – ліки від малярії
|
|
|
CH3 |
|
|
|
|
|
|
|
(CH2 |
)3 |
N(C2H5)2 |
HN |
|
C |
||||
|
||||||
|
|
H |
|
|
|
|
H3CO
N |
Cl |
10
COOH
COOH
2. Ріванол – антисептик, від дезентирії
