
- •Министерство образования российской
- •Содержание
- •От авторов
- •Молекулярная физика и термодинамика
- •11.1. Молекулярная физика и термодинамика. Основные положения и понятия. Динамические и статистические закономерности. Статистический и термодинамический методы исследования
- •11.2. Молекулярно-кинетическая теория
- •11.2.1. Модель идеального газа. Основное уравнение кинетической теории газов
- •11.2.2. Вывод основных газовых законов молекулярно кинетической теории
- •11.2.2.1. Закон Бойля-Мариотта
- •11.2.2.2. Закон Гей-Люссака
- •11.2.2.3. Закон Шарля
- •11.2.2.4. Объединенный газовый закон Мариотта - Гей-Люссака
- •11.2.2.5. Основное уравнение состояния идеального газа (уравнение Менделеева-Клапейрона)
- •11.2.2.6. Закон Авогадро
- •11.2.2.7. Закон Дальтона
- •11.3. Молекулярно-кинетический смысл абсолютной температуры
- •11.4. Экспериментальное подтверждение молекулярно-кинетической теории газов (опыт Штерна)
- •12.1. Распределение энергии по степеням свободы
- •12.2. Вероятность и флюктуации. Распределение молекул (частиц) по абсолютным значениям скорости. Распределение Максвелла. Скорости теплового движения частиц. Средняя длина свободного пробега молекул
- •12.3. Распределение Больцмана. Барометрическая формула
- •12.4. Внутренняя энергия и теплоемкости идеального газа. Классическая теория теплоемкостей
- •Формулы кинетической энергии молекул газа в зависимости от числа степеней свободы
- •13.1. Первое начало термодинамики
- •13.1.1. Первое начало термодинамики в применении к изопроцессам в идеальных газах
- •13.1.1.1. Изотермический процесс
- •13.1.1.2. Изобарический процесс
- •13.1.1.3. Изохорический процесс
- •13.1.1.4. Адиабатический процесс
- •13.2. Обратимые, необратимые и круговые процессы (циклы)
- •13.3. Цикл Карно. Максимальный кпд тепловой машины
- •13.4. Энтропия системы и её свойства. Определение изменения энтропии системы, совершающей какой-либо изопроцесс
- •1. Изотермический.
- •2. Изобарический.
- •3. Изохорический.
- •4. Адиабатический.
- •13.5. Второе начало термодинамики. Термодинамические потенциалы
- •13.5.1. Второе начало термодинамики
- •13.5.2. Термодинамические потенциалы
- •13.6. Третье начало термодинамики. Применения термодинамики
- •14.1. Термодинамика неравновесных процессов
- •14.2. Закон сохранения массы в термодинамике неравновесных процессов
- •14.3. Закон сохранения импульса в термодинамике неравновесных процессов
- •14.4. Закон сохранения энергии в термодинамике неравновесных процессов
- •14.5. Уравнение баланса энтропии
- •15.1. Реальные газы. Молекулярные силы. Уравнение Ван-дер-Ваальса. Изотермы Ван-дер-Ваальса и экспериментальны изотермы реальных газов
- •Критическая температура и температура кипения некоторых жидкостей
- •15.2. Внутренняя энергия реального газа
- •15.3. Эффект Джоуля - Томсона. Сжижение газов
- •15.4. Фазы и фазовые превращения. Фазовые диаграммы. Условия равновесия фаз
- •15.5. Уравнение Клапейрона-Клаузиуса. Метастабильные состояния. Критическая точка
- •15.6. Тройная точка. Фазовые переходы 1-го и 2-го рода
- •16.1. Понятие о физической кинетике. Вязкость жидкостей и газов. Коэффициент вязкости жидкостей и газов. Динамическая и кинематическая вязкости
- •16.2. Диффузия и теплопроводность. Коэффициенты диффузии и теплопроводности
- •Кинетические явления (явления переноса). Переносимая величина, уравнение процесса, коэффициент процесса
- •17.1. Строение жидкостей
- •17.2. Свойства жидкостей (вязкость, текучесть, сжимаемость и тепловое расширение)
- •17.3. Поверхностное натяжение. Энергия поверхностного слоя жидкости
- •17.4. Поверхностные явления на границе раздела двух жидкостей или жидкости и твердого тела
- •17.5. Капиллярные явления. Закон Жюрена
- •17.6. Кинематическое описание движения жидкости
- •17.7. Уравнения равновесия и движения жидкости. Стационарное движение идеальной жидкости. Уравнение Бернулли
- •17.8. Гидродинамика вязкой жидкости. Силы внутреннего трения. Коэффициент вязкости. Стационарное течение вязкой жидкости. Уравнение неразрывности. Течение по трубе. Формула Пуазейля
- •17.9. Жидкие кристаллы
- •17.9.1. Строение жидких кристаллов (жк)
- •17.9.2. Физические свойства жидких кристаллов и их применение
- •17.10. Магнитные жидкости
- •17.10.1. Структура магнитных жидкостей (мж)
- •17.10.2. Получение магнитных жидкостей
- •17.10.3. Свойства магнитных жидкостей
- •17.10.4. Применение магнитных жидкостей
- •17.11. Кристаллическое состояние
- •17.11.1. Отличительные черты кристаллического состояния
- •17.11.2 Классификация кристаллов
- •17.11.3 Физические типы кристаллических решеток
- •17.11.4 Тепловое движение в кристаллах. Теплоемкость кристаллов
- •17.11.5. Скорость звука в кристалле. Цепочечная модель
- •Можно записать дифференциальное уравнение
- •Библиографический список Основной
- •Дополнительный
- •Полунин Вячеслав Михайлович
- •Сычев Геннадий Тимофеевич
- •Конспект лекций по молекулярной физике и термодинамике для студентов инженерно-технических специальностей
13.3. Цикл Карно. Максимальный кпд тепловой машины
Н аиболее
совершенным в отношении КПД является
цикл Карно, который состоит из двух
изотерм (1-2, 3-4) и двух адиабат (2-3, 4-1)
(рис.13.6).
аиболее
совершенным в отношении КПД является
цикл Карно, который состоит из двух
изотерм (1-2, 3-4) и двух адиабат (2-3, 4-1)
(рис.13.6).
Пусть один моль или киломоль идеального газа в состоянии 1 имеет параметры p1, V1, T1.
После
изотермического перехода из состояния
1 в состояние 2, его параметры изменяются
p2,
V2,
T1,
при этом он совершает работу, которая
численно будет равна количеству тепла,
подводимому к системе
![]()
![]() (13.32)
(13.32)
При адиабатическом расширении из состояния 2 в состояние 3 газ, совершив работу за счет изменения внутренней энергии, приобретет параметры p3, V3, T2. При этом
![]() (13.33)
(13.33)
Для возвращения системы в первоначальное состояние необходимо газ изотермически сжать при температуре T2 до объема V4. А это возможно только в том случае, если от системы отбирается некоторое количество тепла Q2, равное работе над системой
![]() (13.34)
(13.34)
При этом параметры газа станут равными p4, V4, T2. Затем сжать адиабатически из состояния 4 в состояние 1. В этом случае, за счет работы, совершаемой над газом, произойдет увеличение внутренней энергии газа на величину
![]() (13.35)
(13.35)
Разность между работой, совершенной системой при расширении, и работой, совершенной над системой при ее сжатии, будет равна работе цикла Карно
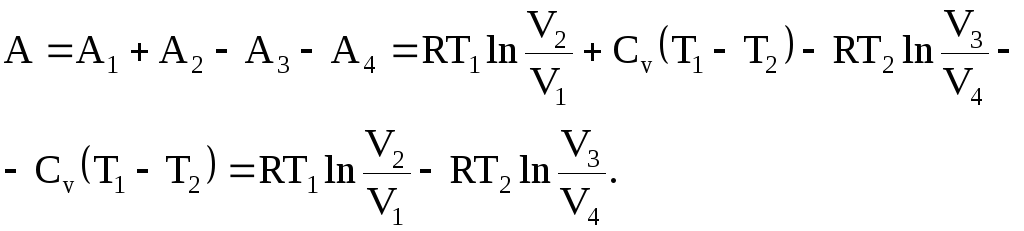 (13.36)
(13.36)
Тогда цикла Карно
![]() (13.37)
(13.37)
О бъемы
V2
и V3,
V1
и V4
лежат на соответствующих адиабатах,
следовательно, согласно уравнениям
Пуассона
бъемы
V2
и V3,
V1
и V4
лежат на соответствующих адиабатах,
следовательно, согласно уравнениям
Пуассона
![]()
![]()
Таким образом
![]() (13.38)
(13.38)
Из полученного соотношения видно, что цикла Карно не зависит от природы вещества, а зависит лишь от температур, при которых теплота, сообщается системе и отбирается от нее.
Коэффициент полезного действия цикла Карно стремится к единице при возрастании T1 и стремлении к нулю температуры T2.
За цикл Карно часть тепла отбирается от внешнего по отношению к системе тела - нагревателя и передается системе. Часть ее превращается в работу, часть - отдается холодильнику. Такой цикл Карно встречается в тепловых машинах (рис. 13.7).
Надо иметь в виду, что цикл Карно обратим, что используется в холодильных машинах. В этом случае в результате совершения работы удается перевести некоторое количество теплоты от тела более холодного к телу более нагретому. Коэффициент полезного действия холодильной машины (холодильника)
![]() (13.39)
(13.39)
Кроме
цикла Карно в технической термодинамике
применяются цикл Отто, состоящий из
двух адиабат и двух изохор, и цикл Дизеля,
с остоящий
из двух адиабат, изохоры и изобары
(рис.13.8).
остоящий
из двух адиабат, изохоры и изобары
(рис.13.8).
13.4. Энтропия системы и её свойства. Определение изменения энтропии системы, совершающей какой-либо изопроцесс
Известно, что внутренняя энергия системы является функцией ее состояния. Характеристикой различных термодинамических процессов является энтропия. Энтропия системы физическая величина, элементарное изменение которой при переходе системы из одного состояния в другое равно полученному или отданному количеству теплоты, деленному на температуру, при которой произошел этот процесс. Энтропия, подобно внутренней энергии, является однозначной функцией состояния системы.
Бесконечно малое изменение энтропии определяется соотношением
![]() (13.40)
(13.40)
При переходе системы из одного состояния в другое, изменение энтропии можно рассчитать так
![]() (13.41)
(13.41)
На основании первого начала термодинамики
![]()
тогда
![]()
а
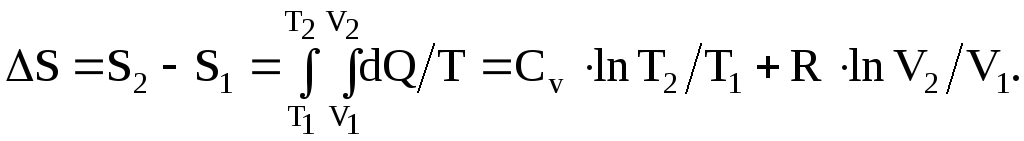 (13.42)
(13.42)
Зная общую формулу для расчета изменения энтропии можно рассчитать изменение энтропии, если система совершает какой-либо изопроцесс, например:
