
- •Макроструктурный анализ
- •Анализ диаграмм состояния двойных сплавов
- •Анализ диаграммы состояния железо-цементит, изучение микроструктуры и свойств углеродистых сталей
- •Изучение структуры чугунов
- •Влияние термической обработки на структуру и свойства углеродистой стали 40
- •Основы термической обработки
Анализ диаграмм состояния двойных сплавов
Цель работы: установить связь между диаграммами состояния, структурой и свойствами сплавов.
План работы
1. Выполнить анализ диаграмм состояния сплавов Рb - Sb и Сu-Ni.
2. Построить кривые охлаждения заданных сплавов.
3. Исследовать микроструктуры сплавов.
Пояснении к работе
Диаграмма состояния системы сплавов представляет собой графическое изображение состояния сплава в зависимости от температуры и концентрации.
Диаграммы состояния строятся экспериментальным путем в координатах состав сплава - температура, Для их построения используется ряд анализов, основные из которых: термический, химический, микроструктурный, рентгеноструктурный. При термическом анализе получают кривые охлаждения в координатах температура - время (рис. 1). Если при охлаждении в исследуемой системе не происходит изменений в строении, то кривая получается плавной, без перегибов (рис. 1,а), В случае охлаждения чистого металла (рис. 1,б) происходящая кристаллизация сопровождается выделением скрытой теплоты, которая полностью компенсирует теплоотвод в окружающее пространство, и температура остается постоянной в течение времени кристаллизации, т. е. чистый металл кристаллизуется при постоянной температуре. Такой же вид имеет кривая охлаждения сплава—смеси эвтектического состава. После завершения кристаллизации температура понижается.
Двойные сплавы в отличие от чистых металлов кристаллизуются в интервале температур. При кристаллизации твердого раствора на кривой охлаждения имеются точки перегиба (рис. 1,в). Кривая охлаждения
сплава—механическая смесь (рис. 1,г) имеет горизонтальный участок,
что соответствует кристаллизации эвтектики.
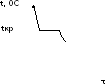
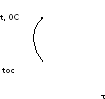
а) б)
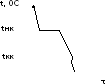
в) г)
Рис. 1 Кривые охлаждения
Точки перегиба на кривых охлаждения соответствуют критическим точкам. Критическая точка - это температура, соответствующая структурным превращениям и сплаве. В обоих случаях верхние критические точки соответствуют началу кристаллизации, а нижние — концу.
Пример построения диаграммы состояния приведен на рис. 2. На кривых охлаждения (рис. 2, а), построенных для сплавов с различной концентрацией компонентов, отмечают критические точки. Эти точки переносят на координатную сетку диаграммы состояния (рис. 5,б). Соединив точки начала и конца кристаллизации, получают линии ликвидус и солидус.
Таким образом, линия ликвидус - геометрическое место точек начала кристаллизации при охлаждении и конца плавления при
нагреве. Линия солидус—геометрическое место точек конца кристаллизации при охлаждении и начала плавления при нагреве.
Выше линии ликвидус сплав находится в жидком состоянии Ж, ниже линии солидус—в твердом (αтв). Между линиями ликвидус и солидус сплав находится в полужидком состоянии (имеются жидкая и твердая фазы).
Анализ диаграммы состояния сплава проводится с помощью правил фаз и отрезков. Для проведения анализа необходимо изучить следующие понятия и определения.
Сплав — сложное вещество, полученное в результате сплавления двух или более компонентов.
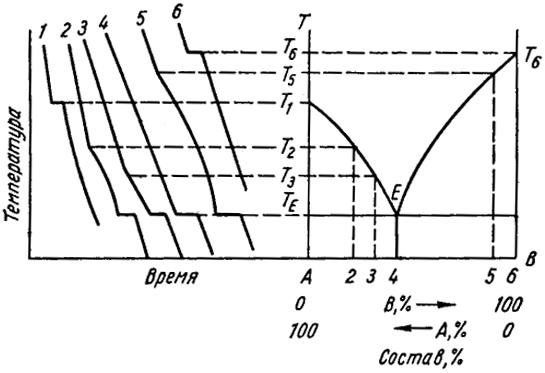
а) б)
Рис. 2. Построение диаграммы состояния по кривым охлаждениям
Компонент—составляющая сплава, им могут быть химические элементы или устойчивые химические соединения.
Система — совокупность веществ в твердом, жидком и газообразном состояниях, при известных условиях (температура, давление), занимающая определенный объем. Системы, состоящие из одного химического элемента или соединения. называют простыми, а из нескольких — сложными.
Эвтектика — мелкозернистая смесь, состоящая из двух или более
фаз, кристаллизующихся одновременно при постоянной температуре из жидкой фазы, имеющая определенный состав и наименьшую для данного сплава температуру плавления.
Фаза — однородная внутри тебя часть системы, отделенная от других частей (фаз) поверхностью раздела, при переходе через которую строение и свойства меняются скачками.
Число степеней свободы (вариантность) системы — число внешних (температура, давление) и внутренних (концентрация) факторов, которое можно изменять без изменения числа равновесных фаз в системе.
Правило фаз (закон Гиббса) дает количественную связь между степенью слободы системы и количеством фаз и компонентов для получения равновесного состояния. Правило фаз можно выразить уравнением С=К - Ф+2, где С — число степеней свободы; К — число компонентов; Ф — число фаз; 2 — внешние факторы равновесия (температура, давление). Если принять, что превращения в сплавах практически происходят при постоянном давлении, тогда правило фаз принимает вид
С=К - Ф+1
Если число степеней свободы С=0 — система безвариантна, при этом нельзя изменить внешний (температуру) или внутренний (концентрацию) факторы без того, чтобы это не вызвало изменения числа фаз. Кристаллизация в данном случае происходит при постоянной температуре.
Если число степеней свободы С=1 — система одновариантна, при этом изменение одного из факторов равновесия не вызывает изменения числа фаз. Процесс кристаллизации протекает при понижающейся температуре.
Если число степеней свободы С=2 — система двухвариантна, возможно изменение обоих факторов равновесия без изменения числа фаз.
Правило отрезков применяется в двух случаях: для нахождения состава фаз и для определения их количественного соотношения.
В первом случае для нахождения состава фаз через точку, характеризующую состояние системы, проводят горизонтальную линию (каноду) до пересечения с линиями, огранивающими данную область диаграммы состояния. Проекции точек пересечения на ось концентрации показывают состав фаз.
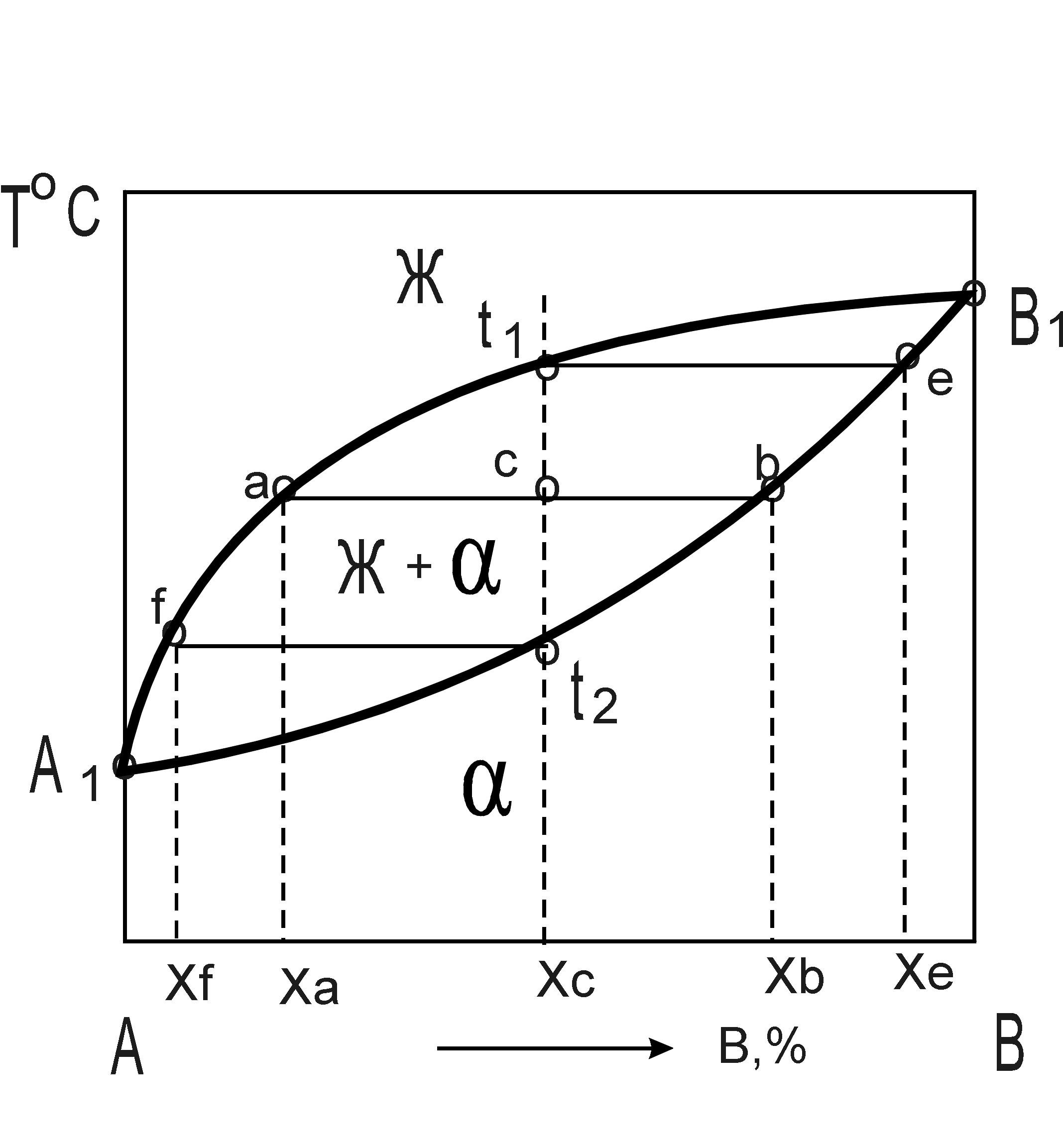
Рис. 3. Определение состава и количественного соотношения фаз с помощью правила отрезков
В приведенном примере (рис. 3) для сплава в состоянии точки «с», проведя линию аb, получаем, что состав твердой фазы соответствует проекции точки b, состав жидкой фазы — проекции точки а.
Количественное соотношение фаз обратно пропорционально отрезкам, прилегающим к точкам, определяющим состав этих фаз. В данном примере отношение количества твердой фазы Qтв к количеству жидкой фазы Qж обратно пропорционально отношению отрезков bc и ca: Qтв/ Qж= ca/ bc.
Если требуется определить долю твердой (или жидкой) фазы во всем сплаве, то соотношение будет иметь следующий вид:
Qтв/ Qспл= ac/аb
Анализ диаграммы состояния системы свинец — сурьма
Сплав Рb — Sb относится к сплавам механическим смесям. Это сплавы, компоненты которых полностью растворимы в жидком состоянии и практически нерастворимы в твердом, т. е. рядом с зернами одного компонента находятся зерна другого.

Рис. 4. Диаграмма состояния системы свинец—сурьма
Линия СЕD — ликвидус, выше этой линии находится область жидкого однофазного состояния. Линия FЕG – солидус, ниже которой сплав находится в твердом двухфазном состоянии—смесь кристаллов свинца и сурьмы.
При охлаждении сплавов различной концентрации по линии СЕ из жидкого расплава выделяются кристаллы свинца. По линии ЕD жидкого расплава выделяются кристаллы сурьмы.
На линии FЕG происходит образование эвтектики, т.е. из жидкой фазы состава точки Е(13%Sb)| одновременно при постоянной температуре выделяются дисперсные кристаллы свинца и сурьмы, поэтому линия FЕG называется линией эвтектического превращения. На ней в равновесии находятся три фазы: жидкая, кристаллы свинца и сурьмы. Точка Е называется эвтектической, сплав
состава точки Е—эвтектическим (Э). Сплавы с содержанием сурьмы менее 13% называется доэвтектическими (Э+Pb), более 13% заэвектическими (Э+Pb).
Для выявления закономерности образования структуры рассмотрим процесс кристаллизации заэвтектического сплава 1 (рис. 4). При охлаждении его до температуры точки 1 сплав находится
в жидком состоянии. При температуре t1 начинается кристаллизация сурьмы, этот процесс продолжается до температуры t2, соответствующей линии эвтектического превращения. При охлаждении сплава в интервале t1-t2 происходит его качественное изменение: в результате выпадения кристаллов сурьмы жидкая фаза обедняется сурьмой (до 13%) и обогащается свинцом. Согласно правилу состав жидкой фазы меняется в соответствии с линией ликвидус от точки 1 при температуре t1 до точки Е при температуре t2. .На линии FЕG кристаллизация сурьмы заканчивается, и затем из оставшейся жидкости состава точки Е происходит образование эвтектики Э.
Описанный процесс кристаллизации можно записать в следующем виде:
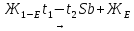 ;
;
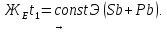
После кристаллизации сплав I будет состоять из двух структурных составляющих: крупных кристаллов сурьмы и эвтектики, представляющей мелкозернистую смесь кристаллов сурьмы и свинца. Структурной составляющей называют обособленную часть структуры, имеющую при данном увеличении микроскопа однообразное строение.
В доэвтектических сплавах в интервале температур от линии: ликвидус до линии солидус из жидкой фазы выпадают кристаллы свинца и жидкость, обогащается сурьмой (до 13%) и обедняется свинцом. Доэвтектические сплавы после затвердевания состоят также из двух структурных составляющих: крупных кристаллов свинца и эвтектики.
Сплав эвтектического состава кристаллизуется при постоянной
температуре, без предварительного образования кристаллов сурьмы и свинца. После затвердевания он состоит из одной структурной составляющей—эвтектики.
Имея диаграмму состояния системы, можно, пользуясь правилом фаз, построить кривую охлаждения сплава любой заданной концентрации. На рис. 4 дан пример построении кривой охлаждения для сплава I.
Анализ диаграммы состояния системы медь—никель
Сплав Сu —Ni относится к сплавам—твердым растворам. Компоненты такого сплава имеют неограниченную растворимость как в жидком, так и твердом состояниях, т. е., смешиваясь между собой, образуют один тип кристаллической решетки. Общий вид диаграммы приведен на рис. 5. Линия асв на диаграмме состояния Сu – Ni называется ликвидус. Выше этой линии все сплавы данной системы находятся в жидком состоянии. Линия адв называется солидус ﴿. Ниже этой линии все сплавы находятся в твердом состоянии. Между ликвидусом и солидусом одновременно находятся две фазы: жидкий и твердый растворы. Чтобы охарактеризовать фазовое состояние конкретного сплава при заданной температуре, необходимо определить природу фаз, находящихся в равновесии при данной температуре, их химический состав и относительное количество. Для примера рассмотрим изменение фазового состояния, происходящее при снижении температуры в сплаве, содержащем 30 % Ni и 70 % Сu.
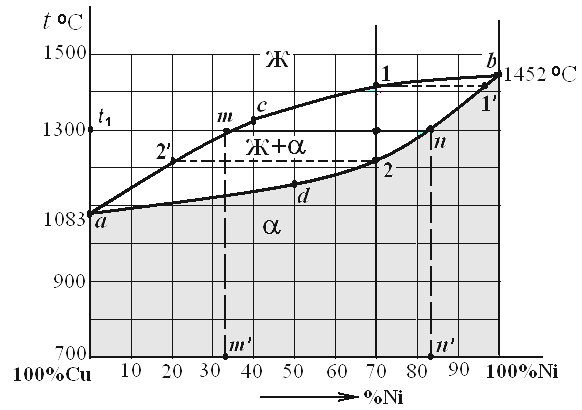
Рис. 5. Диаграмма состояния системы «медь – никель»
Для определения фазового состояния сплава в интервале кристаллизации применяют правило отрезков. Например, при произвольно выбранной температуре t1 через точку, лежащую на ординате сплава, проводят горизонтальную линию - изотерму - до пересечения с ближайшими линиями диаграммы.
Точки пересечения укажут, какие фазы находятся в равновесии у данного сплава при t1 : m – соответствует жидкому раствору, n – твердому раствору α. По проекциям точек пересечения на ось концентрации определяют химические составы равновесных фаз: в жидкой фазе содержится оm' % Ni (остальное – Сu); в α-фазе - оn' % Ni (остальное – Сu).
Количественное соотношение равновесных фаз определяют по отрезкам: количество жидкой фазы пропорционально кn, а α-фазы -mk . Линию mn называют конодой.
При охлаждении сплава из жидкого состояния ниже точки 1, лежащей на линии ликвидус, начинается кристаллизация. При переходе через точку 2 на линии солидус кристаллизация заканчивается. В процессе кристаллизации концентрация компонентов в жидком растворе изменяется согласно ликвидусу от точки 1 до точки 2', а в растворе α – согласно солидусу от точки 1' до точки 2.
После окончания кристаллизации структура сплава состоит из зерен твердого раствора α, имеющих одинаковый состав. Поскольку сплав был выбран произвольно, то рассуждения о формировании его структуры применимы к любому сплаву этой системы, кроме чистых Cu и Ni.
Применение сплавов
Сплавы – смеси применяются в качестве:
Литейных, т.к. они обладают хорошей жидкотекучестью, из-за наличия в их составе эвтектики.
Припоев для пайки.
Тепловых предохранителей, т.к. сплавы при любой концентрации имеют одинаковую температуру начала плавления, что обеспечивает точность срабатывания предохранителей при повышении температуры в помещении до заданных значений.
Типографских шрифтов (доэвтектический сплав Pb-Sb)
Подшипников скольжения (баббиты), состоящие из
мягкой основы – эвтектики и твердых включений, мягкая основа обеспечивает хорошую прирабатываемость подшипника к валу, а твердые включения—высокую износостойкость.
Сплавы – твердые растворы применяются в качестве:
Коррозионностойких (нержавеющих), что обеспечивается их однофазной структурой;
Электросопротивлений, реостатной проволоки (Сu - Ni, Ni - Мn), нагревательных элементов электроприборов (Ni - Сr, Fе-Сr). Высокое электросопротивление имеет место из-за наличии в кристаллической решетке металла—растворителя чужеродных атомов растворенного металла.
Микроструктуры сплавов:
Pb – Sb



х135 х135 х135
доэвтектический (Pb+Э) эвтектический (Э) эвтектический (Pb+Э)
Сu – Ni

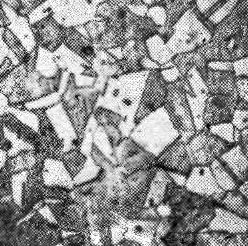
х135 х135
литой деформированный и отожженный
Задание. Построить кривую охлаждения для сплаваPb–Sbзаданной концентрации
|
Вари- ант |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
21 |
22 |
|
Sb, % |
1,5 |
5 |
9 |
12 |
15 |
18 |
19 |
25 |
29 |
36 |
42 |
59 |
65 |
69 |
73 |
82 |
86 |
92 |
95 |
2,5 |
10 |
100 |
ЛАБОРАТОРНАЯ РАБОТА № 4
